Гормонорезистентный рак что это такое
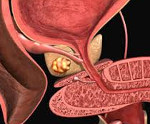
Гормонорезистентный рак простаты — первичная опухоль, изначально не зависящая от уровня андрогенов, или прогрессирование заболевания на фоне достигнутого посткастрационного уровня тестостерона. Симптомы отсутствуют либо связаны с локализацией метастатических очагов и ростом новообразования. Типично усиление болевого синдрома и интоксикация. Диагностика подразумевает определение уровня ПСА, ТРУЗИ, МРТ (КТ) висцеральных органов, легких и малого таза, ПЭТ, сцинтиграфию костей скелета. Тактика может включать изменение схем гормонотерапии, назначение блокаторов выработки андрогенов надпочечников, иммунотерапию, моно- и полихимиотерапию, радионуклидную терапию.
МКБ-10
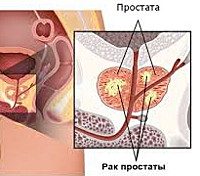
- Причины гормонорезистентного рака простаты
- Патогенез
- Симптомы гормонорезистентного рака простаты
- Осложнения
- Диагностика
- Лечение гормонорезистентного рака простаты
- Профилактика и прогноз
- Цены на лечение
Общие сведения

Причины гормонорезистентного рака простаты
Причины развития опухолевого процесса в предстательной железе остаются неясными, заболевание относят к мультифакторным. Предполагается связь между развитием опухоли и особенностями питания (преобладание красного мяса и жирной пищи), вредными привычками, контактами с канцерогенами, неблагоприятными экологическими факторами (инсоляция, облучение), хроническим простатитом с частыми рецидивами, ИППП (ретровирусная, цитомегаловирусная инфекция, генитальный герпес), иммуносупрессией, вызванной любой причиной, генетическими факторами и предраковой патологией. Относительно причин, вызывающих гормонорезистентность РПЖ, выдвинуто несколько гипотез:
- Теория клонального доминирования. Опухолевая ткань по своей морфологии на 60% гетерогенна, т. е. представлена различными клетками: гормонозависимыми и гормононезависимыми. Под воздействием антиандрогенной терапии последние начинают доминировать.
- Теория стволовых клеток. Доказано, что стволовые клетки способствуют обновлению тканей. Длительно существующее состояние с посткастрационным уровнем тестостерона дает начало поколению новых клеток, свободных от влияния гормонов.
- Адаптивная теория. Адаптационные механизмы помогают клеткам приспособиться к сверхнизким уровням гормонов. Развившиеся в условиях гормонального дефицита, они начинают агрессивно делиться, приобретая рефрактерность к андрогенам.
Патогенез
В патогенезе заболевания прослеживаются молекулярные механизмы. В раковых клетках присутствуют нарушения экспрессии генов, контролирующих процессы пролиферации. Увеличение факторов роста и их рецепторов, активация сигнальных каскадов, связанных с андроген- и эстроген-чувствительными рецепторами, повышение активности эмбриональных сигнальных путей способствует появлению агрессивных свойств в уже видоизмененных клетках, в результате чего начинается их рост, миграция и метастатическая активность. Нарушение экспрессии генов и белков проявляется срывом контроля над апоптозом, из-за чего раковые клетки обретают устойчивость к химиотерапии. Роль эпигенетических факторов, генетических мутаций и сигнальных белков, ответственных за питание опухоли, рост и кровоснабжение, не изучена до конца.
Для развития гормонорезистентной опухоли важно соотношение между андрогенами и андрогенными рецепторами. Даже при терапии антиандрогенами и проведении билатеральной орхиэктомии надпочечники, ткани простаты и сама опухоль за счет усиленной экспрессии цитохрома P450С17 (CYP17) продолжают выработку андрогенов, которых достаточно для активации андрогеновых рецепторов в условиях низкой концентрации тестостерона.
Симптомы гормонорезистентного рака простаты
При гормонорефрактерном РПЖ клинические проявления отсутствуют либо представлены местными симптомами. Задержка мочи регистрируется у 20-25% мужчин, боль в спине и ногах ‒ у 20-40%, гематурия ‒ у 10%. Гемоспермия свидетельствует о вовлеченности в процесс семенных пузырьков. У пациентов с симптоматическим течением наиболее часты жалобы на учащение мочеиспускания (38%), ослабление струи мочи (23%), ургентные позывы (10%). Слабость, повышение температуры в вечерние часы, потливость служат общими проявлениями интоксикации. Для гормонорезистентной опухоли характерно постепенное нарастание клинических проявлений, что связано с ее прогрессированием. Из-за иммуносупрессии повышается восприимчивость к инфекциям.
Метастатические симптомы включают потерю веса и плохой аппетит, боль и ломоту в костях, образование патологических переломов, дискомфорт в нижних конечностях и отечность на фоне непроходимости венозных и лимфатических притоков при метастазах. При сдавлении опухолью или забрюшинными лимфоузлами области мочеточника и его обструкции появляются тошнота, боли в пояснице на стороне поражения, температурная реакция с ознобом, что характерно для присоединения острого пиелонефрита.
Осложнения
Урологические осложнения рака простаты могут проявиться развитием острого воспалительного процесса в мочеполовом тракте, кровотечением на фоне прорастания сосуда опухолью. При обструкции мочевыводящих путей на фоне роста новообразования часто диагностируют рефлюксы и гидронефроз, что может привести к нарушению функций почек. При назначении химиопрепаратов нередко развивается нефропатия с исходом в хроническую почечную недостаточность. Негативные последствия лечения рака предстательной железы проявляются в виде стойкой эректильной дисфункции, чему способствуют терапия андрогенной депривации (биорхиэктомия + гормонотерапия) и простатэктомия. При повреждении сфинктеров и нарушении иннервации мочевого пузыря из-за травматизации во время операции может присоединиться недержание мочи. Патологические переломы и компрессия спинного мозга - осложнения метастатического рака простаты.
Диагностика
Как правило, диагноз рака простаты уже подтвержден, пациент получает либо получил лечение, направленное на максимально возможное уменьшение выработки андрогенов. Онкологические больные с данной нозологией в обязательном порядке наблюдаются у онколога или онкоуролога, регулярно проходят необходимые исследования. Первичную гормонорезистентностиь опухоли можно предположить на основании гистологического типа (базально-клеточные, переходно-клеточные, анапластические, плоскоклеточные раки), при отсутствии ответа на антиандрогенную терапию в течение 3 месяцев, росте ПСА или при появлении новых симптомов, несмотря на прием препаратов. Общие принципы диагностики включают:
- Определения уровня ПСА и тестостерона. О биохимическом прогрессе опухолевого процесса можно вести речь, если зафиксировано последовательное увеличение уровня простатспецифического антигена (на 50% выше от минимально достигнутого) в трех анализах, при обязательном уровне тестостерона менее 50нг/дл (1,7 нмоль/л). Промежуток времени между тестами - не менее недели.
- Общий анализ крови. В результатах общего анализа крови выявляют ускорение скорости оседания эритроцитов, лейкоцитоз, анемию, что может свидетельствовать о прорастании опухоли в мочевой пузырь. Снижение гемоглобина ниже 115-120г/л и одновременный рост ПСА выше 100 нг/мл - неблагоприятный прогностический признак.
- Определение уровня ЛДГ и ЩФ. Повышение уровня лактатдегидрогеназы позволяет предположить висцеральное метастазирование. Избыток щелочной фосфатазы - признак метастатического поражения костной ткани, выявляется у 70% пациентов с генерализацией опухолевого процесса.
- ТРУЗИ и МРТ простаты. Трансректальное ультразвуковое исследование предстательной железы при гормонорезистентном раке может показать увеличение объема железы и инвазию опухоли в соседние органы. Более точную картину дает МРТ органов малого таза, которая не только демонстрирует отношение опухоли с близлежащими структурами, но и в 50-70% позволяет оценить состояние внутритазовых лимфоузлов.
- Инструментальные методы визуализации. Для поиска метастазов исследуют органы грудной клетки с помощью КТ или рентгенографии, проводят ультразвуковое сканирование, МРТ или КТ органов брюшной полости. Радиоизотопную сцинтиграфию назначают при подозрении на метастазы в кости скелета или для отслеживания динамики процесса. ПЭТ-КТ может быть выполнена пациенту с раком простаты после лечения, если метастатические очаги не определяют, а уровень ПСА продолжает расти.
Лечение гормонорезистентного рака простаты
Гормонорефрактерный рак остается одним из самых сложных диагнозов в урологии, сопровождается высокой смертностью, однако существует множество аспектов в лечении, которые позволяют увеличить продолжительность жизни и улучшить ее качество. В течение последнего десятилетия введено несколько новых методов терапии с доказанной безопасностью и эффективностью. Одобрено применение новых лекарств, которые подавляют синтез тестостерона с помощью иных механизмов действия, отличных от предшественников — антагонистов андрогеновых рецепторов 1 поколения (флутамид, бикалутамилд, нилутамид). Внедрены схемы лечения, включающие кетоконазол, эстрогены, эстрамустина фосфат, ЛГРГ, соматостатин и дексаметазон.
Несмотря на множество перспективных разработок, большинство специалистов по-прежнему рекомендуют кастрацию и прием антиандрогенов с заменой препаратов или увеличением дозы. Рассматривают следующие варианты тактики ведения в дополнение к терапии максимальной андрогенной блокады:
- Химиотерапия. Доцетаксел - первый одобренный химиотерапевтический препарат для лечения метастатического гормонорефрактерного рака простаты. Его комбинация с преднизоном считается стандартом лечения. Более современное лекарство с высокой цитотоксичностью - кабазитаксел. Это препарат второй линии, также используется в сочетании с преднизоном в случаях, когда не удалось получить адекватный ответ на терапию доцетакселом.
- Иммунотерапия. Сипулеуцел-Т — представитель нового направления (вакцинотерапии) для лечения гормонорезистентной опухоли простаты. При его введении запускается специфическая активация собственной иммунной системы, которая начинает бороться с опухолевой массой. Вакцина изготавливается для каждого пациента индивидуально, на основе взаимодействия его Т-лимфоцитов с гибридным белком.
- Современные антагонисты гормонов. Антиандрогены первого поколения могут быть заменены на абиратерона ацетат — селективный ингибитор CYP17, коэнзима цитохрома Р450, который способствует подавлению выработки внегонадного тестостерона за счет угнетения активности фермента в надпочечниках, простате, опухолевой ткани, яичках. Энзалутамид — суперселективный антиандроген, его действие направлено на максимальное подавление синтеза тестостерона после прогресса онкологического процесса на фоне терапии доцетакселом.
- Таргетная радиационная терапия. Радия-223 дихлорид — радиофармпрепарат для проведения таргетной радионуклидной терапии. Токсичность от воздействия на организм минимальна. Таргетная терапия подразумевает доставку системного излучения выборочно к опухолевой клетке. Радиофармпрепарат связывается с ионами кальция и направленно подавляет активность костных метастазов. Учитывая малодоступность препаратов для целевой радиотерапии, преимущественно используют бисфосфонаты, чтобы предупредить скелетные осложнения.
Профилактика и прогноз
Прогноз связан с несколькими факторами, включая местную распространенность опухоли, наличие висцеральных и костных метастазов. Показатели безрецидивной и общей выживаемости составляют 12-24 и 24-36 месяцев. Нет доказанной стратегии в профилактике рака простаты, но риск развития патологии можно уменьшить с помощью рационального питания, которое включает низкокалорийную диету с превалированием растительных жиров, достаточное потребление фруктов и овощей, продуктов, богатых омега-з жирными кислотами. Не менее важен здоровый образ жизни с ежедневной физической активностью, регулярные сексуальные отношения. Для своевременного выявления злокачественного новообразования простаты всем мужчинам старше 40 лет необходим ежегодный осмотр урологом.
О гормональной регуляции простаты известно уже более 100 лет, начиная с классических работ А.Т. Cabot (1896) и W, White (1904), а гормональное лечение рака простаты проводится уже более 60 лет благодаря результатам, полученным С.В. Huggins и Ch. Hodges (1941).
Гормональная терапия является паллиативным лечением и позволяет добиться объективного и субъективного ответа у 60-80% всех первичных пациентов.
Однако гормональная чувствительность опухоли сохраняется в течение 18-24 мес и рано или поздно практически у всех пациентов развивается резистентность к гормональной терапии, продолжительность жизни при этом составляет от 7 до 16 мес.
Традиционно считалось, что у больного имеется гормонорезистентный рак простаты (ГРРП), если у него наблюдается клиническая прогрессия или повышение простатспецифического антигена (ПСА) при адекватной андрогенной депривации (АД). Однако более обоснованно говорить о гормонорезистентности можно лишь в том случае, когда опухоль не реагирует на гормональную терапию II линии (отмену антиандрогенов, антиандрогены II линии, эстрогены, кетоконазол и т.п.) в течение 4 нед. За годы клинических испытаний была выработана серия согласованных критериев, которые помогли стандартизировать концепцию ГРРП.
В настоящее время прогрессия во время гормональной терапии признается при возникновении новых метастазов в кости, мягкие ткани или лимфатические узлы и также гормон рефрактерности определяется при:
• Кастрационный уровень тестостерона в сыворотке крови ( 2 нг/мл.
• Отмена антиандрогенов или по крайней мере одна иная модификация гормонального лечения в течение 4 нед.
• Продолжающийся рост уровня ПСА, несмотря на последующие модификации гормонального лечения.
Гормонорезистентный рак простаты имеет значительную гетерогенность, что делает необходимым оценивать прогностические факторы для разделения пациентов на группы риска. Это позволяет выбрать наиболее подходящее лечение для каждого больного, что особенно важно в связи с постоянным ростом количества терапевтических подходов. По данным ряда современных авторов, применимы несколько прогностических показателей: уровень активности пациента по шкале ECOG, уровень гемоглобина, лактатдегидрогеназа, уровень простатспецифического антигена, снижение массы тела, количество костных метастазов и маркеры нейроэндокринной дифференцировки.
Высокие показатели смертности от рака предстательной железы в России объясняются низким качеством диагностики. Несмотря на возрастающие темпы внедрения в клиническую практику современных методов диагностики, в последнее десятилетие число локализованных форм рака предстательной железы не только не ув.
Эпидемиология. Частота рака предстательной железы (РПЖ) неоднородна в разных странах. В США он занимает 2-е место среди злокачественных заболеваний у мужчин, составляет 18% от вновь выявленных опухолей и 10% от всех летальных исходов среди этих больных [Flanders W., 1984]. Выявлена э.
Клиническая картина аденомы простаты определяется тремя компонентами: симптомами нижних мочевых путей, увеличением предстательной железы и дисфункцией мочевого пузыря. Последняя может проявляться инфравезикальной обструкцией, нестабильностью или гипотонией (рис. 1). В клинической картине доброкачест.
К лечению пациентов приступают только тогда, когда патологические изменения достигают стадии клинических проявлений. Вопрос о показанности профилактической терапии сегодня остается открытым, а его целесообразность недоказанной. Если еще 10 лет назад реальной альтернативы операции при аденоме простат.
Наблюдение за больными в послеоперационном периоде является неотъемлемой частью процесса лечения онкоурологических больных. Это обусловлено в первую очередь тем, что у незначительной части больных после операции возникают ранние или отдаленные осложнения (стриктуры, недержание мочи, импотенция и.
Выбор методов лечения рака предстательной железы, последовательность их применения и прогноз зависят от ряда факторов, наиболее значимыми из которых являются стадия заболевания, уровень простатического специфического антигена, степень дифференцировки опухоли по Глисону, наличие периневральной инвази.

-
Содержимое:
- Почему рак простаты становится гормонорезистентным
- Чем опасен переход в гормононечувствительное состояние
- Как лечить гормононечувствительный рак простаты
- Использование гормонотерапии
- Лечение химиотерапией
- Революционные методики терапии
- Как избежать кастрационно-рефрактерного рака простаты
Применение гормонотерапии, лечения, блокирующего выработку тестостерона, существенно замедляет процесс развития ракового заболевания. Со временем назначаемые препараты теряют эффективность. В тяжелых случаях диагностируется гормонорезистентный рак предстательной железы, продолжающий активно прогрессировать, несмотря на низкий уровень тестостерона в крови.
Почему рак простаты становится гормонорезистентным
Европейская ассоциация онкологов разработала критерии оценки заболевания:
- Кастрационный уровень содержания тестостерона в крови 1,7 нг/моль.
- Последовательное повышение ПСА с интервалом не более 7 дней и дифференцированным 50% увеличением уровня простат специфического антигена на 50%.
- Устойчивая прогрессия ПСА, несмотря на применение различных тактик гормонотерапии.
Один из характерных признаков заболевания – уровень простат антигена в крови. Появление инструментальных видов исследований, позволяющих определить уровень ПСА сделало диагностику более достоверной. Уровень антигена при гормон-независимом раке простаты постоянно растет, даже несмотря на полную андрогенную блокаду.

Второй тип онкологии поддается терапии, первый нет. Гормонорезистентный рак имеет низкий порог выживаемости. Прогнозируемое продолжение жизни всего 2-3 года.
Переход с гормонозависимого в гормонорезистентный рак происходит по причине привыкания железы и организма к андрогенам и блокаторам тестостерона. Даже при правильно назначенной терапии существует высокая вероятность развития опухоли, устойчивой к приему медикаментозных средств.
Как лечить гормононечувствительный рак простаты
Лечение гормонорефрактерного рака предстательной железы в отличие от резистивного подвида возможно, хотя и представляет некоторые сложности. Продолжают андрогенную блокаду. При достижении первичной гормонорезистентности назначают химиотерапию, рекомендуют проведение современных альтернативных методик.
Были разработаны схемы терапии, подбираемые по нескольким основным критериям:
- Устойчивость пациента к первой линии лечения.
- Выполнение полной андрогенной блокады.
- Индивидуальные особенности пациента.
Исходя из трех критериев отбора, лечащий врач подберет гормональную терапию, подходящую для каждого пациента в отдельности.

Первая линия лечения гормононечувствительного рака простаты направлена на 1-2 группу клеток. Через время наступает устойчивость онкозаболевания к медикаментозной терапии. Подавление 1-2 группы тканей приводит к развитию раковой опухоли, состоящей исключительно из клеток, не требующих гормонов для роста и выживаемости.
Онкозаболевание для формирования перестает нуждаться в тестостероне. Развивается вторичная гормонорезистентность. На этом этапе гормонотерапия становится полностью неэффективной. Назначается химия.
Раньше считалось, что химиотерапия, по причине своей низкой эффективности, существенно уступает другим методикам лечения раковых заболеваний. На данный момент были разработаны препараты, способные существенно облегчить состояние пациента, улучшить качество его жизни.
Несмотря на эффективность современной химиотерапии, пациенту оказывается исключительно паллиативное лечение, полного исцеления от онкозаболевания не наступает. Критерием эффективности считается продление жизни на 2-3 года.

Последние достижения в лечении позволили использовать в борьбе с онкозаболеванием собственную иммунную систему пациента. В Израильских клиниках был разработан метод использования вакцины против рака, не имеющий аналогов в мире.
Иммунотерапия практически не имеет побочных эффектов и отличается хорошей результативностью.
Методика проводится следующим образом:
- Берется забор крови у пациента.
- Клетки очищаются и обрабатываются синтетическими составами.
- Видоизмененная кровь вводится обратно, провоцируя борьбу с раковыми клетками.
Иммунотерапия в Израиле уже перестала быть экспериментальным лечением и входит в курс терапии крупнейших клиник. В России методика не применяется.
Кастрационно-резистентный рак предстательной железы развивается, несмотря на тщательное планирование стратегии лечения и грамотно назначенный прием медикаментов. Причин этому несколько:
- Сроки возникновения гормонорезистентности оставляют всего 12-18 месяцев.
- Около 30% пациентов отказываются от проведения полной андрогенной блокады (орхиэктомия + гормонотерапия).
- Малая эффективность традиционных препаратов, относящихся к первой линии лечения.
- Недостаток гибкости в назначаемой терапии.
Схема современных методов лечения гормонорезистентного рака простаты, практикуемая в крупнейших клиниках Израиля, состоит в индивидуальном подборе лекарственных средств и постоянной корректировке назначаемых препаратов. Проводятся тесты с целью выявить привыкание раковой опухоли к воздействию медикаментов.
Выбор тактики лечения при кастрационно-резистентном раке предстательной железы связан в первую очередь с состоянием пациента и клиническими проявлениями злокачественных тканей. Только после полного обследования больного можно подобрать соответствующий вид лечения, включая современные методы борьбы с онкозаболеваниями.
Распространенность гормонорезистентного рака среди взрослого мужского населения (после 50 лет) занимает первое место. По мере старения организма, вероятность развития патологии увеличивается до 60-75%, что делает этот вид онкологии одним из самых опасных в мире.

Злокачественные новообразования простаты очень распространены среди мужчин старшего возраста. В последнее время заболевание значительно помолодело: если раньше оно было характерно для мужчин старше 65 лет, то теперь нередко диагноз ставится в 50-55 лет.
В большинстве случаев прогрессирование опухоли напрямую зависит от продукции главного мужского полового гормона, тестостерона, продуцируемого тестикулами и, в значительно меньшей степени, надпочечниками. Медикаментозное воздействие, эффективность которого сопоставима с таковой у хирургической кастрации, значительно снижает выработку организмом тестостерона (до 50 нг/мл и ниже), рост раковой опухоли при этом приостанавливается.
Однако существуют новообразования, продолжающие расти после проведенной гормонотерапии. Эти опухоли называются гормонорезистентными (не чувствительными к гормональной терапии, при раке простаты – кастрационной-рефрактерными). Неопластический процесс в этом случае прогрессирует в продолжение 1-1,5 лет. Выживаемость пациентов с таким видом рака обычно не превышает 2-3 лет (при наличии метастазов в костной ткани – 40 мес., без метастазирования в кости – 68 мес.).

Европейский урологи предложили следующие критерии, позволяющие поставить диагноз гормонорезистентный рак предстательной железы:
- в крови пациента содержание тестостерона 50 нг/мл и ниже;
- при троекратном определении простатического специфического антигена (между анализами проходит как минимум недельный перерыв) видно значительное повышение его концентрации (двукратное 50% возрастание относительно наименьшей концентрации) тогда, когда уровень ПСА превышает 2 нг/мл;
- прием антиандрогенов был прекращен;
- повышение ПСА не взирая на последовательное назначение средств гормональной терапии.
Ученым пока не удалось достоверно установить, по каким причинам злокачественный процесс простаты перестал быть чувствительным к гормонам.
При кастрационно-рефрактерном раке опухолевые клетки продолжают прогрессивно размножаться, не смотря на терапию с использованием аналогов рилизинг-гормона лютеинизирующего гормона (ЛГРГ), андрогенов или произведенную хирургическую кастрацию. Некоторые разновидности опухолей в этом случае могут оказаться чувствительными к препаратам второй линии – эстрогенам, кетоконазолу. Гормонорезистентность предполагает невосприимчивость к любым видам гормонального воздействия.
The request cannot be completed because you have exceeded your quota.
Терапевтические мероприятия

Развитие злокачественной опухоли включает несколько последовательных этапов, на каждый из которых можно воздействовать, используя медицинские методики:
Разрабатываются лекарственные препараты, призванные контролировать протекание патологического процесса до состояния хронической патологии.

Современная терапия при раке простаты, не чувствительном к воздействию гормонов, включает в себя следующие шаги:
- максимальная андрогенная блокада;
- интермиттирующая андрогенная блокада;
- прекращение приема антиандрогенных средств;
- замена используемых антиандрогенных препаратов другими представителями той же группы;
- использование эстроген-содержащих медикаментов;
- использование кетоконазола;
- применение средств, проходящих клинические испытания и еще не появившихся на рынке;
- химиотерапевтическое лечение;
- использование медикаментов, уменьшающих проявления болевого синдрома.

Пациент, переживший хирургическую или медикаментозную кастрацию, регулярно сдает анализы для определения содержания простатического специфического антигена — маркера рака простаты. Увеличение количества этого вещества врач расценивает как невосприимчивость опухоли как минимум к некоторым половым гормонам. Поскольку прекращение андрогенной блокады, как правило, влечет за собой резкое прогрессирование заболевания, имеет смысл продолжать назначение антиандрогенов. Такой рак на данном этапе называют кастрационно-рефрактерным, поскольку все варианты гормональной терапии не были испробованы, соответственно результативность их не оценена.
В случаях, когда в сыворотке уровень тестостерона ниже кастрационного, онколог может порекомендовать дополнительный препарат для полной андрогенной блокады (например, сочетанный прием агонистов и антагонистов ЛГРГ). Если такая терапия не дает положительной динамики, врач отменяет лечение антиандрогенами. У некоторых пациентов этот вариант приводит к снижению уровня ПСА по прошествии некоторого времени (около месяца).

Существует методика интермиттирующей андрогенной блокады: в этих случаях после воздействия медикаментов следует запланированный перерыв, а затем лечение возобновляется. Считается, что подобное лечение способно отсрочить возникновение опухолевого процесса, не восприимчивого к гормональному лечению. Отмечается улучшение качества жизни пациентов и лучшая пятилетняя выживаемость.
Для интермиттирующей андрогенной блокады подходят не все пациенты с опухолью простаты, а только те, кто отвечает следующим критериям:
- локальный рак простаты, не давший костных метастазов или при незначительном метастазировании;
- перенесенная лучевая или химиотерапия;
- плохие биохимические показатели.

Продолжительность интермиттирующей блокады должна определяться максимальным уровнем апоптоза злокачественных клеток, а также временем появления фенотипа опухолевых клеток, отличающихся андрогенрезистентностью. Обычно цикл длится около 8-9 мес., меньшая продолжительность не позволяет достичь оптимального уровня простатического специфического антигена. Дискуссионным вопросом считается целесообразность продолжения лечения в течение нескольких месяцев после достижения ПСА ожидаемого уровня.
Промежуток времени, который следует выжидать между применением медикаментов, обсуждается. Этот перерыв должен обеспечивать поддержание нормального качества жизни и обеспечивать рост чувствительных к тестостерону клеток.
Следующие показатели влияют на время начала повторного курса:
- уровень ПСА до начала терапии;
- уровень ПСА в динамике;
- развитие клинической симптоматики;
- стадия заболевания;
- уровень толерантности к андрогенной блокаде.

Если до начала лечения ПСА находится на высоком уровне, а у пациента определены метастазы в костях, второй курс назначается при достижении ПСА уровня 20 нг/мл. Если перед началом терапии концентрация ПСА умеренная, а сама опухоль простаты локализованная, повторный курс начинают при достижении уровня ПСА от 6 до 15 нг/мл. Пациентам, у которых диагностирован рецидив опухоли после радикальной простатэктомии, лечение возобновляют раньше.
Следующий предпринимаемый шаг – назначение средств, относящихся ко второй линии (например, эстрогенов). Использование эстрогенов в низкой дозировке большинством пациентов воспринимается хорошо.

Хороший терапевтический эффект дает сочетанное применение глюкокортикостероидных средств с адреналовыми супрессантами (кетоконазолом): уровень сывороточного ПСА снижается, симптоматика онкологического заболевания становится менее выраженной. Положительный результат может достигаться и при изолированном приеме глюкокортикоидов в низких дозировках.
Те случаи, когда выполнение всех описанных выше действий не привело к положительному результату, расцениваются врачами как гормонорезистентный рак.
Химиотерапия считается паллиативной методикой, ее назначение – увеличить продолжительность жизни и улучшить ее качество. Продолжительность использования средств для химиотерапии простаты определяется онкологом индивидуально.
Читайте также:

