Гепатит с при лимфогранулематозе
Ассоциативная связь неходжкинских лимфом и вирусного гепатита С хорошо известна и многократно описана. В свою очередь, этиотропная терапия способствует вирусологическому и гематологическому ответу большинства неходжкинских лимфом, связанных с ВГС.
В последние годы противовирусные препараты прямого действия сделали возможным проведение лечения для большинства пациентов с ВГС. Недавно были высказаны некоторые опасения в отношении частоты и характера рецидивов ГЦК среди пациентов получавших данную группу препаратов.
Мы представляем описание клинического случая диффузной крупноклеточной В-клеточной лимфомы (ДККЛ) в стадии ремиссии после соответствующего лечения, на фоне вирусного гепатита С с исходом в цирроз печени, который был вылечен с помощью новых противовирусных препаратов прямого действия. Однако, вскоре после достижения УВО, произошел рецидив лимфомы, приведший к летальному исходу.
Связь между вирусом гепатита С (ВГС) и неходжкинской лимфомой (НХЛ) является распространенной, особенно отметим лимфому маргинальной зоны, диффузную крупноклеточную лимфому (ДККЛ) и в меньшей степени фолликулярную лимфому. Лимфомагенез ВГС представляет собой многофакторную модель злокачественной трансформации, включающую несколько механизмов, включая хроническую антигенную стимуляцию, взаимодействие с инфицированным микроокружением и воспалительными цитокинами, а также прямую трансформацию вирусными белками.
Среди ВГС-ассоциированных агрессивных НХЛ, ДККЛ является наиболее часто встречаемой во врачебной практике. Золотым стандартом и первой линией терапии является иммунохимиотерапия R-CHOP (ритуксимаб, циклофосфамид, доксорубицин, винкристин, преднизон). С целью устранения одного из триггеров развития лимфомы и потенциального снижения риска рецидива, следует уделить внимание противовирусной терапии как в комбинации, так и после завершения иммунохимиотерапии.
Недавно проведенное большое когортное исследование показало, что устойчивый вирусологический ответ (УВО) после противовирусного лечения снижает риск рецидива B-клеточной НХЛ по сравнению с группой пациентов не принимавших лечение, направленное против ВГС.
Мы представляем клинический случай — 57-летнего мужчину направленного на лечение хронического гепатита С (ВГС), с В-клеточной НХЛ в анамнезе. У данного пациента была диагностирована ДККЛ (стадия IIA, по классификации Ann Arbor) после биопсии надключичного лимфатического узла, которая показала инфильтрацию злокачественными клетками CD20, CD10, Bcl-6 (40%), MUM1 (30%), положительной экспрессией Bcl-2 и отрицательной D1, CD5, CD23, CD3. Ki-67 был положительным на 50%. Пациенту провели 6 циклов R-CHOP и достигли полного ответа, подтвержденного КТ всего тела и результатами биопсии костного мозга.
Через восемнадцать месяцев после завершения химиотерапии пациент был направлен в гепатологическое отделение для лечения гепатита С. Клиническое исследование показало незначительное повышение уровня аминотрансфераз (АСТ 46, АЛТ 66), вирусная нагрузка была высокой (ВГС-РНК 1.600.000 МЕ/мл) и выявлен 3a генотип, эластичность печени (оцененная с помощью Fibroscan®) показывала значение 17,6 кПа, что соответствовало циррозу (Child A/5, MELD 8).
Проведенная эндоскопия показала небольшое варикозное расширение вен пищевода, тогда как визуализация печени (КТ брюшной полости) отсутствие любых видов очагового поражения или асцита (рис. 1).
На тот момент пациенту проводили лечение в соответствии с рекомендациями Европейской ассоциации по исследованию печени (EASL) c применением противовирусных препаратов прямого действия (ПППД): софосбувир 400 мг и велпатасвир 100 мг в сочетании с рибавирином длительностью 12 недель. Лечение проходило без каких-либо осложнений. Спустя три месяца после окончания лечения было зафиксировано достижение УВО.
Спустя два месяца после достижения УВО, и, несмотря на то, что неоднократно документировалась полная ремиссия ДККЛ (ПЭТ КТ, гематологические показатели), в течение двух последующих лет наблюдения, пациент поступил в стационар с отчетливой болью в правом верхнем квадранте и ухудшением функций печени.
Визуально отмечалась желтизна кожных покровов и склер. КТ показала генерализованную лимфаденопатию, аномальное утолщение конечной подвздошной кишки, гепатоспленомегалию с выраженным асцитом (рис. 2).

Рис. 2. CECT-сканирование. Неоднородная картина печени (ромб), увеличенные парааортальные лимфатические узлы (овалы), камни желчного пузыря (наконечник стрелки), скопление жидкости (звездочки).
Пункционная биопсия печени показала (рис. 3) обширную инфильтрацию ДККЛ в паренхиму печени (этап IV Энн Арбор при рецидиве, IPS: высокий, R-IPS: низкий). На момент исследования профиль ДККЛ был таким же, как и при первичном обращении (CD20+, PAX-5+, CD3-, CD30-). Летальный исход пациента был обусловлен развитием печеночной недостаточности незадолго до получения химиотерапии.
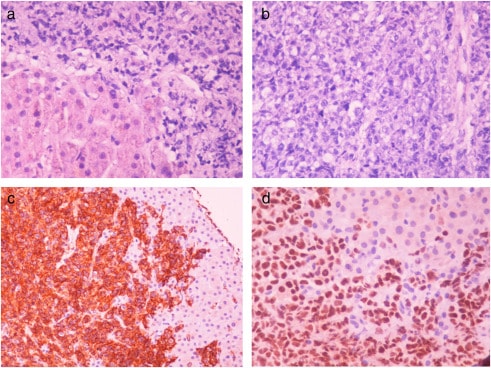
Рис. 3. Биопсия печени с обширной инфильтрацией агрессивной крупной В-клеточной лимфомой.
A и B — окраска гематоксилином и эозином, C — CD20-позитивная цитоплазматическая экспрессия, D— PAX-5, ядерная позитивная экспрессия.
В-клеточная НХЛ тесно связана с ВГС который является триггером хронической антигенной стимуляции. Проводимое этиотропное лечение может привести к вирусологическому и гематологическому ответу у двух третей пациентов с НХЛ, связанных с ВГС.
В мета-анализе 20 исследований, частота ответа при противовирусном лечении составила 73%, при этом, была выявлена сильная корреляция между достижением УВО и лимфомной реакцией. Сообщается, что использование в лечении ПППД снижает частоту возникновения злокачественных В-клеток в периферической крови пациентов, страдающих лимфопролиферативными нарушениями связанными с ВГС, однако моноклональные популяции могут сохраняться после эрадикации вируса.
На данный момент в современной литературе много споров о возможности возникновения рецидива гепатоцеллюлярной карциномы (ГЦК) после применения ПППД в группе пациентов с ВГС и ГЦК. Ряд клинических случаев показал неожиданно высокую частоту и агрессивную картину рецидива ГЦК в данной группе. Тем не менее, недавний систематический обзор и мета-анализ не обнаружили никаких доказательств того, что возникновение или рецидив ГЦК различаются между противовирусным лечением на основе интерферона (ИНФ) или ПППД.
Существует очень мало данных о рецидивах НХЛ после успешной противовирусной терапии ВГС среди пациентов с НХЛ. Недавнее исследование сообщило о возникновении НХЛ после достижения УВО у двух пациентов, получавших софосбувир и ледипасвир без гематологических заболеваний в анамнезе.
В аналогичной работе сообщалось о развитии высокоагрессивной лимфомы мантийной зоны спустя месяц после завершения лечения софосбувиром и рибавирином. В другой серии сообщалось о пяти случаях B-клеточных НХЛ после лечения ПППД, причем все пациенты, кроме одного, достигали не только УВО, но и полной ремиссии НХЛ.
Совсем недавно описание аналогичного случая опубликовали в Японии, в котором пациент проходивший лечение от ДККЛ, имел рецидив с летальным исходом спустя 7 лет после лечения лимфомы: пациент получал софосбувир и ледипасвир, при этом, сразу после достижения УВО, был зафиксирован рецидив агрессивной формы лимфомы.
Механизм возникновения рецидива ГЦК среди пациентов проходившим лечение ПППД пока неясен. Было выдвинуто предположение, что подобные схемы лечения восстанавливают количество и функции ряда иммунных клеток, таких как вирус-специфические CD8+, Т- и NK-клетки.
Кроме того, отсутствие постоянной стимуляции со стороны интерферона после элиминации вируса также может оказывать значительное влияние на внутрипеченочные иммунные реакции. Возможно, именно эти изменения внутрипеченочного иммунологического баланса были связаны с возникновением агрессивного рецидива ГЦК.
На данный момент, ввиду малого числа описанных случаев, нет соответствующих данных для группы пациентов с рецидивом лимфомы.
Восстановление опосредованного Т-клетками и В-клетками иммунного статуса благодаря эрадикации ВГС может привести к нарушению регуляции иммунного ответа, являясь фактором способствующим дополнительной клональной эволюции НХЛ.
Более того, есть подозрение, что ПППД может иметь более низкую антилимфомную активность, чем ИНФ, так как процент пациентов с прогрессом заболевания или гематологическим рецидивом, несмотря на достижение УВО гораздо выше, чем в случае применения ИНФ, который действует как иммунологический модулятор. Другим объяснением возможного снижения эффективности ПППД при ВГС-ассоциированных лимфомах является отсутствие у данной группы препаратов антипролиферативной активности.
В случаях ВГС-положительной ДККЛ была описана решающая роль дисрегуляции сети микроРНК, с последующим подавлением микроРНК-26b (miR-26b) которая напрямую участвует в ослаблении совокупности процессов подавления опухоли. Недавнее исследование показало обратную корреляцию вирусной нагрузки ВГС с экспрессией miR-26b в мононуклеарных клетках периферической крови среди пациентов с ВГС-НХЛ, что было предложено в качестве потенциального биомаркера для прогнозирования реакции лимфомы в данной группы пациентов.
Описанный нами клинический случай ДККЛ и последующим успешным лечением ВГС, вскоре за которым после достижения УВО произошел агрессивный рецидив со смертельным исходом, является редкостью. Это подчеркивает необходимость тщательного наблюдения за пациентами с НХЛ после лечения ВГС используя ПППД, в особенности, после достижения УВО.
Источники:
Коллектив авторов:
- Dimitrios N. Samonakis, Maria Psyllaki et all.
Лимфогранулематоз и другие лимфомы. Определние, распространенность, этиология, патогенез. Классификация лимфогранулематоза (гистологическая, по стадиям) и других лимфом. Особенности клинической картины в зависимости от стадии заболевания. Критерии диагностики. Лечение ходжкинской и неходжкинской. Профилактика и прогноз.
Лимфогранулематоз
Субстрат опухоли: клетки Штернберга-Рид (CD23) (ретракция цитоплазмы, мелкие ядра).
Факторы:
химические вещества: бензол, ТНТ, инсектициды и др.;
лекарственные препараты: цитостатики, сульфаниламиды, амидопирин, мерказолил, левомицетин и др.;
циркуляторно-гипоксический синдром (одышка, тахикардия, слабость, систолический шум над сердцем, бледность кожных покровов);
инфекционно-токсический синдром (лихорадка, ангины, пневмонии, инфекции мочевых путей, вплоть до развития септического состояния);
геморрагический синдром (петехии, экхимозы, гематомы, носовые и маточные кровотечения);
исследование КМ: угнетение всех ростков кроветворения.
этиотропная терапия: прекращение контакта с этиологическими факторами;
патогенетическое и симптоматическое лечение: гемотрансфузии, ТКМ, ГКС, анаболические гормоны, спленэктомия, антибиотики.
наличие первичного опухолевого очага, подобно солидным опухолям.
Лимфогранулематоз (болезнь Ходжкена) — первичное опухолевое заболевание, характеризующееся злокачественной гиперплазией лимфоидной ткани с образованием в лимфатических узлах и внутренних органах лимфогранулём. Характерны два возрастных пика заболеваемости: в 15—30 лет с одинаковой частотой среди мужчин и женщин и старше 50 лет с более высокой заболеваемостью у мужчин.
Неходжкинские лимфомы объединяют группу заболеваний, характеризующихся первичным локальным, преимущественно внекостномозговым опухолевым ростом лимфатической ткани. Эти лимфоидные опухоли различаются по морфологической картине, особенностям клинического течения, прогнозу.
Эпидемиология
Стандартизованные показатели заболеваемости лимфо- и ретикулосаркомами колеблются в пределах 2—6,9 у мужчин, 0,9—5 у женщин.
Неходжкинскими лимфомами мужчины заболевают значительно чаще, чем женщины, возраст их к моменту установления диагноза колеблется в больших пределах.
Классификация
Неходжкинские лимфомы низкой степени злокачественности:
— лимфоцитарный, диффузный тип;
— пролимфоцитарный, нодулярный тип;
Неходжкинские лимфомы промежуточной степени злокачественности:
— пролимфоцитарно-лимфобластный, нодулярный тип;
— пролимфоцитарный, диффузный тип;
— пролимфоцитарно-лимфобластный, диффузный тип.
Неходжкинские лимфомы высокой степени злокачественности:
— иммунобластный, диффузный тип;
— лимфобластный (макро-, микро-, со скрученным и нескрученным ядром), диффузный тип;
Лимфогранулематоз
чаще поражает представителей европеоидной расы. Лимфогранулематоз может возникнуть в любом возрасте. Однако существует два пика заболеваемости: в возрасте 20—29 лет и старше 55 лет. И мужчины, и женщины, за исключением детей до 10 лет (чаще болеют мальчики) болеют лимфогранулематозом одинаково часто, но мужчины всё же несколько чаще, с соотношением 1,4:1.
Частота возникновения заболевания — примерно 1/25000 человек/год, что составляет около 1 % от показателя для всех злокачественных новообразований в мире и примерно 30 % всех злокачественных лимфом.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Этиология неясна. Связывают с вирусом Эпштейн-Барр
• Существуют этнические особенности заболеваемости.
Диагноз лимфогранулематоза ставят только при обнаружении клеток Рид—Штернберга. опухолевые клетки составляют ничтожную часть опухоли, образованной в основном неопухолевыми поликлональными Т-лимфоцитами (CD4+-клетки, Т-хелперы), плазматическими клетками, тканевыми гистиоцитами и эозинофилами. Эта особенность связана с активной секреторной деятельностью клеток Рид—Штернберга, выделяющих многочисленные цитокины и факторы хемотаксиса.
• Опухоль возникает уницентрически обычно в лимфатических узлах шей, надключичных областей, средостения; метастазирует лимфогенным и ге-матогенным путём.
• Вариант с преобладанием лимфоидой ткани. Обнаруживают большое ко-личество неопухолевых лимфоцитов и гистиоцитов и единичные клетки Рид—Штернберга и Ходжкена. В последней классификации ВОЗ выделя¬ют также отдельный вариант — нодулярное лимфоидное преобладание. Именно при этой форме на клетках Рид—Штернберга обнаруживают Аг В-лимфоцитов CD 19, CD20, CD79a, а в их геноме — гены тяжёлых цепей Ig.
• Смешанно-клеточный вариант. Обнаруживают клетки Рид—Штернберга в значительным количестве и клетки гетерогенной популяции реактивно¬го воспаления.
Классификация по стадиям и клиническая картина
Стадия 1 Вовлечение одной группы лимфатических узлов с любой стороны диафрагмы; непосредственное поражение ограниченной области или одного экстранодального очага, являющееся единственным проявлением заболевания
Стадия 2 Вовлечение двух или более групп лимфатических узлов по одну сторону диафрагмы; может вовлекаться селезенка, если группы поражённых лимфатических узлов расположены ниже диафрагмы
Стадия 3 Вовлечение групп лимфатических узлов по обе стороны диафрагмы; может поражаться селезенка
Стадия 4 Вовлечение экстранодальных областей и органов (костный мозг, печень, лёгкое и т.п.)
Все стадии подразделяются на:
А Бессимптомное течение
Б Необъяснимое уменьшение массы тела на 10%; лихорадка неясного генеза выше 38°С; усиленное потоотделение по ночам
Классификацию др лимфом см. выше в неходжкинских
Клиника по стадиям
• Строгое распространение процесса от одной группы лимфатических узлов к другой. Наиболее часто поражаются шейные, надключичные, подключичные лимфатические узлы, узлы средостения. Множественные, различных размеров (иногда достигают 5 см в диаметре), округлые, плотные, чаще безболезненные лимфатические узлы образуют конгломераты, изменяя конфигурацию шеи.
• Поражение средостения нередко бывает массивным (10 см и более). При расширении тени средостения более чем на 2/3 от поперечника грудной
• При поражении печени и костного мозга IV стадия. В то же время следует отличать диффузные, мелкоочаговые поражения печени и костного мозга от солитарных. При солитарном поражении печени при УЗИ обнаруживают очаговые тени; печень увеличена, болезненна при пальпации. При солитарных поражениях костей появляются оссалгии, могут возникнуть патологические переломы. Это прогностически плохая клиническая ситуация.
• Поражение селезёнки часто (обозначают буквой S). Селезёнка увеличена, при биопсии в ней обнаруживают типичные лимфогранулёмы.
• Локализованные экстранодальные поражения (буквой Е). Это могут быть интерстициальные пневмонии с признаками дыхательной недостаточности (одышка, цианоз), лимфогранулёмы в лёгких и плевре, экссудативный плеврит (выраженный болевой синдром, вынужденное положение тела больного, несимметричные движения грудной клетки при дыхании).
• Буквами А и В обозначают соответственно отсутствие или наличие одного или нескольких нижеперечисленных клинических симптомов: ночное профузное потоотделение; повышение температуры тела выше 38° С не менее 3 дней подряд при отсутствии реактивного воспаления; уменьшение массы тела более чем на 10% за последние 6 мес.
Лимфогранулематоз 1Уд стадии с поражением шейных лимфатических узлов слева, костного мозга. Гистологический вариант — лимфоидное истощение. Лимфогранулематоз 111^ стадии, N, S. Нодулярный склероз.
ЛАБОРАТОРНЫЕ И ИНСТРУМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
Характерны лимфопения и увеличение СОЭ.
повышение концентрации ЛДГ, бета2-микроглобулина. повышение активности трансаминаз (При поражении печени), уменьшение концентрации альбумина и диспротеинемию. повышение концентрации гаптоглобина.
Костномозговая пункция и двусторонняя трепанобиопсия
Рентгенографию органов грудной клетки проводят для выявления поражения органов грудной клетки. Для оценки состояния внутренних лимфатических узлов и органов также проводят MPT (КТ) и УЗ И грудной клетки, живота и таза.
Инвазивные методы диагностики
Диагностическая лапаротомия или лапароскопия с биопсией печени и селезёнки, медиастиноскопия или медиастинотомия с биопсией опухоли средостения. Возможно проведение торакоскопии и торакотомии.
Дифференциальная диагностика лимфогранулематоза с лимфомами и со-лидными опухолями проводится только по данным морфологического (а иногда и иммуногистохимического) исследования.
Лимфогранулематоз дифференцируют с лимфаденитом, лейкозом, метастазами злокачественной опухоли, туберкулезом разной локализации (лимфаденит, туберкулезный бронхоаденит, мезаденит), саркоидозом.
Лимфогранулематоз (болезнь Ходжкина)
Регионарное или генерализованное увеличение периферических лимфоузлов, чаще шейных или надключичных, реже паховых и миндалин. Увеличение может быть значительным, узлы плотные, спаяны в пакеты между собой, с кожей не спаяны, как правило, безболезненны, вначале подвижны, а затем по мере роста подвижность их уменьшается.
Нередко рентгенологически выявляется увеличение узлов средостения, что сочетается иногда с признаками сдавления органов средостения.
Более или менее характерным признаком является лихорадка неправильного типа или волнообразная.
Кожный зуд у больных встречается нечасто, но симптом имеет большое диагностическое значение, поскольку не сопровождается каким-либо кожными проявлениями.
Признаками интоксикации является ухудшение общего состояния, ночные поты.
Анализ крови — ускорение СОЭ, лейкоцитоз, лимфоцитопения, реже эозинофилия.
Увеличена активность щелочной фосфатазы.
Решающий метод диагностики — биопсия пораженных лимфоузлов и их гистологическое исследование. Диагноз считается достоверным при обнаружении в биоптатах клеток Березовского-Штернберга. Одновременно устанавливается гистологический вариант ЛГМ, что имеет определенное значение для прогноза и выбора метода терапии.
Неходжскинские лимфомы (НХЛ)
Появление где-либо плотной опухоли, не приносящей беспокойства больному.
Появлению опухоли могут предшествовать признаки интоксикации, аутоиммунной гемолитической анемии, васкулита с изменениями кожи, высыпаний на коже типа экземы. Появление синдрома сдавления венозных или лимфатических сосудов (например, синдрома верхней полой вены).
Более частое, чем при лимфогранулематозе, экстранодальное поражение – желудок, легкие, печень, кожа.
Цитопения может свидетельствовать о поражении костного мозга.
Обнаружение опухолевого образования в брюшной полости и признаки кишечной непроходимости характерны для лимфомы Беркита.
·Решающий метод – биопсия опухолевого образования, увеличенного лимфоузла.
Вид полихимиотерапии и её объём зависят от стадии заболевания.
К факторам плохого прогноза относятся: пожилой возраст, мужской пол, массивные очаги поражения (более 10 см), поражение лимфатических узлов ниже диа¬фрагмы, СОЭ более 30 мм/ч, лейкоцитоз с лимфопенией, анемия. В настоящее время используют критерии Хасенклевера—Диля, они включают:
• концентрация альбуминов менее 4 г/л;
• концентрация НЬ менее 105 г/л;
• IV стадия заболевания;
• возраст старше 45 лет;
• лейкоцитоз более 16- 109/л;
• лимфопения менее 0,6- 109/л (или менее 8%).
• При I—3А стадиях заболевания проводят 6 курсов полихимиотерапии
по схеме ABVD в комбинации с лучевой терапией. Схема ABVD: в 1-й и 14-й дни вводят доксорубицин (адриамицин) 25 мг/м2 в/в, блеомицин 10 мг/м2 в/в, винбластин 6 мг/м2 в/в, дакарбазин 375 мг/м2 в/в.
• При 2Б-4Б стадиях проводят 6—8 курсов ABVD с последующей лучевой терапией по субрадикальной (облучение всех лимфатических коллекторов по обе стороны диафрагмы, за исключением пахово-подвздошных областей) или радикальной программе (в том числе и пахово-подвздошных областей).
• При наличии 3 и более прогностических признаков назначают терапию по программе ВЕАСОРР: циклофосфамид 650 мг/м2 в/в в 1-й день, док¬сорубицин (адриамицин) 25 мг/м2 в/в в 1-й день, этопозид 100 мг/м2 в/в в 1—3-й дни, прокарбазин (натулан) 100 мг/м2 перорально в 1—7-й дни, преднизолон 40 мг/м2 перорально в 1 —14-й дни, винкристин 1,4 мг/м2, но не более 2 мг в/в на 8-й день, блеомицин 10 мг/м2 в/в на 8-й день. Новый курс начинают на 22-й день. Курсы лечения следует проводить в условиях стационара, так как используемые препараты обладают значительной миелотоксичностью.
• При прогностически плохом течении заболевания лечение проводят по усиленному протоколу ВЕАСОРР: циклофосфамид 1250 мг/м2 в/в в 1-й день, доксорубицин 35 мг/м2 в/в в 1-й день, этопозид 200 мг/м2 в/в в
1—3-й дни, прокарбазин (натулан) 100 мг/м2 перорально в 1—7-й дни, преднизолон 40 мг/сутки перорально в 1—14-й дни, винкристин 2 мг в/в на 8-й день, блеомицин 10 мг/м2 в/в на 8-й день. Используемые препараты обладают значительной миелотоксичностью, поэтому необходимо назна¬чить гранулоцитарный или гранулоцитарно-макрофагальный колониести- мулирующий фактор [ленограстим (граноцит), филграстим (нейпоген), молграмостим (лейкомакс)].
• При прогрессировании заболевания на фоне лечения или при отсутствии по-ложительной динамики больного переводят на более интенсивную терапию с применением ломустина (белустин), этопозида, мелфалана, цитарабина, препаратов платины, больших доз дексаметазона. После полихимиотерапии перед началом лучевой терапии проводят контрольное обследование.
Рефрактерные формы, ранние рецидивы
высокодозная полихимиотерапия с мобилизацией стволовых клеток крови или костного мозга и их последующей аутотрансплантацией или трансплантацией аллогенного костного мозга.
Лечение поздних рецидивов (через год после полной ремиссии) проводят по схеме, при помощи которой ранее удалось достичь полной ремиссии.
паллиативное лечение для ослабленных больных пожилого возраста, а также в случаях, когда возможности полихимиотерапии можно считать исчерпанными. Применяют любой из противоопухолевых препаратов, входящих в схемы лечения лимфогранулематоза [например, винкри¬стин, винбластин, хлорамбуцил (хлорбутин), гемцитабин].
ЛИМФОГРАНУЛЕМАТОЗ И БЕРЕМЕННОСТЬ
При ранних сроках беременности (менее 3 мес) показан медицинский аборт с последующей полихимиотерапией в полном объёме. При сроках бе¬ременности более 3 мес показана терапия по программе СОРР, включающей циклофосфамид 750 мг/м2 в/в, винкристин 1,4 мг/м2 (но не более 2 мг) в/в, прокарбазин (натулан) 100 мг/м2 перорально в 1 — 14-й дни, преднизолон 40 мг/м2 перорально в 1—14-й дни. На этих сроках беременности цитостати- ки не проходят через плаценту. После родоразрешения показана терапия по программе ABVD и лучевая терапия.
Химиотерапия, лучевая терапия
Контрольные обследования проводят 1 раз в 3 мес в 1-й год после завершения терапии, 1 раз в 6 мес во 2-й год, 1 раз в год на 3-м году наблюдения и позже. Контроль показателей общего и биохимического анализов крови проводят 1 раз в 3 мес. Рентгенографию грудной клетки проводят 1 раз в год в течение 10 лет. Больным противопоказаны физиотерапия, инсоляции, беременность в первые 2 года после окончания терапии.
Средняя выживаемость в течение 5 лет составляет 60—80%. У пациентов с I или II стадией заболевания безрецидивная выживаемость в течение 5 лет превышает 90%. У больных со стадией пятилетняя выживаемость с полной ремиссией составляет примерно 70%. Проведение химиотерапии у больных со стадией III,*, IIIд или IV обеспечивает ремиссию в 80—95% случаев, более 70% пациентов живут более 5 лет.
Врач-гепатолог
Смежные специальности: гастроэнтеролог, терапевт.
Адрес: Санкт-Петербург, ул.Академика лебедева, д.4/2.

Патологические изменения могут носить как инфильтративный рассеянный, так и очаговый характер.
Лимфогранулематоз, иначе болезнь Ходжкина, получил свое второе название в честь Томаса Ходжкина, британского врача, который первым в середине 19 века подробно описал симптомы данного заболевания.
Именно их присутствие в лимфузлах является ключевым моментом при дифференциальной диагностике. Чаще всего заболеванию подвержены мужчины в возрасте 15-25 лет, женщины болеют значительно реже. У детей лимфогранулематоз встречается крайне редко, а симптомы имеют стертый характер.
Причины лимфогранулематоза
На сегодняшний день специалисты не пришли к единому мнению относительно природы возникновения данного заболевания.
Считается, что возникновение болезни Ходжкина обусловлено генетическими факторами, поскольку в большинстве случаев носителями заболевания становятся люди с нарушенной структурой хромосом, а также представители более молодых поколений одной семьи.
Не исключена передача лимфоцитов матери эмбриону, после чего развивается иммунопатологическая реакция. Существует еще одна популярная теория, согласно которой лимфогранулематоз имеет вирусную природу. Посетив форум по обсуждению данной патологии, можно узнать об иммунной теории происхождения болезни.
Специалисты выделяют несколько разновидностей вирусов, которые способны проникать в незрелые клетки лимфатических узлов, что становится причиной прекращения их созревания и начала патологического деления. Например, паховый лимфогранулематоз обусловлен хламидиозной инфекцией (проявляется в виде эрозии и воспаления паховых лимфоузлов).
Отдельно следует выделить венерическое происхождение заболевания. Лимфогранулематоз считается четвертой венерической болезнью из пяти. К их числу относится сифилис, гонорея, мягкий шанкр, а также донованоз (язвенное поражение гениталий).
Точные причины лимфогранулематоза пока не установлены, однако можно выделить предрасполагающие факторы. Таковыми считаются:
![]()
радиоактивное облучение (сюда же относят и облучение рентгеновскими лучами);- воздействие токсических химикатов (например, вдыхание паров красителей или лаков);
- воздействие некоторых фармакологических препаратов (антибиотики, сульфаниламиды, противовоспалительные, а также соли золота, используемые при лечении артритов);
- инфекционные и вирусные заболевания;
- последствия перенесенных оперативных вмешательств (трансплантация, а также резекция или удаление органов);
- регулярное нервное перенапряжение.
Подтверждением вирусного происхождения может стать факт перенесенного мононуклеоза, а также присутствие антител к вирусному возбудителю Эпштейн-Барр (в 20% случаев). Как гласит форум, лимфогранулематоз – частый спутник ВИЧ-инфекции.
Нередко пациенты спорят на форумах, является ли лимфогранулематоз раком или нет. Можно сказать, что является. Подтверждением злокачественного происхождения патологии являются огромные клетки с множеством ядер, о которых мы упоминали ранее. Помимо них клеточный состав опухоли представлен Т-лимфоцитами, эозинофилами, а также плазма- и гистиоцитами.
Симптомы лимфогранулематоза
Лимфогранулематоз у детей развивается из одного патологического участка, например, шейных или медиастинальных лимфоузлов. Последующее метастазирование может поражать легкие, костный мозг и пищеварительный тракт.
Теперь рассмотрим стадии патологического процесса и возможные клинические признаки болезни. Довольно часто первичные симптомы маскируются признаками других заболеваний, что заставляет пациентов обращаться к различным специалистам.
Стадийность заболевания у больных основана на распространенности патологического процесса:
- для первой стадии (локальной) характерно поражение одной лимфогруппы или одного органа внелимфатической локализации;
- на второй (регионарной) – поражаются две группы или один внелимфатический орган с регионарными лимфоузлами;
- при генерализованной стадии поражаются лимфоузлы с двух сторон, плюс один внелимфатический орган;
- для диссеминированной (четвертой) стадии характерно поражение нескольких экстралимфатических органов (легких, печени или пищеварительного тракта).
Добавление буквы А или В к номеру стадии указывает на наличие или отсутствие клинических симптомов у больных в течение полугода.
Наиболее характерным симптомом лимфогранулематоза является значительное увеличение в размерах лимфатических узлов. На ощупь они безболезненные, плотные, подвижные, не спаянные с окружающими тканями и располагаются в виде цепочки. Чаще всего поражаются узлы в районе паха, шеи и подмышечных впадин.
По мере прогрессирования болезни пораженные лимфоузлы сдавливают дыхательные пути, в результате чего у больных появляется кашель и затрудненное дыхание. Увеличение узлов средостения сопровождается симптомами дисфагии (нарушения глотания).
Если посмотреть на фото больных лимфогранулематозом, можно невооруженным глазом увидеть увеличенные лимфоузлы в районе шеи. Иногда они увеличиваются настолько, что явно деформируют контуры шеи. (тут надо вставить именно фото таких больных)
Кроме того, у больных повышается температура тела и отмечается усиленное потоотделение. За счет сдавления кровеносных сосудов может наблюдаться отечность лица и конечностей. В местах поражения лимфоузлов часто возникает зуд кожных покровов. Обычно у пациента увеличиваются селезенка и печень, в связи с чем может беспокоить боль как в левом, так и в правом подреберье. Отмечается слабость, апатичность и нарушения сна. Как правило, пациент теряет вес.
Посетив форум по заболеванию, можно узнать о частых случаях поражения легких в виде воспалительного процесса с формированием полостей, а также развитием плеврита. Также регистрируются случаи вовлечения в онкопроцесс костных структур (таза, ребер, позвонков), что сопровождается болевыми ощущениями.
При поражении костного мозга угнетаются ростки кроветворения, вследствие чего уменьшается количество эритроцитов, лекойцитов, а также тромбоцитов в кровеносном русле.
Лимфогранулематоз у детей и взрослых распространяется на пищеварительные органы, изъязвляет слизистую и повышает риск кровотечений. Поражение печени проявляется в виде гепатомегалии (увеличения органа) и повышения щелочной фосфатазы.
Возможные осложнения

В результате сдавления дыхательных путей лимфатическими узлами может возникать чувство удушья и нехватки воздуха.
При этом кожные покровы приобретают синеватый оттенок. При компрессии пищевода затрудняется глотательная функция.
При сдавлении желудочно-кишечного тракта могут возникать такие осложнения, как болезненность в эпигастральной области и кровавая рвота.
В результате внутренних кровотечений стул может приобретать черный оттенок (мелена).
При компрессии печени могут пострадать и желчные протоки, в результате чего возникает застой желчи с развитием желтушного синдрома. Он включает желтушность кожных покровов и слизистых, нарушения пищеварения, потемнение мочи, обесцвечивание каловых масса и покалывающие точечные боли в правом подреберье.
Случается так, что у пациента возникают частые позывы к мочеиспусканию, при этом мочевой пузырь не опорожняется до конца. В таких случаях есть основания заподозрить сдавление мочевыводящих путей.
Могут поражаться также клетки мозга (головного и спинного), в результате чего нарушается двигательная функция и чувствительность некоторых участков тела. Пациент страдает от сильных головных болей, ухудшается память, внимательность и логическое мышление.
Диагностика
Перед назначением диагностических исследований врач проводит сбор жалоб пациента, изучает историю его жизни и развития болезни. Необходимо выяснить, есть ли у пациента вредные привычки, наследственные заболевания или иммунная дисфункция.
Врач должен знать, какими препаратами лечился пациент длительное время, чем болеют его близкие родственники, был ли контакт с вредными химическими веществами, и пребывал ли он в экологически неблагополучных районах.
После этого проводится осмотр больного, в ходе которого особое внимание уделяется шейным, подмышечным и паховым лимфоузлам. Пальпируется (прощупывается) правое и левое подреберье на предмет увеличения печени и селезенки. Может также отмечаться бледность кожных покровов.
Артериальное давление обычно пониженное, при этом пульс слегка превышает норму. Если врач выявляет симптомы лимфогранулематоза, назначаются следующие лабораторные и инструментальные исследования:
![]()
общий анализ крови. При болезни Ходжкина может быть понижен уровень эритроцитов и, как следствие этого – уровень гемоглобина, а скорость оседания эритроцитов (СОЭ), наоборот, обычно повышается;- биохимический анализ крови. В первую очередь врач обращает внимание на такие параметры, как уровень креатинина, глюкозы, мочевой кислоты и холестерина;
- рентгенография грудной клетки. Данная диагностическая процедура проводится сразу в двух проекциях для определения разрастания опухолевого процесса в лимфатических узлах между легкими и сердцем. Кроме того, рентгенография позволяет выявить возможные повреждения внутренних органов;
- магнитно-резонансная томография (МРТ) позволяет получить максимально достоверную трехмерную визуализацию внутренних органов и возможных новообразований в них;
- ультразвуковое исследование (УЗИ) применяется для этих же целей, однако дает менее точную информацию в сравнении с предыдущей диагностической процедурой. Несмотря на это, УЗИ широко используется для первичной диагностики болезни;
- гистологическое исследование. Одна из наиболее болезненных для пациента диагностических процедур. При помощи длинной полой иглы под местным обезболиванием и контролем УЗИ осуществляется забор небольшого участка тканей. Ткани изучаются под микроскопом на предмет наличия клеток Березовского-Штернберга-Рида;
- позитронно-эмиссионная томография. В отличие от обычной компьютерной томографии ПЭТ позволяет получить трехмерную визуализацию при помощи радиофармпрепарата, который вводится пациенту перед началом исследования внутривенно. В роли индикатора обычно выступает раствор глюкозы с добавлением радиоактивных изотопов. За счет скопления и характерного свечения данного вещества в тканях с нарушенным метаболизмом врач получает трехмерное изображение того или иного органа. При подозрении на болезнь Ходжкина данная методика исследования считается более эффективной, чем МРТ или КТ;
- трепанобиопсия – диагностическая процедура, при которой происходит забор образцов костного мозга вместе с участком кости и надкостницы. Данное исследование позволяет определить степень распространения патологического процесса на костный мозг. Чаще всего образцы тканей берут из тазовой кости;
- спиральная компьютерная томография. Она представляет собой рентгенологическое исследование на разной глубине тканей, что позволяет с большей точностью определять локализацию онкологического процесса.
Лечение
Результат терапии зависит от своевременности выявления заболевания.
Чтобы вылечить пациента, следует использовать следующие методы:
Следует учесть, что лечение лимфогранулематоза чревато серьезными осложнениями, а именно выпадением волос, угнетением кроветворения, пищеварительной дисфункцией и нарушением обмена веществ с развитием ожирения. С большой долей вероятности может наблюдаться бесплодие за счет существенного снижения способных к оплодотворению половых клеток. Из-за нарушения кровоснабжения миокарда у пациента может развиваться сердечная недостаточность.
На 2В и 3А стадиях проводится комбинированное лечение с использованием нескольких химиопрепаратов и лучевой терапии, которой подвергаются не только увеличенные, но и неизмененные лимфоузлы.
Полихимиотерапия проводится согласно разработанным онкологическим схемам. Результатом лечения может стать полная или частичная ремиссия, уменьшение выраженности клинических симптомов, а также отсутствие положительной динамики, которое проявляется в виде сохранения симптоматики или прогрессии патологии. 
Прогноз
Прогноз лечения относительно благоприятный, несмотря на то, что лимфогранулематоз у детей и взрослых имеет злокачественное происхождение, и нет никакой уверенности, что онкологическое заболевание пройдет без осложнений.
Однако даже при агрессивных формах лимфогранулематоза как минимум две трети пациентов вылечились. Шансы на благоприятный исход существенно повышаются у молодых пациентов, поскольку регенеративные и защитные функции организма у них значительно выше, чем у пожилых пациентов.
Даже, если быстро вылечишься от лимфогранулематоза, нет гарантии, что не будет рецидива. Если ремиссия наблюдается на протяжении 5 лет, пациента можно отнести в группу полностью вылечившихся. Многие из них посещают форум, где обмениваются опытом в восстановлении здоровья и возвращении к полноценной жизни.
При 1, 2 стадиях выживаемость составляет 90% (в течение пяти лет при безрецидивной форме). На 3 стадии – 60-80% (в зависимости от наличия клинических симптомов), на 4 – не более 45%. Неблагоприятный прогноз лимфогранулематоза наблюдается при остром течении болезни, размерах конгломератов лимфоузлов более 5 см, а также одномоментном поражении более трех групп узлов в сочетании с селезенкой.
Также плохой прогноз отмечается при таком увеличении узлов средостения, когда они занимают 30% грудной клетки. Случаи рецидива регистрируются при нарушении схемы проведения поддерживающей терапии, при беременности и интенсивной физической нагрузке.
Ребенок с лимфогранулематозом должен находиться на учете у гематолога или онколога. Для ранней диагностики патологии требуется регулярное проведение флюорографии.
Симптомы, причины, патогенез и лечение лимфомы печени.
Читайте также:



