Где сделать морфологическую верификацию рака легких
Основная задача морфологической диагностики — установить тканевую принадлежность опухоли (гистогенез), при этом тщательно оценивается степень атипии самой клетки и нарушение тканевых структур. В большинстве случаев диагноз устанавливается по традиционно приготовленным препаратам, изучаемым при световой микроскопии. Для морфологического исследования используются различные методы забора материала:
— Соскобы и мазки-отпечатки. Являются распространенным способом диагностики поверхностных изъязвленных опухолей.
— Пункция. Выполняется при поверхностно расположенных узловых образованиях. При малых размерах подозрительных в отношении опухолевого роста образований возможно выполнение пункции под контролем УЗИ. В неясных случаях прибегают к проведению иммуногистохимических , электронно-микроскопических исследований , иногда выявляющих дополнительные морфологические признаки, позволяющие сопоставить опухоль с исходной тканью.В настоящее время при обнаружении опухоли внутренних органов возможно осуществить морфологическое исследование практически в любой части тела.
— Биопсия с забором участка ткани (браш-биопсия). Если пункцию выполнить невозможно, используют эндоскопические методы исследования: фаринго- и ларингоскопию, эзофагогастродуоденоскопию, торакоскопию, бронхоскопию, колоноскопию и др., в ходе которых под визуальным контролем обычно забирают участок ткани (биоптат или браш-биоптат — соскоб специальной щеточкой, смывы с поверхности образования и т.д.) для морфологического исследования.
— Открытая биопсия. Открытая биопсия опухоли выполняется, как правило, после неудачных попыток верифицировать диагноз вышеуказанными методами или из-за необходимости получить больше ткани для выполнения некоторых специфических исследований, например для определения рецепторов гормонов при опухолях молочной железы, иммуногистохимического исследования при гематосаркомах. Биопсия инцизионная предполагает получение участка ткани непосредственно из патологического очага, выполняется под местной анестезией (из опухоли молочной железы, мягких тканей) или под наркозом (из костных опухолей). Биопсия эксцизионная выполняется как хирургическое вмешательство с удалением опухоли в пределах здоровых тканей. Трепанобиопсия в основном используется для исследования новообразований молочной железы, костей, мягкотканных опухолей. При невозможности верифицировать злокачественность опухоли на диагностическом этапе планируют срочное гистологическое исследование во время операции.Эти способы обычно дают достаточно материала для морфологической верификации диагноза. Наиболее информативный материал получают из участков опухоли на границе со здоровой тканью.
— Трепан-биопсия. Гистологическая верификация может быть получена при использовании специальной иглы или трепана, при этом изымается столбик измененной ткани, пригодный для гистологического исследования. Особенно важным в плане адекватной диагностики распространенности опухолей бывает исследование сомнительных по клиническим данным образований в зонах регионарного метастазирования. В большинстве же случаев сопоставление клинических проявлений опухоли с ее симптомами вне основного очага не требует верификации всех обнаруженных метастазов. Производят морфологическое исследование наиболее доступных вторичных опухолей, что само по себе делает ясным представление об истинной распространенности заболевания. Верификация диагноза осуществляется путем чрезкожной пункции метастаза или забора материала при лапаро- или торакоскопии.
Важный этап диагностики рака – определение гистологического типа злокачественного новообразования. Верификация опухоли – это оценка морфологического (клеточно-тканевого) варианта карциномы, предполагающая проведение исследований с биопсийным материалом. Нельзя начинать лечение, не зная гистотип (тканевой состав) и клеточную дифференцировку раковой опухоли.
Выяснив клеточно-тканевой состав опухоли, можно начинать терапию
Верификация опухоли
До момента применения комбинированной терапии надо точно выяснить морфологическую структуру новообразования. Вражеская армия может состоять из агрессивных молодых и необученных бойцов, с которыми легко справится иммунная система. Или противоопухолевой защите придется столкнуться с живучим, хитрым и коварным противником, способным быстро изменяться и приспосабливаться.
Зная состав вражеского войска, можно предвидеть исход битвы.
Верификация опухоли – это микроскопическая оценка взятых при биопсии тканей, на основе которых врач-лаборант точно определит цитоморфологический состав злокачественного новообразования: важен не только факт обнаружения рака, но и гистологический вариант опухолевого роста с отличием от исходных здоровых клеток. Зная состав вражеского войска, можно предвидеть исход битвы.
Варианты биопсийного материала
Врач-лаборант, выполняющий морфологические исследования, будет работать со следующими видами биопсийного материала:
- Кусочки тканей, удаленных при проведении диагностической или лечебной операции;
- Соскоб из полых органов;
- Пунктат из опухоли;
- Мазок-отпечаток с поверхности злокачественного новообразования;
- Жидкость, удаленная из кистозной полости;
- Собранная в первичном очаге секреторная или экссудативная жидкость.
Любая ткань может стать основой для проведения качественной морфологической диагностики, но при одном важном условии – во время выполнения биопсии опухоли надо взять неповрежденный участок из карциномы. Чем сохраннее биоптат, тем качественнее диагностика.
Последовательность морфологических изменений
Рак в своем развитии проходит несколько стадий, поэтому врач-гистолог при проведении микроскопического исследования может увидеть разнообразные картины опухолевого роста – от предраковых изменений до выявления признаков распада злокачественного узла. Верификация опухоли – это обнаружение при исследовании одного из вариантов типичной последовательности онкологических изменений в тканях:
- Гиперплазия (диффузная и очаговая) – обратимый и не опасный процесс;
- Метаплазия (доброкачественное изменение);
- Дисплазия (предрак);
- Рак in situ (преинвазивное раковое поражение);
- Микроинвазия;
- Прогрессирующий рак с метастазированием.
Временные промежутки между этапами формирования опухоли относительны – иногда проходят десятилетия от первичных доброкачественных процессов к инвазии, в худших случаях от дисплазии к раку – за месяцы.

Врач-гистолог по срезам тканей поставит морфологический диагноз
Методы морфологии
Стандартный вариант проведения гистологического исследования – приготовление тончайших срезов биопсийных тканей с последующей микроскопией материала. Эта методика позволяет получить массу полезной информации о клеточно-тканевом составе опухоли. Кроме этого, верификация опухоли – это следующие диагностические методы:
- Гистохимия (использование химических реакций для определения разных вариантов биологически активных веществ опухоли);
- Иммуногистохимия (применение иммунных реакций взаимодействия опухолевых антигенов со специально созданными антителами);
- Иммунофлюоресценция (специальный краситель метит опухолевую ткань, позволяя врачу поставить точный диагноз);
- Иммуноферментный анализ (использование фермента для обнаружения рака).
Вне зависимости от методики, основная цель гистологического исследования – определение типа опухоли и оценка клеточных изменений: зная состав наступающей армии, можно выбрать тактику защиты или принять решение о контрнаступлении.
Влияние лечебных факторов на опухоль
Далеко не всегда с момента начала комбинированной терапии можно получить желаемый положительный результат. Ни хирургическая операция, ни химиотерапия, ни курсы облучения не гарантируют полного излечения, что объясняется способностью опухоли приспосабливаться и видоизменяться. Значительная часть вражеского войска погибнет, но те бойцы, которые смогли выжить, дадут новые генерации солдат, способных противостоять лечебным воздействиям. Лекарственные препараты и облучение способны разрушить опухолевую ткань, что приведет к некрозу и воспалению, но даже единичный метастаз, сохранившийся в лимфоузле, может стать основой для рецидива опухоли. Это вовсе не означает, что рак непобедим: зная, что враг коварен и хитер, нельзя расслабляться и успокаиваться после локальной победы. Длительное наблюдение у врача, поддержка противоопухолевого иммунитета и регулярные контрольные обследования помогут избавиться от болезни.

По словам профессора, обычная химиотерапия препятствует делению клеток, поэтому эффективна против злокачественных опухолей, так как их клетки характеризуются интенсивным делением. Однако эффективность данного метода лечения всегда ограничена потенциальным ущербом нормальным тканям организма. Иммунотерапия отличается тем, что не воздействует на клетки злокачественной опухоли напрямую, позволяя иммунной системе самостоятельно обнаруживать и уничтожать опухолевые клетки. Поскольку применение иммунотерапии активирует собственную иммунную систему организма, эффективность лечения может быть значительно выше по сравнению с другими видами лекарственной терапии.
Сегодня лечение онкологических заболеваний перешло на так называемую персонализацию. Проводится полная морфологическая верификация диагноза и затем подбираются варианты лечения, которые будут направлены на борьбу с опухолью.
По словам онколога, раньше, например, пятилетней выживаемости при четвертой стадии рака легкого заболевания практически не было. Но сегодня при использовании иммунотерапии при распространенном раке легкого можно говорить, что в некоторых группах, каждый третий пациент потенциально может пережить этот срок наблюдения. Сегодня в России, как и во всем мире, доступна иммунотерапия. В настоящее время иммуноонкологические препараты входят в перечни ЖНВЛП и ОНЛС, поэтому многие пациенты с онкологическими заболеваниями имеют право на их получение, сообщает Меддейли.
Ранее медики назвали 5 признаков рака, которые люди часто не воспринимают всерьёз. Так, например, увеличение лимфатических узлов, которые не болят, говорят о развитии рака лимфатических узлов. Именно с этого началось заболевание у Кирилла Малышева. Смоленск сравнительно небольшой городок, где все друг друга знают. Весть о его болезни сразу же разлетелась не только по всем редакциям, в силу специфики его работы, но и по всему городу. Пожалуй, это первый в Смоленске человек, который не только спокойно, но ещё и с юмором может рассказывать о страшном заболевании – раке. Причём не о чужом, а о своём. О раке из первых уст.
Напомним, в Смоленской области от рака умирает каждый седьмой человек. За полугодие в Смоленской области умерло 7283 человек. От новообразований в нашем регионе погибли 1005 человек, что больше на 11 пациентов, чем за аналогичный период прошлого года.
Smolnarod решил выяснить причины смертности от онкологических заболеваний в Смоленской области. За комментариями мы обратились к главному врачу Смоленского областного онкологического диспансера Александру Эфрону. О самых распространённых в нашем регионе видах рака, причинах заболеваемости и способах выявления читайте в нашем материале.
Предположить характер новообразования в организме можно благодаря клиническим и рентгенологическим симптомам, а вот определить его гистогенетическую принадлежность можно только благодаря морфологической верификации диагноза. Основной задачей такой диагностики является перепроверка онкологического диагноза для его подтверждения и подбора эффективного курса химиотерапии.
Морфологическая верификация
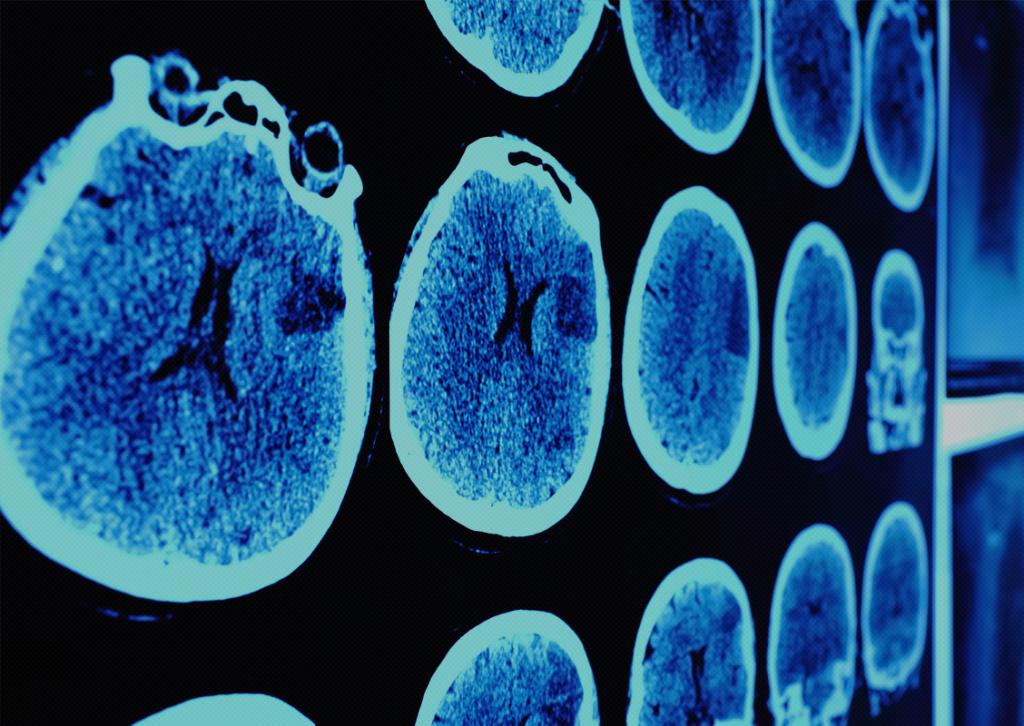
Услышав впервые от доктора о необходимости проведения морфологической диагностики, многие не имеют представления, что это и для чего проводится.
Верификация является важным исследованием, без которого невозможно принять решение о дальнейших действиях. Морфологическая верификация - это медицинская процедура, которая помогает подтвердить или опровергнуть онкологический диагноз. Чтобы провести исследование, необходимо получить материал. Его выбор в основном зависит от локализации образования. После проведения исследования специалист в зависимости от результата определяет дальнейшую тактику лечения, которая может быть консервативной или хирургической. Только после морфологического подтверждения может планироваться адекватное лечение. Показанием для проведения верификации являются объемные образования или диффузные изменения органа или его структур. Для проведения морфологического исследования забор ткани осуществляется следующим образом:
- при поверхностных изъявленных опухолях берется соскоб и мазки-отпечатки;
- при неглубоко размещенных узловых образованиях проводится пункция;
- при невозможности взятия пункции проводится биопсия с забором участка ткани;
- после неудачных попыток верификации всеми перечисленными выше методами проводится открытая биопсия.
Морфологическая верификация диагноза практически ничем не отличается от цитологической пункции. Чтобы взять материал на исследование, сначала человеку проводят анестезию мягких тканей и кожного покрова, после этого выполняется незначительный разрез кожи, через который внедряется специальный инструмент в мягкие ткани и непосредственно в ткань опухоли. Все последующие действия напрямую зависят от используемого прибора.
Методы верификации
Стандартным вариантом гистологической верификации диагноза является забор тончайших срезов биопсийных тканей для последующего микроскопического исследования. Благодаря им получается полезная информация о составе опухоли.
Морфологическая верификация опухоли проводится следующими способами:
- гистохимией;
- иммуногистохимией;
- иммунофлюоресценцией;
- иммуноферментным анализом.
Независимо от того, какая методика для проведения исследования будет выбрана, целью верификации является не только определение разновидности опухоли, но и оценка клеточных модификаций. По результатам исследования появляется возможность безошибочно принять решение и выбрать тактику лечения.
Гистохимическое исследование

С помощью гистохимической методики можно получить ценную информацию о функциональной активности образования, его типе и гистогенезе. Данный метод позволяет точно поставить диагноз и решить вопрос его дифференциальности.
В расположении гистохимии находятся многочисленные реакции, которые оказывают содействие выявлению разных классов веществ.
Иммуногистохимия
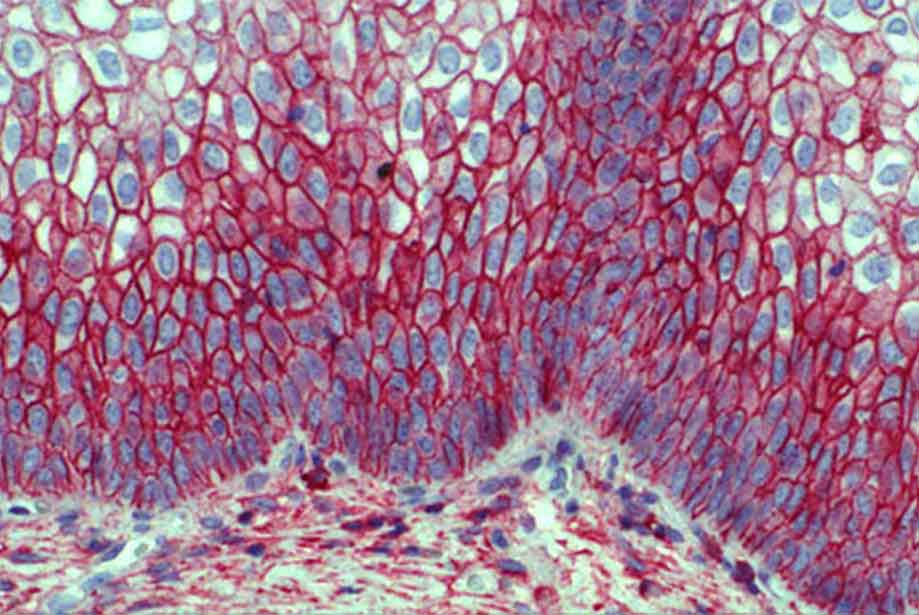
ИГХ является методом визуализации, который помогает определить локализацию веществ в препаратах тканевых срезов. В основе данного метода лежит принцип характерного взаимодействия антигенов с антителами, полученными особенным методом.
Иммунофлуоресценция
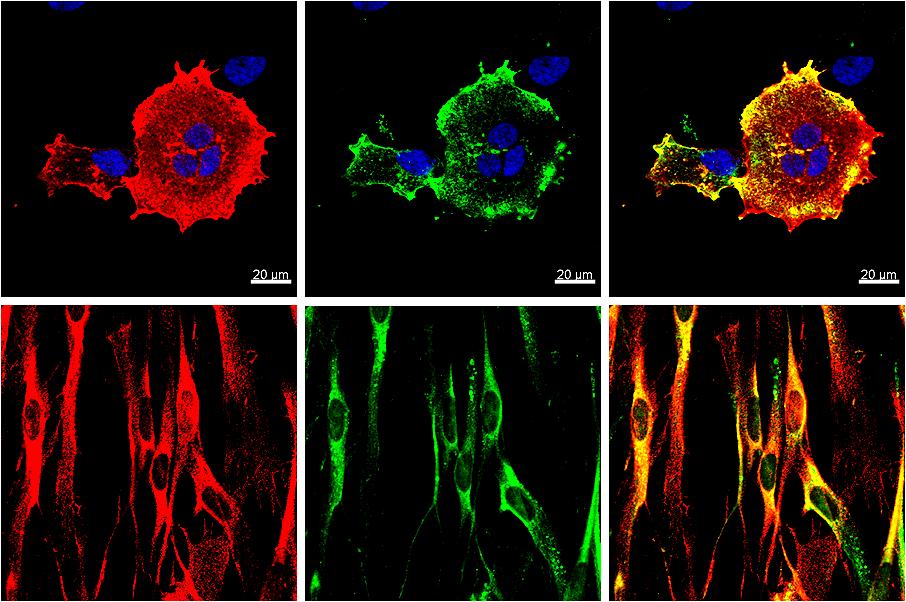
Метод исследования основан на чувствительности флюоресцентной микроскопии и специфичности иммунологической реакции. В процессе его проведения опухолевая ткань метится специальным красителем, который помогает доктору точно определить диагноз. Особенностью этого метода является простота и необходимость использования минимального количества изучаемого материала.
Иммуноферментный анализ
Метод диагностики обладает высокой восприимчивостью и позволяет устанавливать минимальные количества вещества. В современных методах диагностики именно с помощью этого способа определяется локализация антигена. Для проведения анализа используются специальные ферменты для обнаружения рака.
Независимо от выбранной методики целью любого морфологического исследования считается точное определение типа опухоли и оценки изменений на клеточном уровне. Можно сказать простыми словами, что морфологическая верификация - это определение разновидности опухоли и ее запущенности для правильного выбора тактики лечения.
Методы получения материала для морфологического исследования
Для морфологической верификации диагноза необходимо получить материал. Сделать это можно следующими способами:
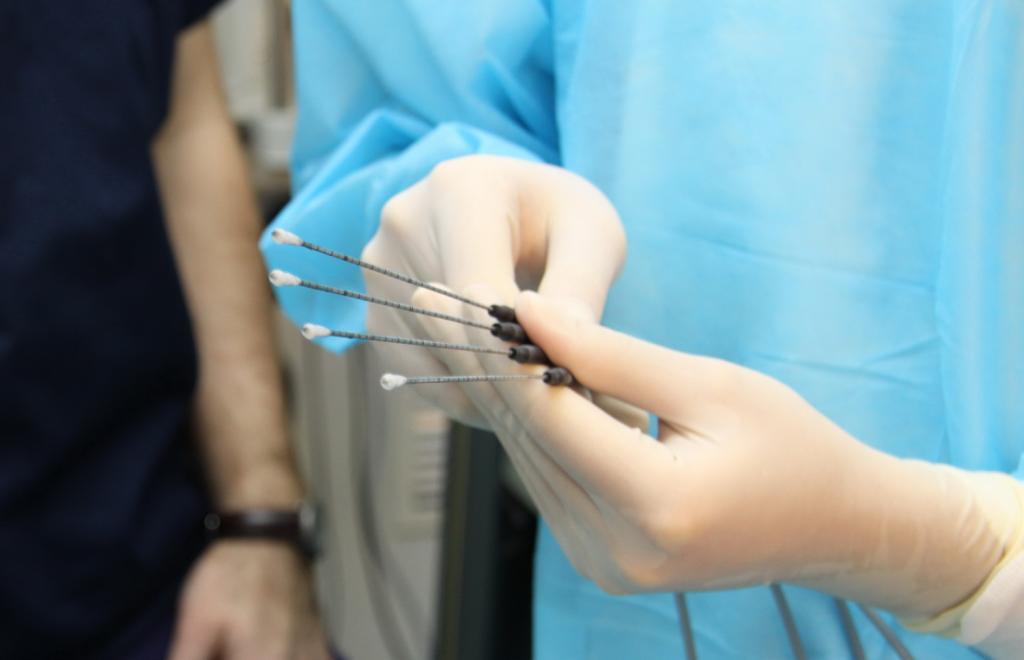
- Трепан-биопсия – считается одной из самых результативных процедур, несмотря на то что имеет определенные недостатки. Для взятия материала используются специальные иглы с внутренними режущими механизмами. С их помощью получается столбик ткани из опухоли. Этот метод позволяет провести морфологическую верификацию молочных желез, предстательной железы, легкого, печени, позвоночника и лимфатических узлов.
- Инцизионная биопсия – самый популярный метод, который выполняется с помощью скальпеля, которым берется материал из центра подозрительных участков, по периферии опухоли. При этом обязательно нужно делать это вне зон отека, некроза и кровоизлияния грануляционной ткани.
- Эксцизионная биопсия – суть такого метода заключается в полном радикальном удалении опухоли. Этот способ применим только если новообразование имеет небольшие размеры. В таком случае этот способ наиболее предпочтителен, так как имеет как диагностическое, так и терапевтическое значение.
Выбор способа морфологической верификации определяет лечащий врач в зависимости от особенностей сложившейся ситуации.
Последовательность морфологических изменений
Что это такое морфологическая верификация диагноза, и в какой последовательности происходят изменения в процессе развития рака, знают не многие. К сожалению, в основном люди начинают интересоваться подобной информацией, только когда сталкиваются с проблемой.
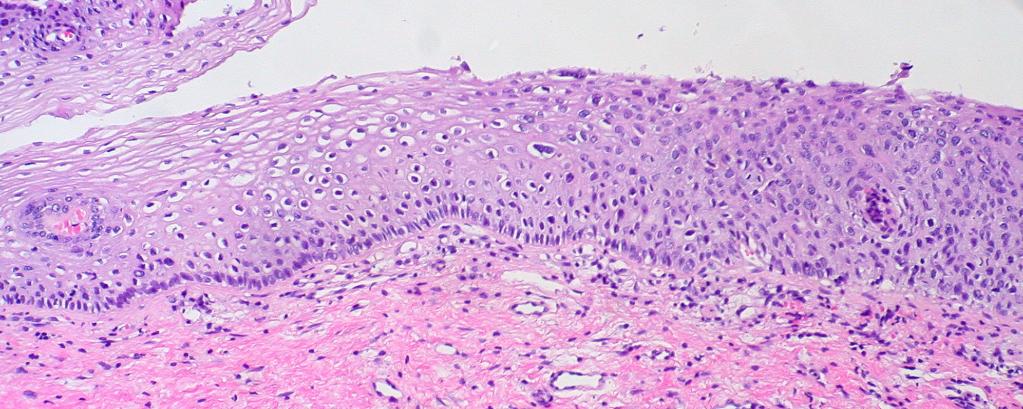
Онкология в процессе развития проходит определенные стадии, и в результате проведения морфологической верификации доктор может наблюдать разные нюансы развития. При верификации могут обнаруживаться следующие изменения в тканях:
- диффузная и очаговая гиперплазия – процесс не опасный и обратимый;
- метаплазия – доброкачественное новообразование;
- дисплазия – предраковое образование;
- рак in situ – преинвазивное раковое поражение;
- микроинвазия;
- прогрессирующий рак с метастазированием.
Промежутки времени между перечисленными этапами индивидуальны и в каждом отдельном случае могут варьироваться от нескольких месяцев до десятилетий.
Главной задачей морфологической диагностики является установление тканевой принадлежности опухоли. При этом выявляется не только ее наличие и разновидность, но и скрупулезно оценивается степень атипии клетки и нарушение тканевых структур. Чаще всего проводится морфологическая верификация щитовидной железы, молочной, предстательной, печени, почек и позвоночника. Метод проведения исследования в каждом отдельном случае определяется персонально.
РАК ЛЁГКИХ
Диагностика рака легкого
В настоящее время у онкопульмонологов благодаря использованию полного арсенала комплексной диагностики выработан определенный алгоритм диагностической тактики у больных с опухолью легкого:
- Первичная диагностика рака легких с установлением локализации и клинико-анатомической формы опухоли
- Уточняющая диагностика, направленная на определение степени распространения опухоли, установление ее операбельности.
- Морфологическая верификация опухоли с уточнением гистологической структуры и степени дифференцировки опухоли.
- Определение исходного статуса больного, функциональных возможностей жизненно важных органов и систем с целью планирования тактики лечения.
Объективное обследование (наружный осмотр, аускультация) имеет при раке легкого второстепенное значение, особенно при его распознавании на ранних этапах заболевания. В поздней стадии рака легкого клиническая картина осложняется симптомами его распространения за пределы пораженного легкого с вовлечением в процесс лимфатических узлов средостения и(или) шеи, плевры, грудной стенки, возвратного и диафрагмального нервов, а также метастазами в других органах. Диагностика рака легких при этом несложна, но лечение уже малоэффективно.
Рентгенологический метод является ведущим в диагностике рака легкого. Он включает в себя: 1) стандартную рентгенографию в прямой и боковой проекциях, 2) томографию в прямой, косой и боковой проекциях, 3) компьютерную томографию грудной клетки (с контрастным усилением).
Не останавливаясь подробно на описании рентгенологической картины опухоли легкого, отметим только, что основные проявления центрального рака легких обусловлены нарушением вентиляции участка легкого вследствие сужения пораженного бронха. Это проявляется уменьшением прозрачности сегмента или доли, расширением сосудистого рисунка. Нарастающее нарушение бронхиальной проходимости при раке легких приводит к развитию обтурационной пневмонии, что проявляется уменьшением объема и неоднородным уплотнением сегмента.
Периферический рак легких выявляется в виде узла в паренхиме легкого овоидной, полигональной или шаровидной формы, или инфильтрата с размытыми, нечеткими контурами. Вокруг узла обычно имеется неравномерная лучистость, что более характерно для быстрорастущих низкодифференцированных опухолей. Встречаются полостные формы периферического рака легких с неоднородными участками распада.
Рентгенологическое исследование больного раком легких должно быть направлено также на выявление увеличенных лимфатических узлов корней легких и средостения. При раке легких поражение бронхопульмональных лимфатических узлов характеризуется расширением тени корня легкого, наружный контур корня полициклический или выпуклый. Очень часто, особенно на томограммах, в корне видны округлые тени. Лимфатические узлы этой регионарной группы нередко сливаются с тенью первичной опухоли. При поражении лимфатических узлов верхней трахеобронхиальной группы тень средостения в верхних отделах расширена, контур ее выпуклый или полициклический.
Важнейший симптом рака легких — увеличение трахеобронхиальных лимфатических узлов справа — выявляется на прямых томограммах потерей дифференцировки тени непарной вены. Поражение лимфатических узлов паратрахеальной группы характеризуется расширением верхних отделов средостения. Тень увеличенных лимфатических узлов может сливаться с тенью ателектаза верхней доли. Поражение бифуркационных лимфатических узлов при раке легких распознается по увеличению угла бифуркации трахеи и дугообразному оттеснению средней трети контрастированного пищевода влево и кпереди.
Следует отметить, что увеличение размеров лимфатических узлов еще не свидетельствует об их опухолевой природе — это наблюдается у 40 % больных раком легкого. В связи с этим рентгенологические данные о наличии увеличенных лимфатических узлов, несомненно, имеющие самостоятельное диагностическое значение, используются также для отбора больных раком легких с целью морфологической верификации при помощи бронхологического (трансбронхиальная пункция) или хирургических (медиастиноскопия, видеоторакоскопия) методов.
Рентгеновская компьютерная томография - более информативный метод диагностики рака легких по сравнению с традиционным рентгенологическим исследованием, несмотря на дороговизну, в последние годы в специализированных клиниках является обязательным методом исследования. Он наиболее эффективен при диагностике метастазов в отдаленных органах. Наиболее ценным методом при выявлении метастазов в головном мозге при раке легких является магнитно-резонансная томография (МРТ).
Иногда для определения отношения первичного рака легких и лимфогенных метастазов к магистральным сосудам корня и средостения, рентгенологическое исследование дополняется рентгеноконтрастными методами исследования рака легких – бронхографией, ангиопневмографией, бронхиальной артериографией, контрастным исследованием пищевода и др.
Бронхологическое исследование - одно из основных в диагностике рака легкого. Современные фибробронхоскопы позволяют под местной анестезией рассмотреть бронхиальное дерево, включая самые мельчайшие разветвления бронхов. Различают прямые и косвенные анатомические признаки бронхогенного рака легких. К прямым относят опухолевые разрастания различной формы, окраски и плотности; инфильтраты слизистой оболочки с измененной поверхностью; сужение или ампутация бронха с ригидностью стенок.
Косвенные признаки рака легких: уплощенные шпоры между бронхами, сдавление бронхов, уплотнение их стенок, нарушение подвижности и дислокация устьев, стертость хрящевого рисунка, рыхлая, отечная, кровоточащая слизистая оболочка и др. Бронхологическое исследование позволяет не только визуально исследовать все бронхи, увидеть непосредственно опухоль, определить границы распространения рака легкого при расположении в бронхе, косвенно судить об увеличении лимфатических узлов корня легкого и средостения, но и произвести биопсию для гистологического исследования, получить материал как для гистологического (кусковая биопсия), так и для цитологического (мазки-отпечатки, соскоб или смыв из бронхиального дерева, транстрахеобронхиальная пункция) исследования, то есть морфологического подтверждения диагноза и уточнения гистологической структуры опухоли.
Морфологическая верификация диагноза достигается в 95-100% случаев при центральном раке легкого и в 50-70% - при периферическом. Направленная катетеризация бронхов под рентгенологическим контролем повышает частоту морфологической верификации диагноза при периферическом раке легких до 95%.
В последние годы в эндоскопии больных раком легких внедряются высокотехнологичные бронхологические методики: хромобронхоскопия, флюоресцентная бронхоскопия на основе аутофлюоресценции или с использованием дериватов гематопорфирина и криптонового лазера, ультразвуковая бронхоскопия, бронхорадиометрия. Эти методики позволяют выявить рентгенонегативный и самые начальные, доклинические формы центрального рака легких, то есть повышают результативность истинно ранней диагностики заболевания.
УЗИ органов брюшной полости – рутинный метод, позволяющий выявить метастазы рака легких в паренхиматозных органах и лимфатических узлах брюшной полости и забрюшинного пространства или исключить их наличие. Для больных раком легких УЗИ грудной клетки применяется редко, чаще всего при выпотном плеврите, перикардите, врастании опухоли в грудную клетку, а также при рецидивах опухоли после удаления легкого. Радионуклидные методы исследования - сканирование легких, сканирование костей скелета, позитронно-эмиссионная томография также применяются для выявления отдаленных метастазов.
Серологические маркеры все чаще применяются преимущественно для лабораторного контроля возможного прогрессирования опухоли после радикального лечения. Онкомаркеры рака легких – это вещества, определяемые в крови в больших концентрациях при опухолевом процессе. Некоторые из них имеют специфичность при конкретных гистотипах опухоли, например, нейронспецифическая енолаза при мелкоклеточном раке легкого.
Хирургические (инвазивные) методы диагностики рака легких направлены на уточнение степени распространения опухоли, а также получения морфологической верификации диагноза. Прескаленная биопсия – удаление нижних шейных лимфатических узлов – применяется при их увеличении у больных раком легкого или при рентгенологическом проявлении обширного метастазирования в лимфатических узлах средостения. Сейчас чаще применяется пункционная аспирационная биопсия этих узлов, по показаниям – под контролем УЗИ.
Медиастиноскопия и парастернальная медиастинотомия – методы прямого визуального и пальпаторного исследования лимфатических узлов передневерхнего средостения, а также определения отношения рака легкого и регионарных метастазов к окружающим органам и структурам. Оба метода позволяют выполнить биопсию лимфоузлов средостения и уточнить характер их поражения. Из инвазивных методов исследования наиболее распространенным в последнее время является диагностическая видеоторакоскопия. Показаниями к ней являются: экссудативный плеврит неясного происхождения, необходимость уточнения степени распространения рака легкого, опухоли средостения, внутригрудная лимфаденопатия, метастатическое поражение легкого и плевры, первичные опухоли плевры и др.
Для планирования лечения больного раком легкого важнейшее значение имеет морфологическое (гистологическое, цитологическое) подтверждение диагноза рака легких и уточнение его типа. Цитологическое исследование мокроты является одним из первых диагностических мероприятий у больных с легочной патологией и одновременно простым способом морфологической верификации диагноза. Это исследование позволяет выявить даже рентгенонегативный рак и применяется как скрининговый тест в группах риска. Целесообразно исследовать мокроту не менее 5-6 раз. Раковые клетки обнаруживают у 50-80% больных центральным раком легкого и у 30-60% - периферическим.
Методом морфологической верификации периферического рака легкого является трансторакальная (чреcкожная) пункция опухоли легкого под ультразвуковым, рентгенологическим или компьютерно-томографическим контролем с цитологическим исследованием пунктата. Диагноз рака удается подтвердить у 80% больных. На результатах морфологического исследования базируется окончательный диагноз и определяется тактика лечения, поэтому чрезвычайно важна квалификация и опыт патоморфологов, участвующих в постановке диагноза рака легкого.
Ранняя диагностика рака легкого
Больные с опухолью легкого поступают в специализированные стационары в запущенных стадиях, когда возможность радикального лечения исключается. По разным данным, от 35 до 80% больных раком легкого выявляются с III-IVстадией. В связи с этим онкологи встали на путь активного выявления опухоли до ее клинических проявлений. Ранняя диагностика рака легкого – это организационная работа, направленная на выявление опухоли в доклиническом периоде развития. Она осуществляется, прежде всего, массовыми профилактическими рентгенологическими обследованиями населения.
Массовые флюорографические исследования с целью выявления рака легкого в нашей стране и за рубежом проводятся с 1950-х гг. Выявляемость опухоли среди практически здорового населения незначительная, поэтому многие авторы рекомендовали проведение профилактических осмотров только среди контингентов с повышенным риском заболевания рака легкого. Однако эпидемиологическая обстановка по отношению к туберкулезу легкого не позволила отказаться от полного обследования населения. Необходимым условием эффективной флюорографической диагностики наряду с достаточным количеством современных флюорографов, является наличие квалифицированных специалистов.
Однако даже при активной работе этих комиссий наблюдалась достаточно большая доля запущенных случаев рака легкого . Причины позднего выявления больных скрыто протекающим раком легкого : а) небрежное отношение больных к своему здоровью; б) врачебная ошибка (пропуск патологии); в) особенности течения заболевания (быстрый рост опухоли при отсутствии симптомов). В странах Северной Америки и Западной Европы проводились и проводятся исследования по рентгенологическому и цитологическому скринингу рака легкого .
По результатам большинства из них массовое применение компьютерной томографии как высокочувствительного метода ранней диагностики рака легких , не оправдало себя ни в экономическом, ни в медицинском отношении. Смертность от рака легкого в обследованных контингентах достоверно не уменьшилась, тем временем финансовые затраты были огромными. Последние годы в рамках научных исследований, в том числе в нашей стране, проводится бронхологический скрининг с применением новейших бронхоскопов (ультразвуковых, ауто- и хромофлюоресцентных), которые позволяют выявлять участки предраковых изменений в слизистой оболочке бронха, недоступные обычным оптическим методам.
Диагностика предопухолевых поражений и минимальных участков рака легких позволяет радикально излечить больного на доклинической стадии и избегнуть травматичных оперативных вмешательств. Проводится также цитологическое исследование мокроты в контингентах группы риска (курильщики старше 40 лет, лица, страдающие хроническими бронхолегочными заболеваниями). Однако основным методом ранней диагностики рака легких по-прежнему остается флюорографическое исследование, рекомендуемое всему населению раз в год, а лицам из групп риска – два раза в год.
Читайте также:

