Энуклеация опухоли печени это
Хирургическое удаление опухоли — единственный радикальный метод лечения рака печени. Однако, операцию можно выполнить далеко не у всех пациентов. Зачастую очагов много, и они разбросаны по всему органу, опухоли оказываются слишком большими или успевают прорасти в кровеносные сосуды, желчевыводящие пути, соседние органы.
При раке печени проводят два вида хирургических вмешательств:
- резекция — удаление части органа;
- трансплантация.
Возможность радикального хирургического лечения определяют по данным КТ и МРТ с ангиографией. При неоперабельных опухолях прибегают к возможностям интервенционной хирургии.
Резекция печени
Такая операция может быть выполнена только при определенных условиях:
- Опухоль локализованная (находится в одном месте) и не прорастает в кровеносные сосуды.
- Очаг относительно небольшого размера.
- Нет метастазов в лимфатических узлах и других органах.
- Ткань печени не поражена циррозом и может нормально справляться со своими функциями.
К сожалению, возможность удалить злокачественную опухоль есть далеко не всегда. В зависимости от объема, резекция печени может быть долевой, сегментарной, атипичной.

Насколько большую часть печени можно удалить во время операции? Печень обладает высокой способностью к регенерации, поэтому во время резекции врач может удалить достаточно большую часть органа. Прежний размер восстанавливается примерно через 6 месяцев. Однако, хирург должен действовать предельно аккуратно. Нужно постараться полностью удалить опухоль, при этом оставить как можно больший объем здоровой ткани.
Если обнаружен цирроз — означает ли это, что врачи однозначно откажут в операции? В целом цирроз является противопоказанием к резекции. Даже если удалить небольшое количество ткани, есть риск, что оставшаяся часть печени не сможет адекватно справляться со своими функциями.
Но иногда, если функции печени нарушены не сильно, операция всё же возможна. Для того чтобы оценить функциональное состояние органа, пользуются пятью критериями Чайлда-Пью: уровень билирубина и альбумина в крови, протромбиновое время (показатель свертываемости крови), наличие асцита (скопления жидкости в брюшной полости), печеночной энцефалопатии (поражения мозга в результате нарушения функции печени).
Пациентов делят на три класса:
- Класс A — когда все пять показателей в норме. У таких больных резекция, скорее всего, возможна.
- Класс B — легкие отклонения от нормы. Вероятность того, что пациента возьмут на операцию, ниже.
- Класс C — тяжелые отклонения. Хирургическое лечение противопоказано.
Почему резекция печени считается сложным хирургическим вмешательством? Проведение операции требует от хирурга большого опыта, потому что:
В Европейской онкологической клинике работают опытные врачи-гепатоонкологи и функционирует превосходно оснащенная операционная. Мы выполняем операции любой сложности при раке печени и других органов пищеварительной системы.
Трансплантация печени
Для некоторых онкобольных с нерезектабельным раком альтернативой может стать трансплантация печени. Хирург удаляет пораженный опухолью орган и заменяет его на донорский. Трансплантация возможна, когда есть один очаг не более 5 см в диаметре или 2–3 очага, диаметр каждого из которых не превышает 3 см. При этом опухоль не должна прорастать в кровеносные сосуды, не должно быть метастазов.
Получить донорскую печень можно от трупа или от живого донора, в роли которого обычно выступает близкий родственник. В России, как и во всех странах мира, ситуация с донорскими органами напряженная. Пересадка печени бывает необходима не только при раке, но и при других заболеваниях: вирусных гепатитах, циррозе, болезни Вильсона-Коновалова.
Хирургическая тактика в зависимости от стадии
Резектабельная опухоль I–II стадии. К сожалению, такая ситуация встречается редко, но она позволяет провести радикальную операцию, удалить пораженную часть органа, и после этого может наступить ремиссия. Хирургическое лечение дополняют курсом неоадъювантной химиотерапии.
Нерезектабельная опухоль, когда не поражены регионарные (близлежащие) лимфатические узлы, нет метастазов. Проводят паллиативную терапию. Прибегают к методам интервенционной хирургии:
- Радиочастотная аблация — процедура, во время которой тонкий электрод в виде иглы вводят в опухоль и разрушают её током высокой частоты.
- Химиоэмболизация — введение в сосуд, питающий опухоль, особого эмболизирующего препарата в сочетании с химиопрепаратом. Эмболизирующий препарат состоит из микрочастиц, которые блокируют приток крови к опухолевой ткани, а химиопрепарат уничтожает раковые клетки.
- Интраартериальное введение химиопрепаратов. Лекарство вводят в печеночную артерию, благодаря чему оно оказывает более мощное локальное действие и не поступает в общий кровоток. Такое лечение пациенты переносят лучше, чем системную химиотерапию (внутривенное введение препаратов).

Иногда эти меры помогают уменьшить опухоль и сделать её резектабельной.
Небольшая опухоль, которая неоперабельна из-за другого заболевания. Бывают ситуации, когда операцию нельзя проводить из-за цирроза или других противопоказаний, не связанных с самим раком. В таких случаях применяют радиочастотную аблацию, химиоэмболизацию, химиотерапию, таргетную терапию.
Рак печени, который успел распространиться в лимфатические узлы и метастазировать. Такие опухоли имеют неблагоприятный прогноз. Но даже в запущенных случаях пациенту можно помочь, облегчить симптомы при помощи правильного паллиативного лечения.
Рецидивирующий рак печени. Если рецидив локальный, без распространения в лимфоузлы и метастазов, можно повторно провести резекцию. В других случаях лечение будет носить паллиативный характер.
Операции при метастазах рака в печень
Чаще всего раковые клетки метастазируют в печень из опухолей легких, кишечника, желудка. Если есть один или несколько мелких очагов, проводят резекцию. В других случаях применяют радиочастотную аблацию, химиоэмболизацию, назначают химиотерапию, таргетную терапию.
В Европейской онкологической клинике проводятся миниинвазивные вмешательства, которые помогают справиться с осложнениями рака: механической желтухой, асцитом.
Сколько живут после операции при раке печени?
Рак печени — злокачественная опухоль, с которой очень сложно бороться. Даже после резекции в течение 5 лет остается в живых не более 20% больных.
После радикальной операции в печени могут продолжаться патологические процессы, которые вызвали рак, со временем они приведут к рецидиву.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
- Показания
- Техника проведения
Техника энуклеации предполагает экстирпацию новообразования без нарушения целостности стенок ограничивающей его капсулы и вырезания (иссечения) окружающих тканей. А в случаях энуклеации целого органа операция должна проводиться без рассечения его оболочки.

[1], [2], [3], [4], [5], [6], [7], [8], [9]
Показания
Основные показания к проведению энуклеации включают наличие небольших по размеру опухолей доброкачественного характера с локализацией в молочных железах (фиброаденома, липома), предстательной железе (аденома простаты), бартолиновой, щитовидной железе, а также одиночные узловые образования миометрия (мышечного слоя матки) у женщин детородного возраста.
На сегодняшний день энуклеация является методом выбора при параовариальных кистах и тератоме яичника; ретенционных кистах влагалища и шейки матки; непаразитарной кисте печени или селезенки; кистозных образованиях в молочной железе (см. – Лечение кисты молочной железы); кисте сальной железы (см. – Удаление атеромы); в стоматологии – при десневых кистах.
Энуклеация целого органа чаще всего проводится в офтальмологической хирургии по поводу тяжелых травматических (проникающих) повреждений глазного яблока, а также при злокачественной опухоли глаза (ретинобластоме или увеальной меланоме).
Кроме того, можно говорить об идентичности терминов: лапароскопический метод удаления, то есть через небольшие разрезы – путем лапароскопического доступа к органу – с использованием оптического инструмента лапароскопа, и эндоскопический способ (поскольку при проведении операции используют тот же эндоскоп, вводимый путем лапароскопии). Также можно встретить название операции – эндоскопическое вылущивание. В любом случае хирург проводит операцию специальными инструментами, глядя на монитор.
Сегодня проводится и лазерная энуклеация – с помощью коротковолновых лазеров, в том числе, неодимовых и гольмиевых. Специалисты заверяют, что лазерная энуклеация является эффективным малотравматичным методом удаления четко локализованных и отграниченных доброкачественных опухолей и кистозных образований, обеспечивающим успешный результат с минимальной кровопотерей и быстрым заживлением.

[10], [11], [12]
Техника проведения энуклеации
Удаление или энуклеация глазного яблока может производиться, когда невозможно иссечь раковую опухоль глаза больших размеров, при сопровождаемой нестерпимыми болями терминальной стадии глаукомы (зрение в больном глазу при этом уже потеряно), а также, если невозможно спасти глаз из-за тяжелой травмы или ранения.
Энуклеация глазного яблока обычно проводится под общим наркозом и длится в среднем не более 1-1,5 часа. Сразу же после того, как глазное яблоко было удалено, в глазнице размещают орбитальный имплантат чуть меньшего размера, чем глазное яблоко. Это позволяет сохранить тонус глазных мышц и облегчить дальнейшее офтальмологическое протезирование.
Больше информации в материале – Энуклеация глазного яблока

[13], [14], [15]
Стандартом хирургического лечения большинства доброкачественных овариальных кист считается энуклеация кисты яичника, при которой не проводят вскрытие и аспирацию ее содержимого, а удаляют непосредственно все образование. При этом окружающие кисту ткани не затрагиваются. Энуклеация имеет то преимущество, что весь образец отправляется для срочного гистологического исследования, так что онкология не может быть пропущена.
Одним из распространенных способов энуклеации кист яичника является лапароскопическая операция – см. подробнее Лапароскопия кисты яичника. Среди преимуществ такого оперативного вмешательства отмечаются низкий уровень инвазивности и быстрая послеоперационная реабилитация: через несколько часов после операции пациентки могут вставать и передвигаться, выписка из клиники происходит на второй-третий день, а ограниченный режим продолжается не более месяца.
Медики отмечают, что энуклеация кисты яичника без вскрытия капсулы гарантирует, что ее содержимое не попадет в брюшную полость. Это особенно важно при наличии дермоидной и муцинозной кист, а также папиллярной цистоаденомы. И данный хирургический метод позволяет избежать серьезных осложнений в будущем.

[16], [17], [18], [19], [20], [21], [22], [23], [24], [25]
Вылущивание или энуклеация фиброаденомы молочной железы – наряду с секторальной резекцией – является основным хирургически методом удаления доброкачественных фиброэпителиальных образований молочных желез.
Обязательное условие для проведения энуклеации – небольшой размер новообразования и гистологическое подтверждение его доброкачественности, которое врач получает после цитологического исследования биоптата, взятого с помощью пункционной аспирации фиброаденомы.
Энуклеация фиброаденомы молочной железы чаще всего осуществляется под местным обезболиванием, и общая продолжительность операции не превышает 45-60 минут. Место, где производится рассечение груди, зависит от локализации образования, но чаще всего используется параареолярный доступ, то есть на границе окружающей сосок пигментированной области (в секторе, где находится фиброаденома). Техника энуклеации включает рассечение железы, выведение подвижной опухоли к месту рассечения, отделение близлежащих тканей (не повреждая их острыми инструментами), удаление образования, накладывание швов.
Пациентки после данной операции находятся в условиях клиники не более суток, а шов обычно снимается на пятый день (если нет воспаления). А вот болеть прооперированная грудь может два-три месяца. Читайте также – Удаление фиброаденомы молочной железы

[26], [27], [28], [29], [30], [31], [32], [33], [34], [35], [36]
На сегодняшний день энуклеация миоматозных узлов (миомэктомия) может проводиться несколькими способами в зависимости от их локализации и количества.
При нескольких крупных узлах целесообразнее делать лапаротомию – с рассечением стенки брюшной полости (длина разреза 9-12 см), несколькими рассечениями стенки матки и энуклеацией всех узлов миомы. Восстановление после операции длится до двух месяцев; осложнения после энуклеации с открытым доступом заключаются в кровотечении и образовании спаек, а отдаленные последствия могут быть связаны с большим риском разрыва матки на поздних сроках беременности.
Техника энуклеации при лапароскопически сопровождаемой брюшной миомэктомии (с двусторонней окклюзией маточной артерии для контроля кровопотери) больше всего подходит для пациенток с очень крупными миоматозными узлами, расположенными в мышце стенки матки (интрамурально) или во внутренней слизистой (субсерозно), а также серозно-фиброзными узлами на ножке. Доступ осуществляется через разрез (длиной около 4 см) по линии бикини, а также дополнительный разрез (длиной до 6 мм) ниже пупка.
В ходе визуализируемого лапароскопического вмешательства, при условии, что узел одиночный, небольшой (от 3 до 7 см) и имеет субсерозное или интрамуральное расположение, хирург после общей анестезии делает четыре лазерных надреза по 1,5 см в области брюшной полости. Энуклеация миоматозных узлов (после их подтягивания к месту рассечения) производится диссектором, а вылущенное образование морцеллятором удаляется через разрез. Реабилитационный период после такой операции не превышает десяти дней.
Гистероскопическая энуклеация миоматозных узлов показана, когда они выступают в полость матки, но их размер не превышает 5 см. Данный эндоскопический инструмент не требует разрезов и вводится в матку (под общим наркозом) через влагалище и шейку. Узлы вылущиваются петлей с помощью электрического тока, а затем удаляются из полости матки.
Восстановление пациенток после операции происходит в течение трех-четырех дней, а возможные осложнения после энуклеации с помощью гистероскопа включают кровотечение, образование рубцов и спаек, перфорацию матки.

[37], [38], [39], [40], [41], [42], [43]
Интракапсулярная энуклеация узла щитовидной железы проводится, если в неизмененной паренхиме железы обнаруживается патологическое образование, нарушающее работу органа. Техника энуклеации узла щитовидной железы включает разрез до капсулы железы и выведение ее из ложа в область операционного поля.
На кровеносные сосуды над узлом накладывается зажимы, стенка капсулы надсекается, захватываются и надсекаются тканевые тяжи вокруг узла, узел выдавливается в образовавшееся отверстие и вылущивается с помощью ножниц. Разрез на капсуле ушивают, затем послойно ушивается и наружный разрез.
В отечественно хирургии щитовидной железы интракапсулярная энуклеация считается методом, который в максимальном объеме сохраняет здоровые клетки органа. Западные специалисты считают, что в отношении всех подозрительных узлов щитовидной железы (в том числе кист) лучше всего применять малоинвазивную эндоскопическую гемитиреоидэктомию, то есть полностью удалять ту долю железы, в которой образовался узел. Это связано с большим риском малигнизации новообразований данной локализации.
Энуклеация предстательной железы в случае ее доброкачественной гиперплазии осуществляется путем вылущивания части органа с помощью биполярной вапорезекции специальным петлевым электродом с доступом через уретру или с использованием гольмиевого лазера (HoLEP).
Лазерная энуклеация простаты позволяет с большей точностью убрать всю часть предстательной железы, которая может блокировать выведение мочи. Кроме того, данный метод энуклеации сохраняет удаленную ткань железы для гистологического исследования, необходимого для исключения рака предстательной железы.
Техника энуклеации лазером: с помощью эндоскопа хирург видит, какие ткани нужно удалить, и лазером вылущивает их, оставляя на месте только капсулу; вырезанную ткань перемещают в мочевой пузырь, а затем используется морцелляционное устройство для измельчения и удаления ткани.
Таким же образом, под общим наркозом, проводится лазерная энуклеация аденомы простаты. Операция позволяет полностью удалить все аденоматозные ткани, сводя к минимуму риск повреждения здоровой ткани предстательной железы и необходимость будущего повторного лечения; обеспечивает быстрое облегчение симптомов и восстановление пациентов.
Хотя имеются и осложнения после энуклеации предстательной железы и аденомы простаты, которые могут выражаться в проблемах с мочеиспусканием, гематурией, мочеполовыми инфекциями и импотенцией.

[44], [45], [46], [47], [48], [49], [50], [51], [52], [53], [54], [55]
Злокачественная опухоль печени, симптомы которой на первых стадиях не проявляются, бывает двух типов – первичного и вторичного. Первый тип онкологического заболевания образуется при влиянии клеток органа, вторичный тип появляется из злокачественных клеток, которые из пораженных внутренних органов попадают с кровеносным потоком.
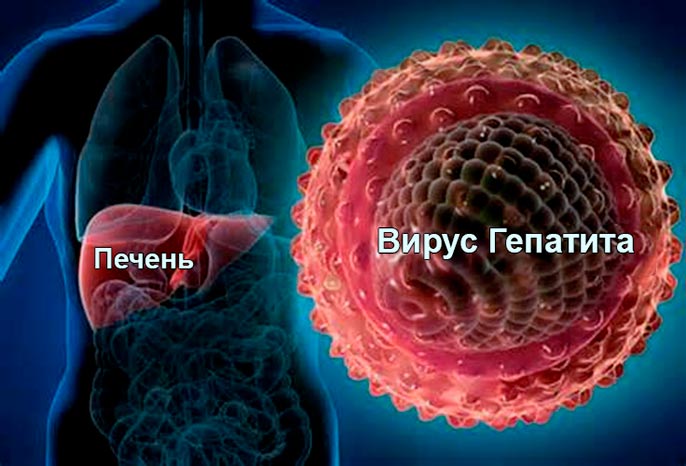
Метастатические новообразования проявляют реакцию чаще в несколько раз.
Влияние оказывает особенность кровоснабжения печени.
Факторы риска
До конца не изучено заболевание опухоль в печени, симптомы, причины и осложнения известны только косвенные.
Окончательно установлена прямая связь между хроническим гепатитом и развитием на его фоне новообразования.
Доказано, что 80% людей, которые болеют гепатитом В более 20 лет, имеют рак печени на разных стадиях.
Поэтому страны Африки и Азии, которые наиболее страдают от вируса, болеют первичной формой онкологического заболевания печени чаще, чем жители Европы и США.
В странах СНГ больший процент заболевания раком печени виден с северных городах.
Причины развития злокачественной опухоли печени
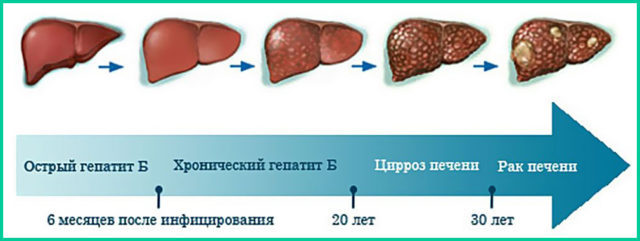
- Гепатит вида В и С. Люди, страдающие хроническим гепатитом (вирусным), процент риска развития онкологического заболевания имеют больший.
- При употреблении алкоголя начинается атрофия клеточной дегенерации, сначала развивается цирроз печени, а затем гепатоцеллюлярная карцинома.
- Описторхоз. Это паразитарное заболевание, возбудителем которого является кошачья двуустка (тип плоских червей). Начинает свое действие в желчных протоках печени, в следствии чего в органе начинается воспаление, дисплазия эпителия, а отток желчи нарушен.
- Попадание в организм грибка вида Aspergellus flavus, он продуцирует афлотоксин В.
- Экологические предпосылки.
Как возникает опухоль в печени
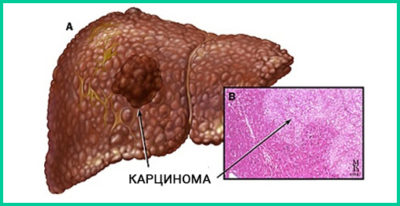
Нормальное обновление клеток печени нарушается из-за влияния неблагоприятных факторов, клетки делятся более стремительно, зрелого состояния не достигают.
Также опухоль печени под действием вируса гепатита может развиваться как мутирующий ген.
Новообразование, развивающееся из клеток печеночной паренхимы, диагностируют как гепатоцеллюлярную карциному.
Если из эпителия желчных протоков – холангиокарциному.
Новообразованию может придаться вид одного или больше узлов, которые способны поразить орган полностью. Это диффузная форма рака.
Вторичное онкологическое поражение — это метастазы, переходящие в печень опухолей, которые в других органах развились.
Достаточно часто пораженные новообразованием клетки мигрируют из кишечника в печень (особенность кровотока с этим связана), из легких переходят реже.
Классификация опухолей печени
Существует много видов опухолевого поражения, вот самые известные из них:
- Опухоль печени эпителиальная.
- Печеночно-клеточный (гепатоцеллюлярный) рак.
- Заболевание эмбрионального происхождения.
- Поражение желчных внутрипеченочных протоков.
- Смешанный гепатохолангиоцеллюлярный рак.
- Опухоль недифференцированная.
- Цистаденокарцинома протоков.
- Опухоль печени Мезенхимальная.
В эту группу онкологических заболеваний, поражающих печень, относятся те, опухоли которых развиваются из кровеносных сосудов:
- Гемангиоэндотелиома неопластическая.
- Опухоль, развивающаяся из перителия сосудов и эндотелия.
- Гемангиоэндотелиома эпителиоидная.
- Новообразование, которое образуется из соединительной ткани.
- Фиброзная гистиосаркома (злокачественная).
- Новообразования неопределённого генеза (мезенхимальные).
- Опухоль, исходящая из гладких мышц.
- Неходжкинская злокачественная лимфома (новообразование из лимфоидной ткани).
- Злокачественная опухоль, которая образуется из гоноцитов.
- Плоскоклеточный рак (опухоль из плоского эпителия).
- Новообразование, развивающееся из клеток мезотелия.
- Поражения с гистиоструктурой неуточнённой.
- Рак печени холангиоцеллюлярный со смешанными эпителиальными опухолями.
Симптомы опухоли печени

Первая стадия заболевания проходит практически незаметно, а течение развития опухоли достаточно быстрое, это стало причиной того, что почти всегда заболевание диагностируют на дальних стадиях.
Как показывает практика, жалобы в медицинские учреждения поступают спустя несколько месяцев, после того, как проявятся первые симптомы опухоли печени.
В основном пациенты жалуются на следующие недомогания:
- В правом подреберье ноющие боли.
- Уменьшается масса тела из-за отсутствия аппетита.
- Ухудшается общее самочувствие, тошнота, вялость, быстрая утомляемость.
- Беспокоит вздутие в животе.
- Температура тела повышается.
- Кровотечение из носа.
- Кожные покровы приобретают желтоватый оттенок.
- Диарея.
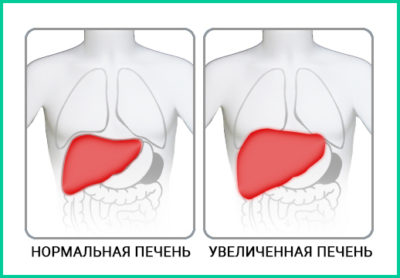
Первичные симптомы в 90% случаев – появление гепатомегалии (размеры печени увеличиваются).
Нижняя грань органа увеличена на 10 см, нижняя грань растет до четвёртого ребра, грудная клетка при этом также увеличивается.
Примерно половина заболевших этим опухолевым недугом отмечают асцит (в брюшной полости скапливается много жидкости).
Имеет соответствие портально- гитертензийному синдрому, присутствует гемморагический характер, при этом асцитическая жидкость опухолевых клеток не содержит.
При наличии одного или нескольких признаков поражения формируется симптоматика первичной формы.
- Абсцесс печени напоминает форма.
- Гипогликемическая предпосылка.
- Наличие признаков желтухи.
- Гепатомегалическая форма.
- Форма цирротическая.
- Форма карциноматозная диффузная.
Признаки опухоли печени

Отток желчи в кишечник из печени блокируется на стадиях, когда опухоль достигает больших размеров.
Диагностируется механическая желтуха, которая является признаком поздних стадий онкологического заболевания, патология проявляется по причине того, что из внутрипеченочных протоков желчь попадает непосредственно в кровь.
При механической желтухе наблюдается пожелтение кожи, изменение слизистых и склер, раздражение и зуд кожных покровов, моча потемневшая, а стул наоборот, посветлевший.
Данный симптом неспецифичен, его можно обнаружить при любых стадиях затруднения желчного оттока. Не ощущается сильных болей, поэтому диагностировать сложнее.
Поздние сроки развития злокачественной опухоли в печени приводит к кровотечению из приближенных органов, развитию анемии, скоплению в брюшной полости жидкости, организм отравляется продуктами распада кислот желчи.
Диагностика опухоли печени
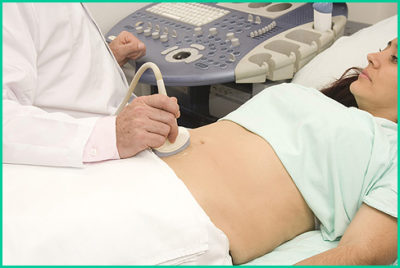
При своевременном обращении к специалисту можно определить уровень увеличения размеров органа, уплотнение печени, а также неоднородность поверхности.
Когда орган начинают осматривать и прощупывать, чувствуется небольшой дискомфорт.
При визуальном осмотре обнаруживается желтушное окрашивание кожных покровов и склер, но это на более поздних стадиях можно определить.
Диагностировать очаг поражения и интенсивность можно стандартизированным способом – анализируется строение клеток, а затем проводится исследование кусочка опухолевой ткани под микроскопом.
Но это возможно не всегда при изменении формы печени, проводится УЗИ брюшной полости для определения интенсивности роста новообразования.
В диагностировании заболевания печени первыми применяются высокотехнологичные инструментальные исследования.
Хирургическое лечение опухоли печени
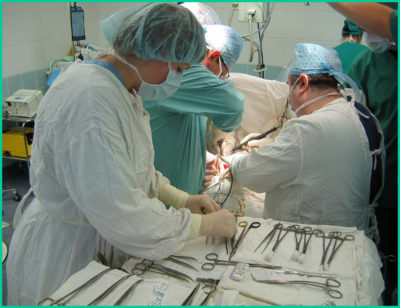
Нижняя грань органа увеличена на 10 см проводится в специализированном учреждении (онкологии).
Радикальным и наиболее действенным способом устранения опухоли является хирургическое вмешательство. Оно сочетает в себе резекцию печени, а также её трансплантацию.
Резектабельность при диагнозе опухоль печени может достигать 66%.
Летальный исход после операции в процессе проведения резекции печени по данным достигает 15%.
Повышается процент в зависимости от осложнения, при циррозе печени летальный исход имеет больший шанс.
На сегодняшний день известны несколько для проведения на печени операции.
Широко применяются три способа: Рио-Бранка, Кохера и Федорова.
При проведении обширного оперативного вмешательства, назначаются использование торакоабдоминального доступа.
Химиотерапевтическое лечение опухоли печени
При опухоли печени данный вид лечения не всегда приносит желаемый эффект.
Нерезектабельный процесс имеет годовой порог, который не превышает семи месяцев.
Внутриартериальная химиоэмболизация помогает достичь положительных результатов, но в некоторых случаях.
Процесс проведения этого метода включает в себя введения в почечную артерию химиотерапевтического препарата.
Только предварительно препарат следует развести в липоиде или смешать пропорционально с микроэмболами.
Двухгодовой порог жизни после применения химиоэмболизации составляет около 27%.
Лучевая терапия и криотерапия
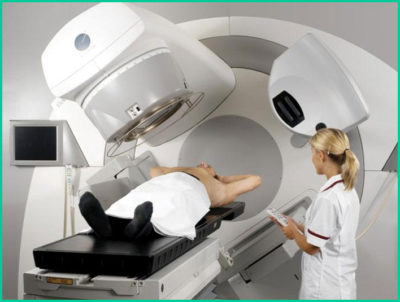
При диагнозе опухоль печени лучевое лечение не проводится. На сегодняшний день проводятся исследования, но, на сколько известно, этот метод в данном случае не имеет эффективности.
Криохирургия проводится посредством интраоперационного охлаждения жидким азотом новообразования, холод подается при помощи специального хирургического зонда.
Но при размерах новообразования более 5 см криохирургия не применяется, так как нет эффективности.
После проведения данного вида лечения трехлетняя выживаемость составляет примерно 20%.
Алкоголизация и радиочастотная абляция
Метод алкоголизации опухолевых узлов получает большую популярность в применении.
Основой лечения является введение спиртосодержащего раствора в новообразование. Применяется небольшая игла.
Процедуру следует проводить только под УЗИ контролем. Пятилетний уровень выживаемости в этом случае составляет 30-40%.
Абляцией является не удаление новообразования, а только местное его разрушение.
Для радиочастотной абляции применяются высокоэнергетические радиоволны. Проводится лечение под контролем УЗИ или КТ.
Intoxic — антигельминтное средство, которое безопасно выводит паразитов из организма.
Intoxic лучше антибиотиков, потому что:
1. В короткий срок убивает паразитов и мягко выводит их из организма.
2. Не вызывает побочных эффектов, восстанавливает органы и надежно защищает организм.
3. Имеет ряд врачебных рекомендаций, как безопасное средство.
4. Имеет полностью натуральный состав.
В опухоль через кожу вводится игловидный датчик, в новообразование поступает высокочастотный ток.
Раковые клетки таким образом нагреваются, что приводит к их разрушению.
Но подобный метод лечения применяется в случае, если размер новообразования не превышает 5 см, а самих опухолей не должно быть более четырех.
Профилактика опухоли печени
Применяется ряд профилактических мероприятий для предупреждения развития раковых клеток:
- Мероприятия, отнесенные к снижению заражения и лечению гепатитов типа В и С. Население повышенного риска проводит вакцинацию, проводятся исследования донорской крови и т.д.
- Термическая некоторой продукции препятствует возникновению инвазии (описторхозной).
- Профилактика табакокурения и алкоголизма.
- Продукция , привезенная из стран Южной Африки Юго-Восточной и Азии проверяется на наличие грибка типа Aspergellus flavus, он может быть причиной возникновения афлотоксинов.
Ранние стадии онкологического заболевания быстрее вылечиваются и не приводят к осложнениям.
Поэтому важно своевременно проходить медицинский осмотр при малейшем подозрении на опухоль печени.
Читайте также:

