Эндобронхиальный рак на кт
Эндобронхиальный рак относительно рано, даже при совсем небольших размерах опухоли, приводит к сужению просвета соответствующего бронха. Поэтому его основными проявлениями оказываются признаки нарушения бронхиальной проходимости. До появления этих признаков выявление опухоли в просвете бронха при обычном рентгенологическом исследовании практически невозможно.
Эндобронхиальные опухоли отчетливо видны на аксиальных срезах в случаях, если они занимают значительную часть просвета бронха, но не обтурируют его полностью. Такие образования имеют форму полипа, широким основанием прилежащего к одной из стенок крупного бронха. Контуры опухоли гладкие и четкие, структура обычно однородная, плотность мягко-тканная. Отличительной особенностью эндо-бронхиальных гамартом в сравнении с бронхогенным раком являются включения кальция и жира, отчетливо видимые на аксиальных срезах. Кроме того, Эндобронхиальный компонент опухоли часто наблюдается при карциноидных образованиях. Они относятся к нейроэндокринным злокачественным эпителиальным новообразованиям. При КТ-ангиографии такие образования быстро и интенсивно накапливают контрастное вещество, что позволяет предположить наличие карциноид-ной опухоли.
Наиболее демонстративно эндобронхиальные опухоли видны при многоплоскостной реформации. Особенно важны такие изображения при локализации опухоли в бронхах, расположенных перпендикулярно или под углом к плоскости сканирования. Плоские новообразования небольшого размера, едва выступающие над поверхностью слизистой, крайне трудны для распознавания при стандартном КТ исследовании. Обычно они выявляются только после предварительного бронхологического исследования.
Эндобронхиальные опухоли могут иметь и доброкачественную природу. В большинстве своем они представлены аденомами и папилломами Реже встречаются хондромы, фибромы и некоторые другие неэпителиальные образования. Клиническое течение и методы лечения таких новообразований имеют некоторые особенности. Установить гистологическую природу эндобронхиалыюй опухоли можно только по результатам морфологического исследования. Ровные гладкие контуры эндобронхиального образования не являются свидетельством доброкачественной их природы.

Рис. Эндобронхиальный рак промежуточного бронха. На аксиальном срезе (а) и многоплоскостных реформациях(б, в) патологическое образование диаметром 1, Осм прилежитквнутренней стенке промежуточного бронха, имеет четкие ровные контуры. Просвет бронха частично сохранен. Воздушность легоч-нойткани не изменена.

Рис. Эндобронхиальный рак верхушечного сегментарного бронха левого легкого. На аксиальном срезе (а) выявляется незначительноеутолщениестеноксегментарногобронха. На реформации в сагиттальной плоскости(б) выявляется патологическоеобразованиенеправильнойформы, исходящее иззаднейстен-ки верхушечного сегментарного бронха и свисающее в просвет бронха Б1 -2.
В тех случаях, когда эндобронхиальные опухоли занимают весь просвет бронха, их изображение теряется на фоне мягкотканных структур и сосудов корня легкого. Дистальная часть опухоли сливается с ателектазированной долей легкого. Проксимальная часть граничит с воздухом в просвете бронха и имеет типичную выпуклую, полуокруглую форму. При болюсном усилении плотность опухолевой ткани повышается, но обычно это не позволяет отличить ее от безвоздушной легочной ткани. Гораздо большее значение КТ-ангиография имеет для выявления возможного перибронхиального компонента опухоли и разграничения его с сосудами корня легкого.

Рис. Эндобронхиальная опухоль бронха верхней доли правого легкого. Культя бронха (а) имеет типичную прямоугольную форму за счет обтурации его просвета патологическим образованием. Дисталь-нее (б) опухоль сливается с ателектазированной легочной тканью и увеличенными лимфатическими узлами бронхопульмональной группы.

Рис. Эндобрнохиальная опухоль, верхней доли правого легкого. Сегментарный бронх (*) полностью обтурирован патологическим образованием округлой формы.
Конспект врача рентгенолога в схемах и таблицах.
Рентгеносемиотика центрального эндобронхиального рака.
Центральный рак лёгкого.
Касаясь клинической симптоматологии рака лёгкого необходимо помнить высказывание Р.Г. Оверхолта по поводу широко известной триады:
- чем меньше клинических симптомов, тем больше вероятность наличия рака при нахождении изменений на рентгенограммах;
- вероятность излечения обратно пропорциональна количеству симптомов;
Клиническая симптоматология рака лёгкого отражена в нижеприведенной таблице.
Относится к первым признакам заболевания. Может быть сухим, приступообразным. Надсадный кашель встречается редко, и связан с присоединением инфекции. При увеличении обтурации кашель сопровождается выделением слизистой или слизисто-гнойной мокроты.
Как правило, при раке на ранней стадии – это прожилки крови. Так как кровохарканье связано также с распадом опухолевого узла и прорастанием стенок сосудистых элементов, по мере роста опухоли частота этого симптома увеличивается.
Является постоянным симптомом прогрессирующего процесса. Литературные данные свидетельствуют, что на степень одышки, влияют локализация опухоли, рефлекторные механизмы. Также одышка зависит от степени компрессии крупных сосудов и сосудов средостения опухолевым процессом, от наличия и количества плеврального выпота.
Является проявлением общей интоксикации организма, всасыванием продуктов метаболизма опухоли (А.И. Савицкий)
Повышение температуры тела
Также является проявлением интоксикации организма.
Чаще всего, в повседневной практике, при проведении рентгенологического исследования, регистрируются не скиалогические признаки самой опухоли, а вторичные изменения, вызванные ей, явлениями парапроцесса.
С учётом роста опухоли выделяют:
- смешанный – экзо - эндобронхиальный рак.
Общая теневая картина центрального эндобронхиального рака
обуславливается отображением следующего морфологического субстрата:
- последствиями нарушения проходимости бронха;
- осложнениями, связанными с ростом опухоли, присоединением парапроцесса, метастазированием.
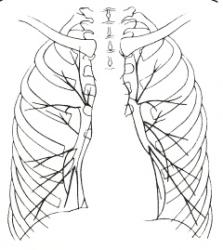
2 фаза развития рака , ведущим синдромом которой является гиповентиляция, в результате нарушения бронхиальной проходимости проявляется определенной теневой картиной.
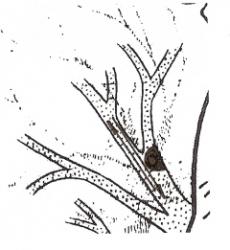
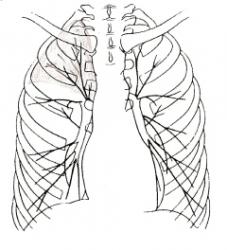
1 степень сужения бронха – гиповентиляция характеризуется следующим:
- уменьшение прозрачности структурной единицы лёгкого (доли, сегмента) – иллюстрация 2, 3, 4;
- незначительное уменьшение объёма с намечающимися вогнутыми границами;
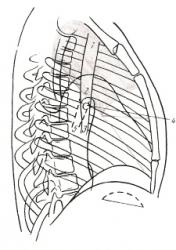
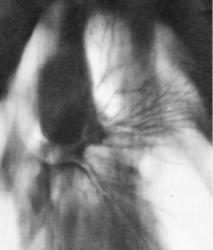
3 фаза развития рака. Просвет бронха в фазе выдоха обтурирован.
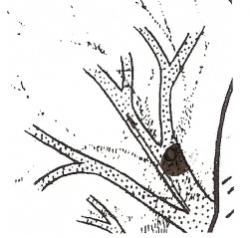
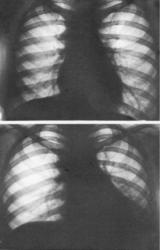
2 степень сужения бронха - клапанная эмфизема (иллюстрация 6) обуславливает следующую теневую картину:
- увеличение прозрачности легочного фона структурной единицы лёгкого (доли, сегмента);
- увеличение объёма структурной единицы лёгкого;

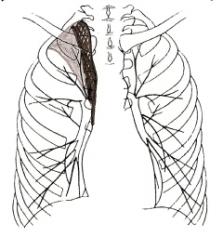
4 фаза развития рака. Просвет бронха обтурирован полностью – иллюстрация 8.
3 степень сужения (полная) бронха – ателектаз характеризуется типичной картиной:
- тень ателектазированной структурной части лёгкого приближается к треугольной форме – иллюстрации 9, 10;
- уменьшение объёма структурной единицы лёгкого;
- смещение и деформация междолевых щелей;
- смещение сосудистых стволов.
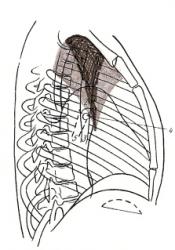

5 фаза развития рака. Просвет бронха обтурирован полностью – 3 степень сужения. Ведущим скиалогическим признаком является ателектаз и осложнения.
Ателектаз с распадом и пневмонией, метастазы в регионарных лимфатических узлах, плеврит:
- неоднородное затемнение треугольной формы;
- жидкость в плевральной полости.

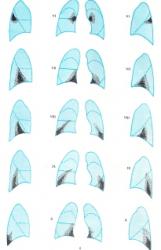
Ниже приведены схемы спадения долей и сегментов (по Anacker H ., 1963) – иллюстрации 11, 12, 13.
Для своевременной диагностики, как долевых, так и сегментарных ателектазов необходимо уделять внимание следующему:
- положение и наличие деформации междолевых и межсегментарных щелей;
- степень спадения отдельных структурных единиц лёгкого;
- закономерности их перемещения при спадении;
- состояние окружающих тканей лёгкого;
- возможности перемещения диафрагмы, средостения и здорового лёгкого – иллюстрация 14.
| Вложение | Размер |
|---|---|
| 1. | 36.26 КБ |
| 2. | 32.75 КБ |
| 3. | 36.08 КБ |
| 4. | 45.39 КБ |
| 5. | 24.49 КБ |
| 6. | 33.44 КБ |
| 7. | 29.48 КБ |
| 8. | 39.3 КБ |
| 9. | 36.17 КБ |
| 10. | 44.44 КБ |
| 11. | 32.58 КБ |
| 12. | 39.25 КБ |
| 13. | 39.92 КБ |
| 14. | 39.92 КБ |
![]()
У меня два коммента.
В наше время основная классификация по которой и определяется метод и тактика лечения (а зачем-же тогда вообще нужны классификации?) рака легких (ВОЗ) это мелкоклеточный рак легких и не-мелкоклеточный рак легких (Small Cell Lung Cancer CCLL & Non-Small Cell Lung Cancer NCCLL). Для постановки стадии рака (TNM staging) необходимо КТ исследование; на основании одного рентгена правильно поставить стадию невозможно!
Классический рентген как метод диагностики при раке легких я вижу в на этапе первичного выявления и при контроле лечения (химиотерапии например); хотя и с оговорками; ибо КТ все равно яляется предпочтительнее для динамического контроля; другой вопрос что нельзя его часто использовать из-за высокой лучевой нагрузки.
Если немного отвлечься; коли уже на рентгенораммах выявляются такие классические признаки которые так хорошо описал доктор Катенев; то как правило такой рак уже находистя на продвинутой стадии развития; и говорить о положительном исходе приходится не так часто. В Европе и США главный упор сделан на выявление мелких узелков (pulmonary nodules) на рентгенораммах; даже придумано отдельный термин для такой находки: одиночный узел в легком (SPN, solitary pulmonary nodule) и разработан алгоритм что делать дальше на основании КТ исследования такого узелка. Подробнее данная тема хорошо раскрыта в журнале Европейская Радиология за февраль 2007 года.
- ВойтиЗарегистрироваться
![]()
Спасибо Вам за комментарий.
Уважаемый доктор Марио! запись в блоге называется "Конспект врача-рентгенолога", т.е. то, что "дают" традиционно курсантам, как на первичке, так и на курсах повышения квалификации по рентгенологии.
И второе, что никогда не надо забывать НИКОМУ. Основная часть наших граждан проживает в сельской местности, лечится и обследуется в лучшем случае в ЦРБ, где нет ни КТ, ни СКТ, ни МРТ. Там есть в лучем случае, я подчеркиваю В ЛУЧШЕМ СЛУЧАЕ цифровой флюорограф, рентгеновский аппарат хорошо если с УРИ И ВСЕ.
ВОТ ИСХОДЯ ИЗ ЭТОГО и надо реформировать наше здравоохранение, чтобы гражданин Российской Федерации получал "стандартную" лечебно-диагностическую помощь независимо от места проживания село - город - мегаполис. В настоящее время мы наблюдаем несколько другую ситуацию.
2. В первичном звене - ЛПУ уровня ЦРБ, как правило, морально устаревшая и технически изношенная аппаратура, правда в нашей Белгородской области довольно интенсивно заменяется, но - это в Белгородской области, где этот вопрос находится под контролем нашего Губернатора. Нехватка врачей лучевых диагностов в ЦРБ. Я знаю районы, где вообще нет врача-рентгенолога, в большинстве районов - один врач-рентгенолог, который не может смотреть на норматив - нагрузка не "выше крыши", а выше неба. Редко где в районах - 2 - 3 рентгенолога, при наличии должностей в два раза больше, которые пустуют. Не хотят молодые и перспективные врачи ехать в район, хотят минимум - в областной центр. А ПЕРВИЧНАЯ, СВОЕВРЕМЕННАЯ ДИАГНОСТИКА ИМЕННО ДОЛЖНА БЫТЬ НА УРОВНЕ ЦРБ.
Кстати, доктор Марио на данном сайте размещено много материала из практики, и именно случаев диагностики "малых раков", именно методом классической рентгенодиагностики.
Вот такие дела. Спасибо Вам за комментарий и за активное участие в обсуждении. С уважением В. Катенёв.
а) Терминология:
1. Синонимы:
• Липома, лейомиома, нейрогенные опухоли, гемангиома, хондрома
2. Определение:
• Редкие опухоли трахеи и бронхов, характеризующиеся отсутствием специфических лучевых признаков
б) Лучевые признаки редких новообразований дыхательных путей:
1. Основные особенности:
• Оптимальный диагностический ориентир:
о Патологические образования дыхательных путей, характеризующиеся отсутствием специфических лучевых признаков, за исключением липомы
о Обычно диагноз ставят после выполнения резекции или биопсии
• Локализация:
о Вариабельна в зависимости от типа образования
• Размер:
о 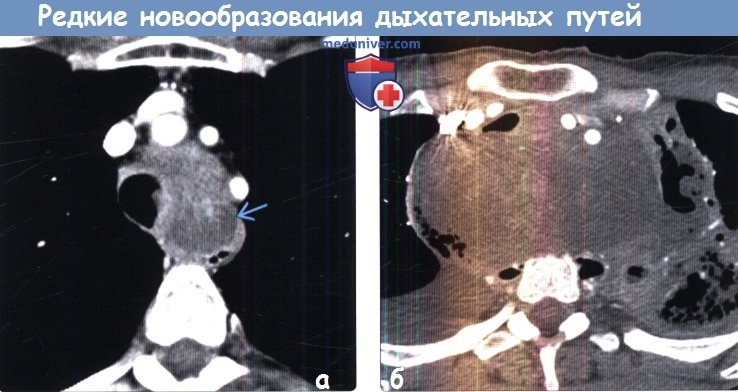
(а) При КТ с контрастным усилением в трахее определяется крупное объемное образование с очагами некроза , расположенное преимущественно вне просвета трахеи. При биопсии была выявлена плеоморфная аденома.
(б) У этого же пациента при КТ с контрастным усилением визуализируется выраженное увеличение размеров плеоморфной аденомы, которая инвазирует и сдавливает крупные сосуды, пищевод и тело прилежащего грудного позвонка. Агрессивный характер роста соответствует злокачественной форме данной опухоли.
• Липома:
о Обычно поражает проксимальные бронхи; в трахее встречается реже
о Растет из жировой ткани, расположенной в подслизистом слое трахеи и бронхов
о Состоит полностью из жировой ткани, что является почти пато-гномоничным признаком
о Часто растет на тонкой ножке
о Эндобронхиальная гамартома также может содержать жировую ткань
• Нейрогенная опухоль (шваннома или нейрофиброма):
о 25% от всех нейрогенных опухолей органов дыхательной системы локализуются в бронхах о форма шаровидная, овоидная, дольчатая, контур четкий
о Гомогенная структура и характер контрастирования
о Может возникать злокачественная дегенерация; SUV >пула крови средостения
о Нейрофиброма встречается чаще, чем шваннома
• Гемангиома:
о Наиболее частая опухоль подголосового отдела гортани у детей о Объемное образование в задней или заднебоковой стенке подголосового отдела гортани
о Часто сопровождается развитием гемангиом на лице
• Хондрома:
о Узелок с четким контуром, содержащий кальцификаты о Выглядит схоже с гамартомой
• Фиброэпителиальный, или воспалительный, полип:
о Крупные отделы дыхательных путей
о Развивается в ответ на раздражение или воспаление, например, при попадании инородных тел или вдыхании едких газов
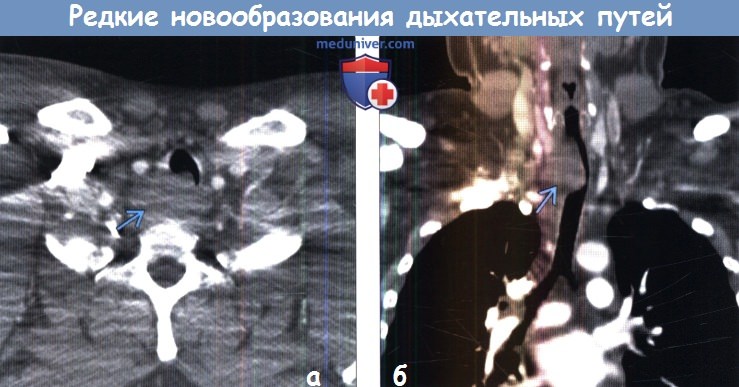
(а) При КТ с контрастным усилением в трахее определяется крупное объемное образование, сдавливающее справа и сзади мембранозную стенку трахеи. Образование расположено преимущественно вне просвета трахеи. При бронхоскопической биопсии был выявлен внелегочный мелкоклеточный рак.
(б) У этого же пациента при КТ с контрастным усилением на реконструкции в коронарной плоскости в трахее лучше визуализируется овоидное объемное образование, гомогенно накапливающее контрастное вещество. Внелегочный мелкоклеточный рак встречается редко — только в 2-4% случаев.
• Плеоморфная аденома:
о Редкое новообразование крупных отделов дыхательных путей, схожее гистологически с опухолями слюнных желез
о Вариабельные лучевые признаки в зависимости от степени агрессивности роста образования
- Для медленно растущих опухолей характерны четкий контур и полиповидная форма
- Для злокачественных опухолей характерны инфильтративный рост и распространение за пределы дыхательных путей; могут достигать больших размеров
• Прочие:
о Аденома слизистых желез, фиброма, онкоцитома, зернисто-клеточная опухоль, аневризмальная костная киста, гломусная опухоль, мелкоклеточный рак
4. МРТ:
• Доброкачественные новообразования трахеи и бронхов характеризуются отсутствием специфических лучевых признаков:
о Узелок эндобронхиальной или эндотрахеальной локализации, не распространяющийся за пределы дыхательных путей
• Исключением является эндобронхиальная липома; во всех импульсных режимах характеризуется интенсивностью сигнала, характерной для жировой ткани
5. Рекомендации к проведению лучевых исследований:
• Оптимальный метод лучевой диагностики:
о МСКТ является методом выбора для диагностики патологических изменений дыхательных путей
о Виртуальная бронхоскопия позволяет планировать хирургическое вмешательство
• Рекомендации по выбору протокола:
о МСКТ с контрастным усилением, мультипланарная реконструкция изображений:
- Реконструкция изображений, параллельных коронарной и сагиттальной плоскостям трахеи:
Позволяет определить, возможно ли выполнить резекцию
о В случае злокачественных новообразований трахеи и бронхов ПЭТ/КТ облегчает выявление метастазов, что позволяет избежать напрасного выполнения резекции
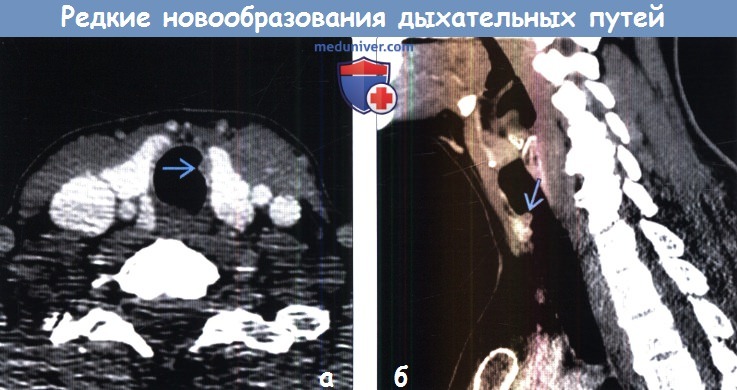
(а) При КТ с контрастным усилением в трахее определяется небольшой узелок. При резекции была выявлена хондрома.
(б) У этого же пациента при КТ с контрастным усилением на реконструкции в сагиттальной плоскости видно, что узелок происходит из передней стенки трахеи. Данная лучевая картина не является специфической, вследствие чего для постановки диагноза обычно необходимо выполнять бронхоскопическую биопсию.
в) Дифференциальная диагностика редких новообразований дыхательных путей:
1. Плоскоклеточный рак:
• Наиболее частое первичное злокачественное новообразование дыхательных путей
• Обычно встречается у курильщиков
• Трахея > проксимальные бронхи
• Контур нечеткий, распространяется за пределы дыхательных путей
• В 33% случаев на момент выявления имеются метастазы в легких или средостении
2. Аденоидно-кистозная карцинома:
• Вторая по частоте первичная опухоль трахеи
• Обычно локализуется вблизи бифуркации трахеи и может распространяться на главные бронхи
• Узелок в подслизистом слое или циркулярное утолщение стенок
• Часто распространяется продольно вдоль дыхательных путей
• ± опухолевый компонент за пределами дыхательных путей
3. Карциноид бронха:
• Часто поражает лиц молодого возраста
• Чаще встречается в долевых бронхах
• Узелок шаровидной или овоидной формы с дольчатым контуром
• В 25-30% случаев содержит кальцификаты
• ± интенсивное накопление контрастного вещества
4. Гамартома:
• ± кальцификация в виде попкорна или макроскопические жировые включения
5. Метастаз:
• Выявленная ранее первичная злокачественная опухоль любой локализации
• Солитарный метастаз в дыхательных путях встречается значительно чаще, чем множественные метастазы
• Гематогенные метастазы меланомы, злокачественных опухолей молочной железы, толстой кишки или почечно-клеточной карциномы
• Прямая инвазия при лимфоме, бронхогенной карциноме, карциномах щитовидной железы и пищевода
6. Мукоэпидермоидная карцинома:
• Эндобронхиальное образование с четким контуром
• Часто расположено по длинной оси дыхательных путей
• Чаще всего встречается в долевых и сегментарных бронхах
• 50% пациентов моложе 30 лет
7. Папиллома:
• Эндобронхиальное объемное образование с четким ровным или дольчатым контуром
•
Редактор: Искандер Милевски. Дата публикации: 2.2.2019
В связи с низкой толерантностью критических органов грудной полости при наружном облучении суммарная очаговая доза (СОД), как правило, не превышают 60 Гр, что при высокодифференцированном и умеренно дифференцированном плоскоклеточном и аденогенном раке не обеспечивает стойкого локального контроля и в большинстве случаев позволяет достичь лишь паллиативного эффекта.
Вместе с тем при осложненном течении местно-распространенного рака асфиксия и(или) пневмонит, обусловленные выраженным стенозом трахеи и крупных бронхов, в ряде случаев препятствуют реализации дистанционной лучевой терапии (ДЛТ).
Сложен выбор лечебной тактики при небольших по распространенности первично-множественных синхронных и метахронных опухолях бронхов и трахеи, а также при рецидивах.
Это объясняется многообразием клинических ситуаций: состоянием после пневмонэктомии и наличием опухоли в бронхах единственного легкого; несколькими зонами поражения в бронхах, что влечет за собой необходимость облучения значительных объемов легочной ткани; рецидивом в культе бронха после комбинированного лечения с облучением в СОД 30-40 Гр и др.
Необходим дифференцированный подход к планированию и проведению лучевой терапии у больных, которым выполнена паллиативная операция и у которых выявлена опухоль полиции резекции бронха. В тех случаях, когда отсутствуют внутригрудные метастазы, на всю локорегионарную зону достаточно подвести дозу 40-46 Гр, а на культю бронха — до 70 Гр, что при ДЛТ может привести к развитию лучевых повреждений.
Таким образом, в описанных и ряде других ситуаций невозможно обеспечить стойкий локальный эффект с минимальным повреждением нормальных тканей путем проведения дистанционного облучения.
Эндобронхиальная лучевая терапия
В связи с этим особый интерес представляет метод сочетанного лучевого воздействия, включающий наружное дистанционное облучение и эндобронхиальную лучевую терапию (ЭБЛТ). Благодаря ЭБЛТ можно значительно увеличить подводимую непосредственно к опухоли дозу ионизирующего облучения без повреждения окружающих нормальных тканей.
Внутриполостная лучевая терапия — направление в лучевой терапии, очередной этап развития которого базируется на применении современной радиотерапевтической техники последнего поколения.
Радиоактивный источник жестко фиксирован к тросу, с помощью которого возможно его поступательное перемещение с заданным шагом и временем в каждой позиции. Автоматическое выполнение заданной программы облучения обеспечивает компьютеризированный блок управления.
За прошедшие полтора десятилетия накоплен значительный мировой опыт применения ЭБЛТ при раке бронхов. В последние годы возможности ЭБЛТ значительно расширились благодаря применению эндоскопической и лазерной техники. При выраженном стенозе бронхов и трахеи лазерная деструкция или электродеструкция экзофитной части опухоли, выполненная на первом этапе лечения, обеспечивает восстановление просвета трахеи и бронхов, улучшает вентиляцию дистально расположенной легочной ткани, создавая тем самым условия для эндобронхиальной лучевой терапии и дистанционной лучевой терапии.
Эндобронхиальное облучение относится к категории высоких технологий лучевой терапии. ЭБЛТ может быть применена как самостоятельный вариант лучевого лечения, но чаще ее проводят в сочетании с дистанционным наружным облучением.
Распространенность процесса является определяющим фактором при выборе варианта лечения.
Внутриполостную лучевую терапию как в качестве самостоятельного варианта, так и в сочетании с наружным дистанционным облучением осуществляют по радикальной программе или с паллиативной целью. На первых этапах изучения метода ЭБЛТ использовали преимущественно с паллиативной целью для купирования тягостных симптомов болезни (Albert W. et al., 1986; Hilaris В.S.,1986).
У 2/3 пациентов удалось достичь стойкого паллиативного эффекта только благодаря проведению ЭБЛТ, дополнительные паллиативные противоопухолевые воздействия не потребовались до конца жизни пациентов. При этом лечение не сопровождалось тяжелыми реакциями и осложнениями.
Р.Н. Kohek (1990) проводил сочетанную лучевую терапию и только ЭБЛТ у 79 больных с местно-распространенным раком легкого, в основном при поражении крупных бронхов.
После эндобронхиальной лучевой терапии (независимо от сочетания с дистанционным компонентом) улучшение бронхиальной проводимости отмечено у 87% больных, осложнения констатированы у 7% больных.
В последние годы идеология эндобронхиальной лучевой терапии существенно изменилась — от паллиативного облучения перешли к радикальному воздействию, которое включает многократные сеансы ЭБЛТ и дистанционное облучение с использованием нетрадиционных вариантов фракционирования дозы в сочетании с лазерной реканализацией и без таковой. Радикальное лучевое лечение с ЭБЛТ предусматривает получение стойкого и длительного эффекта.
Последняя особенно необходима при опухолевом поражении межсегментарных шпор базальных бронхов. Так, например, облучение IX сегментарного бронха при его обтурации осуществляют путем последовательного введения эндобронхостата в VIII и X сегментарные бронхи.
В зависимости от общего плана лечения величина разовой очаговой дозы при эндобронхиальной лучевой терапии составляет 5-10 Гр. Режимы облучения: по 5 Гр через день 3 раза в неделю до суммарной очаговой дозы 25-30 Гр; по 7-10 Гр 1 раз в неделю до СОД 28-40 Гр.
В зависимости от клинической ситуации дистанционное облучение проводят в различных режимах фракционирования до суммарной очаговой дозы 40-60 Гр. Интервал между компонентами сочетанного лучевого лечения составляет в среднем 10-20 дней.
На различных этапах лечения для удаления экзофитной части опухоли, расширения просвета трахеи и бронхов используют лазерную и(или) электродеструкцию. Все необходимые подготовительные, в том числе эндоскопические, манипуляции и сеанс лучевой терапии проводят под местной анестезией, что имеет большое практическое значение.
Подготовка к внутриполостному облучению включает проведение предлучевой тонометрии и дозиметрического расчета.
После общеклинического обследования с установлением локализации и степени распространеннения опухолевого процесса для предлучевой топометрии дополнительно необходимо выполнить: разметочную трахеобронхоскопию, при которой оценивают возможность установки эндобронхостата определенного типа и диаметра, протяженность экзофитного компонента и расстояние от его дистального и проксимального края до резцов; компьютерную томографию для уточнения степени перибронхиального распространения опухолевого процесса и толтины экзофитного компонента на всем протяжения опухоли, а также для реконструкции углов бронхов, что является необходимой информацией для проведения дозиметрического расчета.
Методика проведения эндобронхиальной лучевой терапии включает: установку эндобронхостата в пораженном бронхе и(или) бронхах, трахее пол контролем бронхоскопа; фиксацию эндобронхостата; контроль за положением эндостата с имитатором источника излучения в двух проекциях с помощью электрорентгенограммы (рис. 7.8) и при бронхоскопии; ввод дозиметрического плана в компьютер ралиотерапевтического аппарата; проведение сеанса ЭБЛТ; извлечение эндобронхостата; контроль за состоянием больного в течение суток.

Рис. 7.8. Рентгенологический контроль положения эндостатов с имитаторами позиций облучения больного с опухолевым поражением бифуркационных лимфатических узлов
а — прямая проекция; б — боковая проекция.
Противопоказания к эндобронхиальной лучевой терапии: заболевания сердечно-сосудистой системы и сахарный диабет в стадии декомпенсации; выраженная легочная недостаточность вследствие хронических заболеваний легких; активная форма туберкулеза легких; прорастание опухоли в соседние органы.
Больные, как правило, переносят ЭБЛТ вполне удовлетворительно. Местные лучевые реакции проявляются в виде очаговых или сливных эпителиитов слизистой оболочки трахеи и бронхов в конце курса облучения.
Лучевые реакции не препятствуют проведению лечения и купируются в течение 10-14 дней. Однако в мировой практике наблюдались случаи возникновения стеноза, кровотечения с летальным исходом, образования свищей, развития медиастинита (табл. 7.2, 7.3).
Таблица 7.2. Частота кровохарканья при проведении эндобронхиальной брахитерапии путем облучения мелкими и средними дозами 
Таблица 7.3. Частота возникновения смертельного кровотечения при эндобронхиальной брахитерапии путем облучения высокими дозами 
В МИНОЙ им. П.А.Герцена из 60 пациентов, которым была проведена ЭБЛТ, осложнение возникло лишь у одного: развилась некротическая язва в области бифуркации трахеи после однократного облучения в дозе 7 Гр.
Непосредственные результаты эндобронхиальной лучевой терапии достаточно хорошие и зависят от дозы внутриполостного облучения (табл. 7.4, 7.5).
Таблица 7.4. Непосредственные результаты паллиативной ЭБЛТ (1-3 внутриполостных облучения) 
Таблица 7.5. Непосредственные результаты ЭБЛТ при использовании высоких доз облучения 
При сочетанном лучевом лечении больных местно-распространенным нерезектабельном раком легкого одногодичная выживаемость составила 38%, 2-летняя — 23% (Reddi R. et al., 1992). В исследованиях, проведенных М. Peral (1997), после сочетанного лучевого лечения с использованием высоких доз эндобронхиального облучения у больных с местно-распространенным немелкоклеточным раком легкого более 1 года прожили 75% больных, более 2 лет — 58%. Медиана выживаемости 28 мес. Без рецидива (подтверждено морфологически) более 1 года живут 75% больных.
Сочетанная лучевая терапия у функционально неоперабельных больных центральным раком легкого обеспечила значительное удлинение безрецидивного периода по сравнению с таковым после дистанционного облучения (Huber R. et al., 1997).
Даже при паллиативном лечении медиана выживаемости после эндобронхиальной лучевой терапии составила 14,4 мес, без возобновления роста опухоли более 2 мес наблюдались 48,5% больных (Hennegnin G. et al., 1997).
Благодаря ЭБЛТ можно расширить показания к радикальному лучевому лечению, в том числе больных с поражением обоих главных бронхов и трахеи, ранее считавшихся инкурабельными.
Проведение ЭБЛТ и сочетанной лучевой терапии способствует значительному улучшению онкологических результатов и повышению качества жизни больных благодаря купированию тягостных симптомов болезни.
Читайте также:

