Дренирование печени при раке

-
3 минут на чтение

Дренаж печени необходим при скоплении гноя или токсинов в органе. Вредные кровяные примеси оседают в печени и она, как и другой орган, загрязняется. Помимо дренажа, применяется и тюбаж — откачивание жидкости из желчного пузыря. Все эти действия должен осуществлять специалист, иначе можно серьезно навредить организму.
- Что такое дренаж печени
- Показания
- Неспецифические инфекции
- Наличие паразитарной инфекции в печени
- Противопоказания
- Ход проведения
- Результат
- Последствия
Что такое дренаж печени
Процедура включает в себя удаление гнойного содержимого, который скапливается в паренхиме органа при абсцессе. Абсцесс — это полость, образованная в каком-либо органе, которая заполняется гноем.
Развиться абсцесс может из-за воспаления в печени. При постепенном разрушении долей органа внутри их образуется полость, которая заполняется гноем. Она представляет собой круглое образование с окруженной оболочкой. На начальном этапе абсцесса у человека появляются признаки интоксикации организма.
Дренаж применяется не только при скоплении гноя в самом печеночном органе, гной откачивается и из желчного пузыря и околопеченочной клетчатки.
Показания
Дренаж печени показан при двух патологиях.
Они вызывают процессы воспаления и как следствие скопление гноя в образовавшихся полостях, то есть, к абсцессу. Могут быть вызваны патогенными бактериями, которые проникают в печень из желчевыводящих путей.
Чаще это эхинококки и печеночный сосальщик. Это приводит к кистозным образованиям в полости органа, хотя появлению подобных кист способствуют и другие причины.
Нужен ли дренаж печени, определяет врач, исходя из имеющихся токсинов и гноя в полости печеночного органа. Если этого не сделать, то токсины начнут всасываться в кровь, что приведет к общей интоксикации организма. При помощи консервативных методов и медикаментов гной вывести из печени невозможно.
Противопоказания
Существуют и противопоказания для дренирования печени. Так, дренаж не проводится в следующих случаях:
- Желтуха.
- Беременность на поздних сроках.
- Лишний вес.
- Нарушения в работе сердечной и дыхательной системы.
Если не учесть все эти противопоказания, то могут случиться различные последствия. Самые легкие из них это появление кровотечений, проникновение инфекции, неполное выведение желчи, гноя и т.д.
Ход проведения
Дренаж печеночного органа представляет собой действие врачей, которые осуществляются в условиях стационара. Проводит его хирург.
В области предполагаемого абсцесса делается прокол кожи. Для помощи задействуется УЗИ, которое осуществляет контроль процедуры. В место прокола вводится длинная игла, которая достигает абсцесса, и при помощи ее откачивается гнойная жидкость. То есть эта скопившаяся жидкость при стерильных условиях выходит наружу через иглу. Такой биоматериал обязательно отправляется в дальнейшем на микробиологическиое исследование.
После этого игла не вынимается, а шприц заполняется раствором антисептика, которым промывается образовавшаяся полость для того, чтобы не распространились патогенные бактерии. При необходимости врач накладывает шов или стерильную повязку.
После проведенного дренажа печени человек должен принимать курс антибактериальной терапии с препаратами широкого спектра действия, например, цефалоспорины, амкоксиклав и др. Если выкачивание применяется при паразитарном поражении печени, то техника его такая же, единственным исключением является замена антибиотиков противогельминтными средствами. Иногда гнойное содержимое абсцесса тяжело выкачать обычной иглой, поэтому применяется более толстая, диаметром 1,2-2 мм.
Сдавление желчевыводящих путей злокачественными новообразованиями приводит к развитию механической желтухи. У пациентов повышается уровень билирубина, развивается интоксикация. Онкологи выполняют дренирование желчных протоков при механической желтухе. В Юсуповской больнице работают профессора и врачи высшей категории. Дренирование желчных путей выполняют ведущие онкологи. Все сложные случаи заболевания обсуждают на заседании экспертного совета.
Дренирование желчевыводящих протоков выполняется с целью создания анастомоза между желчными протоками и тонкой кишкой. Оперативное вмешательство позволяет продлить жизнь пациентов, страдающих раком желчного пузыря или печени. Онкологи выполняют дренирование желчного пузыря у пациентов с новообразованиями пузыря и желчных протоков, опухолями в области большого дуоденального сосочка, раком головки поджелудочной железы.
Различают следующие виды дренирования желчных протоков:
- наружное – отток желчи происходит по специально установленному внешнему приёмнику;
- наружно-внутреннее – большая часть желчи попадает в кишку, протекая по ближнему каналу, а меньшая собирается в расположенном снаружи приёмнике;
- внутреннее дренирование – требует эндопротезирования (билиарный дренаж применяют в качестве паллиативного метода лечения неоперабельного рака).
Онкологи Юсуповской больницы индивидуально подходят к выбору метода дренирования желчных протоков при механической желтухе.
Методы дренирования желчных путей
Онкологи предпочитают выполнять у пациентов с механической желтухой опухолевого происхождения наружновнутреннее или, при наличии технических возможностей, наружное дренирование желчных протоков. Оба метода достаточно эффективны при предоперационной подготовке к радикальному оперативному вмешательству или в качестве окончательного метода лечения. Их преимуществом является:
- постоянный контроль поступления желчи;
- возможность активного удаления из желчных протоков крови, гноя, сгустков;
- промывание протоков асептическими растворами;
- динамическое рентгенологическое наблюдение за нахождением дренажной трубки.
В отличие от наружновнутреннего дренирования, по наружному дренажу желчного пузыря желчь полностью поступает наружу. Недостатком наружного дренирования желчных протоков по сравнению с наружновнутренним является полное поступление желчи по дренажу наружу. Для компенсации жизненно важных веществ, которые содержатся в желчи, пациенты вынуждены пить собственную желчь или медицинский персонал вводит её через назогастральный дренаж. При наружновнутреннем дренаже отдалённый конец трубки находится дальше места сужения и большая часть желчи поступает непосредственно в кишку. Сохраняется возможность контролировать проходимость и промывать дренаж, заменить внутренним транспапиллярным эндопротезом.
Внутреннее эндопротезирование желчных протоков выполняют после ликвидации желтухи. Это завершающий этап лечения неоперабельных пациентов. Для успешного выполнения наружной или наружновнутренней холангиостомии онкологи используют набор специальных инструментов: проволочные проводники, специальные пункционные иглы, бужи и катетеры.
Под местным обезболиванием с помощью иглы Шиба хирург туго заполняет контрастным веществом желчные протоки. Длинной иглой диаметром 1,5-1,7 мм осуществляет пункцию одного из сегментарных протоков. Затем по ней проводит проволочный проводник. Конец проводника проводят дальше сужения, по нему выполняют расширение суженного места бужами и устанавливают дренажную трубку. Её фиксируют к коже и промывают желчные протоки стерильными растворами.
Этот метод дренирования имеет недостатки: существует угроза подтекания желчи и крови в брюшную полость в момент извлечения иглы, при проведении проводника или бужировании канала. Кроме того, с этим осложнением можно столкнуться, если наружный диаметр иглы больше наружного диаметра проводника. Для того чтобы уменьшить число осложнений, связанных с пункцией печени, онкологи используют методику установки холангиостомы с помощью стилет-катетера.
Эндоскопический метод
При помощи эндоскопа врачи выполняют назобилиарное дренирование желчевыводящих путей. Показания к эндоскопическому дренированию желчных путей являются:
- механическая желтуха, вызванная злокачественными и доброкачественными новообразованиями;
- острый гнойный холангит;
- наружные желчные свищи;
- повреждение стенок внепеченочных протоков, ретродуоденальные прободения;
- острый холецистит.
Противопоказания к эндоскопическому дренированию отсутствуют за исключением тех случаев, когда трубку для дренирования желчных путей невозможно провести через область опухолевого сужения. Эндоскопический набор для дренирования желчных путей через нос включает:
- проволочный проводник;
- дренажи разнообразной формы;
- соединительную трубку для собирания желчи и промывания дренажа;
- носовую трубку, зажим и шпатель.
Операция эндоскопического дренирования желчных путей включает следующие этапы:
- холангиографию для определения уровня и места установки дренажа;
- введение дренажа с металлическим направителем-проводником;
- извлечение проводника и эндоскопа;
- контрольную холангиографию;
- оценку позиции дренажа;
- перевод дренажа изо рта в нос и фиксацию на голове.
После использования эндоскопического метода дренирования желчных протоков осложнения не развиваются. Они могут возникнуть по причине прогрессирования болезни.
Дренаж после удаления желчного пузыря
После холецистэктомии хирурги часто устанавливают дренаж желчного пузыря. Показаниями к холецистэктомии являются:
- желчекаменная болезнь;
- острый холецистит;
- карцинома желчного пузыря.
Операцию выполняют лапаротомным или лапароскопическим методом. Дренажи из брюшной полости после открытой холецистэктомии удаляют на восьмой день, а у ослабленных и онкологических больных – на двенадцатый день. Для того чтобы не воспалилась кожа вокруг дренажа, желчь отводят в специальный сосуд. Кожные покровы в окружности раны смазывают цинковой мазью или пастой Лассара. Меняют дренажи не ранее двенадцатого послеоперационного дня. При этом проводят фистулографию через дренаж для того чтобы убедиться в свободной проходимости желчных протоков. Удаление дренажей после холецистэктомии производят не четырнадцатого дня, а при дренировании желчных протоков – не ранее двадцать первого дня после удаления желчного пузыря.
Запишитесь на приём, позвонив по телефону. Врачи Юсуповской больницы применяют различные методики дренирования желчных протоков при механической желтухе. Медицинский персонал осуществляет уход за дренажом желчного пузыря и желчных путей.

Билирубин – это конечный продукт метаболизма гемоглобина, который содержится в эритроцитах. Когда состарившиеся эритроциты распадаются, содержащийся в них гемоглобин в ходе нескольких процессов трансформации в итоге превращается в билирубин.
В норме билирубин должен был бы выводиться с желчью в просвет двенадцатиперстной кишки, однако при наличии препятствия такому оттоку он попадает в кровь и оказывает токсическое действие на весь организм.
В онкологической практике причиной механической желтухи, как правило, является сдавление желчных протоков первичными или метастатическими опухолями печени, поджелудочной железы, забрюшинного пространства.
Чем опасна механическая желтуха?
Билирубин обнаруживается в крови и в норме. Однако его максимальные концентрации, как правило, не превышают 20,5 мкмоль/л.
При механической желтухе его концентрация в крови начинает постоянно нарастать и может достигать нескольких сотен мкмоль/л. Такой высокий уровень билирубина оказывает выраженное токсическое действие практически на все биохимические процессы, органы и системы организма. Кроме того, при наличии механической желтухи невозможно ни хирургическое, ни химиотерапевтическое лечение основного заболевания. Дальнейший рост концентрации билирубина приводит к гибели пациента.

Как лечат механическую желтуху опухолевой этиологии?
В настоящее время наиболее эффективной тактикой борьбы с механической желтухой, обусловленной сдавлением желчных протоков опухолями являются дренирующие вмешательства на желчных протоках. Как правило, они выполняются под контролем рентгенотелевидения и (или) ультразвука.

Чаще всего на первом этапе при помощи тонкой и длинной иглы (игла Chiba) доступом через межреберье пунктируются желчные протоки. Через иглу вводят специальное контрастное вещество, которое позволяет увидеть на рентгене сами желчные протоки, а также определить уровень, на котором они заблокированы. Это вмешательство называют пункционная холангиография.
Далее при помощи специального инструмента возможна установка в желчные протоки специального дренажа. Различают дренирование:
- наружное - при котором вся желчь отводится только наружу;
- и наружно-внутреннее - при котором дренаж ставится таким образом, что желчь эвакуируется как наружу, так и в естественном направлении, в кишку.
Как правило, наружно-внутреннее дренирование более физиологично, поскольку при этом не теряются многие важные вещества, содержащиеся в желчи, которое в норме всасываются обратно в кишечнике.
В некоторых случаях, когда опухолевое сдавление изолирует несколько разных сегментов желчного дерева, может потребоваться установка нескольких дренажей.
Хотя дренирование и позволяет справиться с самим симптомом, оно существенно ограничивает качество жизни пациента – дренаж постоянно раздражает брюшную стенку, требует постоянного ухода, есть риск его смещения или даже случайного удаления, а также развития инфекционных осложнений в месте стояния.
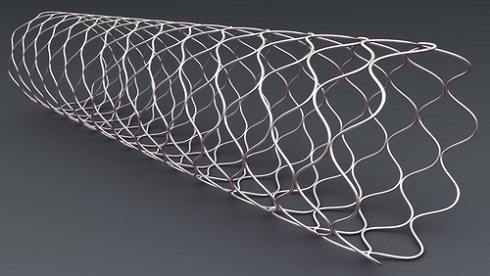
Для преодоления этих недостатков дренирования относительно недавно было предложено завершать дренирующие вмешательства стентированием желчных протоков. Суть стентирования заключается в установке в зону сдавления желчного протока специального (чаще металлического) эндопротеза – стента, который поддерживает желчный проток в открытом состоянии за счет большой радиальной жесткости. При этом дренажную трубку можно удалить совсем, отток желчи будет осуществляться в нормальном направлении по стенту, а точнее по желчному протоку, восстановленному при помощи стента.
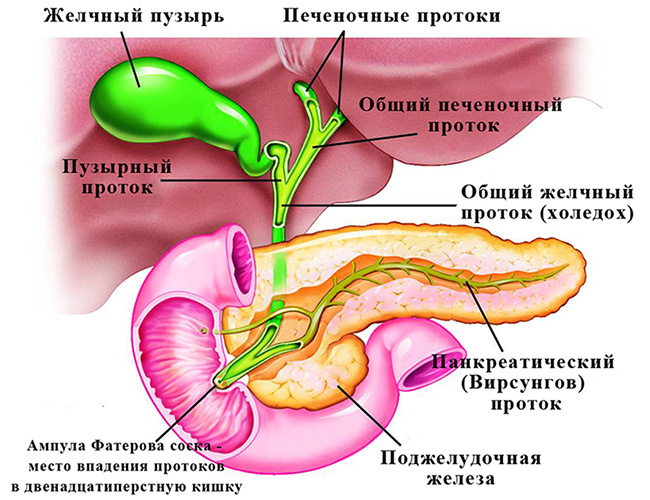
Рис. 1 -Анатомическое строение желчевыводящих путей в норме
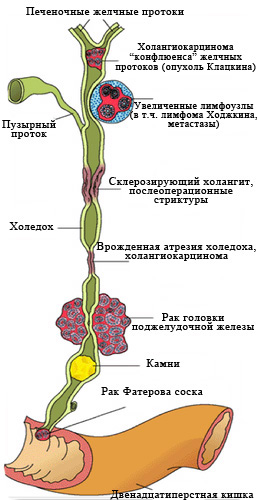
Рис. 2 Наиболее частые причины
возникновения механической желтухи.
Заболеваний, вызывающих нарушение оттока желчи, множество.
Основные - перечислены на рис 2.
К сожалению, в 40-67% случаев причиной механической желтухи являются опухоли, причем доброкачественными они бывают лишь в 2-3% случаев.
Самая частая причина, с которой приходится сталкиваться врачам – это рак головки поджелудочной железы.
Опухоль сдавливает проток извне, нарушая отток желчи. (рис. 3)
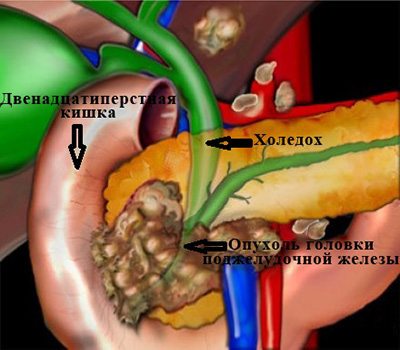
Рассмотреть все возможные виды лечения при различных причинах возникновения механической желтухи в рамках одной статьи невозможно. Поэтому я остановлюсь более подробно на вариантах лечения самой сложной категории больных – со злокачественными образованиями, вызывающими сдавление желчных протоков.
В каждом случае вопрос о возможности полного удаления опухоли решается индивидуально, это зависит от множества факторов: распространенности процесса, возраста больного, наличия сопутствующих заболеваний и т.п. Эти операции считаются одними из самых сложных в современной абдоминальной хирургии и выполняются, как правило, в специализированных отделениях опытными хирургами-онкологами.
Как я уже упоминал, основным параметром, который оценивает выраженность механической желтухи, является уровень общего билирубина в крови. Все вышеперечисленные способы лечения, в том числе и радикальное хирургическое вмешательство, за редким исключением, возможны при уровне общего билирубина крови ниже 50-90 мкмоль\л (норма 3-17 мкмоль\л) из-за высокого риска осложнений. Однако видимая желтушность склер и кожи возникает, как правило, при уровне билирубина выше 100-120 мкмоль\л. При уровне выше 300-350 мкмоль\л билирубин начинает проникать через гематоэнцефаличсекий барьер, т.е. поступать в головной мозг и при дальнейшем нарастании вызывает тяжелую интоксикацию, вплоть до летального исхода.
По данным литературы в условиях обструкции желчных путей и их воспаления оперативное лечение является рискованным, сопровождается большим количеством осложнений, а летальность достигает 10-34%, что в 4 раза выше, чем в тех случаях, когда механическую желтуху удается ликвидировать до операции.
Поэтому одной из первых задач при лечении механической желтухи является снижение уровня билирубина в крови – для лечения интоксикации и подготовки больного для того или иного вида специализированной медицинской помощи (операция, химио- или лучевая терапия).
Консервативная терапия (внутривенные инфузии препаратов) у больных механической желтухой опухолевого генеза редко бывает эффективна. И на первый план выходят хирургические способы декомпрессии желчных протоков – т.е. способы, направленные на восстановление оттока желчи из желчных протоков в пищеварительный тракт. Среди хирургических способов лечения механической желтухи можно выделить три основных направления:
декомпрессии желчных протоков – т.е. способы, направленные на восстановление оттока желчи из желчных протоков в пищеварительный тракт. Среди хирургических способов лечения механической желтухи можно выделить три основных направления:
Последний способ на сегодняшний день используется достаточно редко, так как он сопряжен с боʹльшим количеством осложнений. Его применяют при технической невозможности выполнения операции первыми двумя способами или при отсутствии в стационаре специалистов нужного профиля.
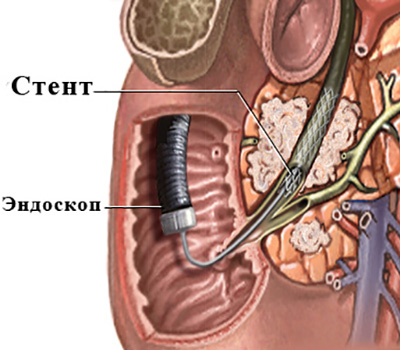
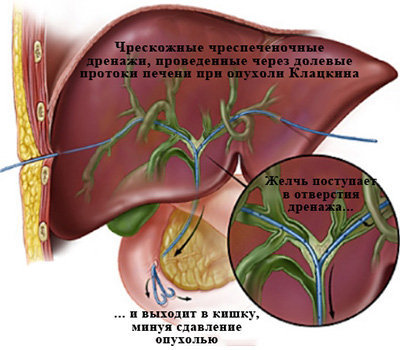
У 70-80% процентов пациентов с механической желтухой возможно применение обоих способов декомпрессии, и тогда выбор во многом зависит от того, насколько тот или иной способ более распространен в конкретном стационаре (техническая оснащенность, опыт того или иного специалиста, от которого во многом зависит процент успешных вмешательств и количество осложнений).
Подробнее о малоинвазивных методиках чрескожногочреспеченочного дренирования и стентирования желчных протоков для купирования механической желтухи можно узнать из второй части статьи.
Являясь специалистом-рентгенохирургом, хочу подробнее остановиться именно на методике чрескожной чреспеченочной декомпрессии желчных протоков при злокачественной природе механической желтухи.
Необходимым условием для выполнения чрескожной пункции является расширение внутрипеченочных желчных протоков до 3-5 мм. При механической желтухе любой этиологии это явление достаточно распространено, при нарушении оттока желчи, она начинает накапливаться в первую очередь именно в протоках, постепенно расширяя их. Если препятствие (камень или опухоль) не полностью сдавливает холедох, т.е. часть желчи все-таки оттекает в кишку, то этот процесс может занять некоторое время.
- Выполняется под местной анестезией (т.е. не требует проведения общего наркоза)
- В опытных руках частота успешного дренирования составляет 98-100% (что превышает технический успех эндоскопических методов).
- Меньшее количество осложнений (при наличии необходимого оборудования и опытных специалистов).
- Выполняется под контролем рентгеноскопии (хотя современное оборудование позволяет снизить дозу излучения до минимальных цифр – меньше, чем при проведении компьютерной томографии).
- При установке наружного или наружно-внутреннего холангиодренажа часть желчи оттекает в специальный пластиковый контейнер, который нужно носить с собой от 3 до 14 дней, что ухудшает качество жизни пациента.
В стационаре больные с механической желтухой поступают на отделения хирургии/онкологии. Как правило, операции направленные на декомпрессию желчных протоков являются ургентными – т.е. достаточно срочными, чтобы избежать осложнений, связанных с интоксикацией билирубином, но при этом и не выполняющиеся сразу же при поступлении больного. Обычно у врачей есть 1-3 дня на дообследование пациента – установку причины желтухи (камень, опухоль, стриктура), определение уровня билирубина крови, и др. анализы, которые нужно учитывать при подготовке к операции.
Больному объясняются цели операции, ее риски и возможные осложнения, подписывается добровольное информированное согласие на процедуру. Накануне разрешается легкий ужин, в день вмешательства – голод.
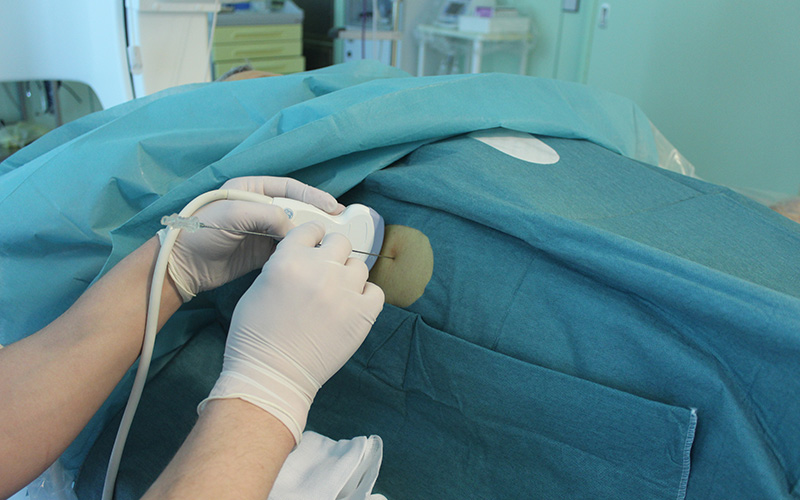
Рис. 2. Пункция желчных протоков под контролем ультразвука справа в 8 межреберьи.
Операции чрескожного чреспеченочного холангиодренирования (ЧЧХД) и стентирования проводятся в специально оборудованной рентгеноперационной.
Вмешательство выполняется под местной анестезией, как правило, 20-30 мл 1% раствора лидокаина. В условиях нашего стационара в операционной всегда находится врач анестезиолог-реаниматолог, который в случае необходимости обеспечивает проведение внутривенной анестезии.
Место пункции выбирается индивидуально, в зависимости от анатомического строения и локализации препятствия. Как правило, доступ к протокам правой доли печени осуществляется из 7-8 межреберья по линии проведенной перпендикулярно от переднего угла подмышечной впадины. Доступ к протокам левой доли – из-под мечевидного отростка.
Правильный выбор доступа в наибольшей степени влияет на безопасность методики.
После обработки кожи раствором антисептика и анестезии, кожа в месте пункции надсекается скальпелем, для облегчения ввода пункционной иглы. Сама игла имеет диаметр менее 1 мм. Под контролем ультразвука или рентгеноскопии она проводится на глубину в 5-10 см до попадания в расширенный желчный проток.
Через иглу вводится несколько миллилитров неионного йодсодержащего контрастного препарата (омнипак, оптирей). Это делается для того, чтобы убедиться в попадании именно в желчный проток, а не сосуды печени. Через просвет иглы заводится тонкий мягкий проводник диаметром до 0,3 мм, игла извлекается, а по установленному проводнику заводится тонкий пластиковый катетер (диаметр менее 2 мм). Через него вводится 20-30 мл контрастного вещества – выполняется т.н. холангиография.
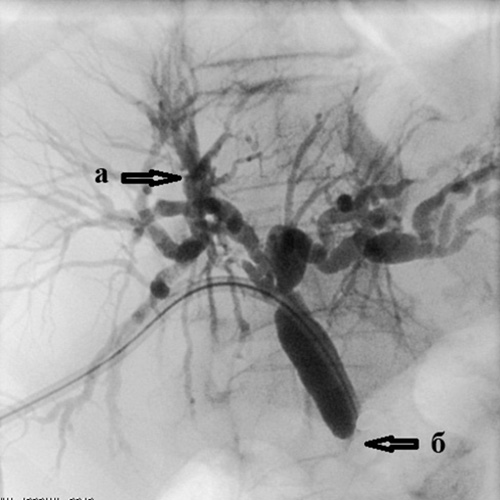
Рис. 3. Чрескожная чреспеченочная холангиография.
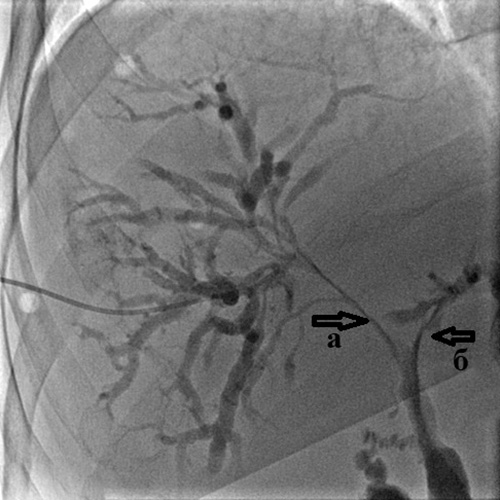
Рис. 4. Холангиография при механической желтухе,
вызванной опухолью Клацкина.
Холангиография при механической желтухе, вызванной опухолью Клацкина.
Определяется выраженное сужение правого (а) и левого (б) долевых желчных протоков
из-за прорастания холангиокарциномы.
Тугое заполнение желчных протоков позволяет с точностью определить уровень
и степень блокирования желчных протоков, степень их расширения, дефекты их заполнения
(видны крупные конкременты ивнутрипросветные опухоли), а также определить тактику
и способ дальнейшего лечения – декомпрессии желчных протоков.
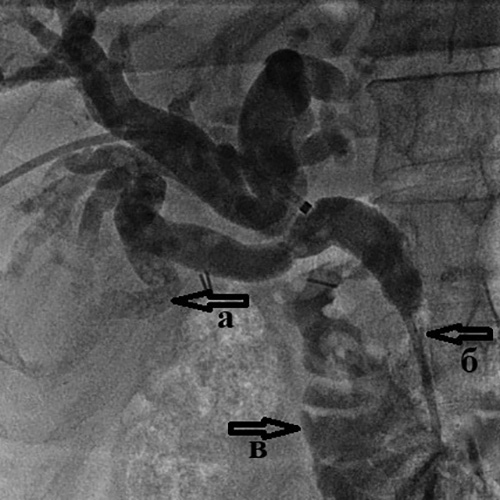
Рис. 5. Холангиография при внутрипеченочном
холангиолитиазе
Холангиография при внутрипеченочном холангиолитиазе:
а) множественные мелкие конкременты (камни) размером до 2-3 мм
внутри расширенных желчных протоков правой доли печени;
б) доброкачественная (поствоспалительная) стриктура терминального отдела холедоха;
в) поступление контрастного вещества в двенадцатиперстную кишку
через установленный чрескожный чреспеченочный дренаж.
Желчь, полученную при первичной пункции желчных протоков,
часто берут на посев и определение чувствительности к антибиотикам.
Это очень способствует борьбе с таким частым осложнением механической желтухи,
как холангит – т.е. воспаление стенки желчного протока.

Рис. 6 - Дренажная трубка для чрескожного чреспеченочного
дренирования желчных протоков.
После определения уровня блока врач при помощи катетеров различной формы и проводников разной жесткости, выполняет реканализацию препятствия (проводник через стриктуру или сдавленный извне холедох проводится в тонкую кишку).
По проводнику в кишку для восстановления оттока желчи заводится пластиковая трубка диаметром около 3 мм с большим количеством отверстий – дренаж.
Он позиционируется таким образом, чтобы дренажные отверстия находились и до и после препятствия. Таким образом, желчь попадает в дренажную трубку до препятствия и выходит из отверстий в кишку уже после него.
На первые 2-3 суток к наружному концу дренажа (в межреберьи) подсоединяется пластиковый мешок. Это позволяет ликвидировать избыток желчи, находящейся в протоках и проконтролировать (вовремя выявить) возможные осложнения, такие как гемобилия – кровотечение в желчные протоки.
Если препятствие пройти не удается, то дренаж оставляется только на наружный отток, чтобы уменьшить уровень билирубина в крови и его токсические эффекты. Желчь в таких случаях больному приходится пить (вместе с соком или водой), так как с ней теряются необходимая жидкость и микроэлементы, которые необходимы и без того истощенному организму. Через несколько дней, когда проходит воспаление и отек стенки желчных протоков, как правило, предпринимается повторная попытка прохождения препятствия. После установки дренажа в нужной позиции он фиксируется к коже швом, что снижает риск его смещения.
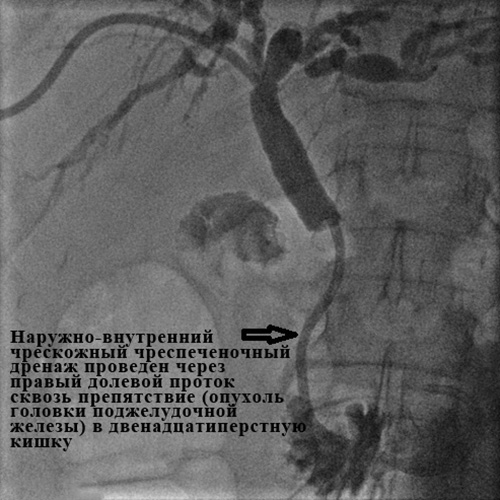
Рис. 7. Наружно-внутреннее чрескожное чреспеченочное холангиодренирование.
Успех дренирования во многом зависит от наличия в стационаре всего спектра инструментария и опыта хирурга, выполняющего вмешательство. В нашем отделении успех наружно-внутреннего дренирования с восстановлением нормального пассажа желчи в кишку составляет 98-99%.
Для того, чтобы избежать этих осложнений, у больных с неоперабельным злокачественным процессом (в некоторых случаях и при других причинах механической желтухи) была разработана операция стентирования желчных протоков. По сути, она является логическим продолжением операции дренирования, и, по-возможности, выполняется стабильным больным с удовлетворительным прогнозом по выживаемости.
Диаметр раскрытого баллона составляет 6-8мм. Баллон сдувается и удаляется, а по тому же проводнику заводится стент.
Стент (как и баллон) свернут на специальной системе доставки, которая является достаточно тонкой, и не требует дополнительного расширения канала, в котором ранее находился дренаж.
Стент заводится и открывается таким образом, чтобы перекрыть стриктуру, но не перекрыть при этом остальные желчные протоки.
 | 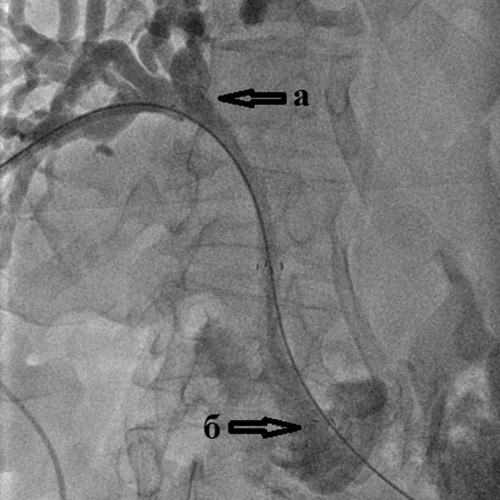 |
| Рис. 11. Стент-графт с политетрафторэтиленовым покрытием для стентирования желчных протоков. | Рис. 12. Стент-графт установленный в холедох от места слияния долевых желчных протоков (а) до двенадцатиперстной кишки (б) для лечения механической желтухи, вызванной метастазами рака толстой кишки в ворота печени. |
При необходимости, в момент раскрывания баллона и стента используют добавление внутривенной анестезии. После установки стента за больным наблюдают несколько дней в условиях хирургического отделения, затем, убедившись в отсутствии осложнений, выписывают для продолжения лечения (химиотерапия, лучевая терапия, фотодинамическая терапия) в специализированном учреждении или по месту жительства (симптоматическая терапия).
В большинстве стационаров Санкт-Петербурга, малоинвазивные операции выполняются платно, т.к. требуют достаточно дорогостоящего расходного материала и наличия опытных специалистов.
Лечение раковых опухолей направлено на то, чтобы полностью удалить или уничтожить злокачественную опухоль, а также все ее метастазы. Такая терапия называется куративной. На поздних стадиях заболевания, когда полное излечение уже невозможно, применяется паллиативная терапия, направленная на улучшение качества жизни больного.
Рак печени (гепатома, гепатоцеллюлярная карцинома) встречается довольно редко.
Печень — самый крупный и один из самых сложных по строению внутренних органов человека.
После сбора анамнеза врач проводит клиническое обследование.
Реабилитация и наблюдение являются важными составляющими лечения онкологических больных.
В настоящее время при раке печени шанс на полное выздоровление есть только в случае успешного оперативного лечения. Существует два варианта удаления опухоли: удаление части органа (частичная резекция печени, гепатэктомия) и пересадка (трансплантация) печени.
Трудность заключается в том, что в большинстве случаев общее состояние пациента не позволяет провести оперативное вмешательство.
В ходе частичного удаления (резекции) печени хирургическим путём удаляется опухоль и часть окружающей её здоровой ткани. Различают анатомическую и атипичную резекцию печени.
Анатомическая резекция подразумевает удаление правой или левой половины печени (гемигепатэктомия), причем граница удаляемого участка не совпадает с границами долей печени, а определяется в зависимости от его кровоснабжения.
В некоторых случаях нужно удалять до 85 % ткани печени, но, если оставшаяся часть органа здорова, то он может нормально функционировать.
Однако если оставшаяся ткань печени поражена циррозом, есть вероятность, что после операции она уже не будет справляться со своими функциями, и пациент может умереть вследствие отказа печени.
Атипичная резекция печени проводится, чтобы сохранить как можно больше ее ткани. Она заключается в том, что иссекается только сама опухоль с минимальным количеством окружающей её здоровой ткани. Эта операция может быть альтернативой для больных циррозом печени, тем не менее, если цирроз находится на прогрессирующей стадии, то она не принесёт желаемого эффекта и её проведение исключается.
Кроме того, цирроз печени зачастую приводит к развитию портальной гипертензии (повышенного давления в воротной вене). В этом случае проведение операции также связано с большим риском.
Резекция печени не исключает вероятность возникновения рецидива. Причиной могут стать микроскопические части опухоли, которые не были удалены в ходе операции. Кроме того, иногда в оставшейся части печени развивается новая опухоль.
Пересадка печени (трансплантация) подразумевает полное удаление печени пациента и замену её здоровым донорским органом.
Этот метод лечения прежде всего рассматривается при циррозе печени с портальной гипертензией, так как трансплантация одновременно избавляет и от этого заболевания. Кроме того, пересадка печени показана пациентам с множественными мелкими очагами опухоли.
Обязательным условием для проведения трансплантации является хорошее общее состояние пациента и отсутствие сопутствующих заболеваний.
После пересадки печени пациент должен в течение долгого времени принимать специальные препараты для подавления активности иммунной системы, чтобы избежать отторжения трансплантата. При ослабленном иммунитете даже самое безобидное инфекционное заболевание может стать угрозой для жизни.
После трансплантации вероятность возникновения новой опухоли существует лишь с том случае, если в организме остались опухолевые клетки вне печени.
Если опухоль нельзя удалить, необходимо сдерживать её рост. В настоящее время существует много возможностей местного лечения опухолей печени, а так как злокачественные новообразования этого органа редко дают метастазы, это позволяет значительно продлить жизнь пациенту и улучшить её качество.
Цель местного лечения — остановить рост опухоли либо разрушить её. Для этого проводится либо склерозирование опухоли, либо остановка её кровоснабжения (эмболизация).
Печень снабжается кровью через две сосудистые системы: печеночную артерию и воротную вену. При этом в опухоль кровь практически всегда поступает по ветвям печеночной артерии. Эта особенность позволяет применять для разрушения опухоли трансартериальную химиоэмболизацию (TACE). Суть этого метода заключается в том, что артерии, по которым кровь поступает в опухоль, закупориваются, в результате чего раковые клетки погибают, а опухоль уменьшается.
В ходе трансартериальной химиоэмболизации через бедренную артерию под местной анестезией вплоть до сосуда, снабжающего опухоль, вводится тонкая трубочка (катетер). Затем в него впрыскивается смесь из нескольких медикаментов: средств, способствующих закупорке сосудов, контрастного вещества или цитостатических препаратов, уничтожающих раковые клетки. Таким образом, происходит двойное воздействие на опухоль: останавливается её кровоснабжение и разрушаются злокачественные клетки.
В ходе лечения может возникнуть ряд побочных эффектов, например, боли в верхней части брюшной полости, повышенная температура и тошнота. Эти симптомы хорошо поддаются лечению и обычно исчезают по окончании терапии.
Обязательным условием для проведения трансартериальной химиоэмболизации является проходимость как печеночной артерии, так и воротной вены. При нарушении проходимости воротной вены эта процедура не проводится, так как в противном случае кровоснабжение печени будет полностью остановлено, что приведёт к смерти пациента.
Одним из видов лечения при помощи теплового воздействия является радиочастотная термоабляция (РЧА). Она заключается в том, что в опухоль через кожу вводится специальный зонд, нагревание которого приводит к гибели раковых клеток.
РЧА проходит под контролем УЗИ или компьютерной томографии. Введение зонда абсолютно безболезненно, так как осуществляется под местным или общим обезболиванием. Сама процедура также не вызывает болевых ощущений, так как в печени нет нервных окончаний.
Аналогичной процедурой является микроволновая абляция (МВА).
Этот инновационный метод (Selective internal radiation therapy, SIRT) основан на введении мельчайших радиоактивных микросфер в опухолевые очаги печени. Они вводятся в организм через катетер в печёночную артерию, откуда частицы попадают в кровеносные сосуды, снабжающие опухоль. В результате происходит остановка кровоснабжения опухоли, а раковые клетки подвергаются радиоактивному облучению. В настоящее время эта терапия активно исследуется.

Лучевая терапия (радиотерапия) является одним из важнейших методов в лечении рака. Ионизирующее излучение воздействует на ядро клетки. Оно разрушает её генетическую информацию (ДНК), в результате чего клетка больше не может делиться. В то время как здоровые клетки в большинстве случаев восстанавливаются после таких изменений, раковые клетки не могут справиться с повреждениями, нанесёнными излучением, и поэтому погибают.
Особенность клеток печени состоит в том, что они не могут регенерироваться после облучения и погибают вместе с раковыми. Поэтому лучевая терапия при лечении опухолей печени применяется только для болеутоления, лечения метастазов и в рамках клинических исследований.
Если опухоль печени уже метастазировала, или же, если очаг расположен так, что проведение локального лечения затруднено, используется системная терапия, воздействующая на весь организм. Под ней подразумевают биологическую, антигормональную или химиотерапию.
В последние годы для лечения рака печени применяют специальные молекулы, подавляющие рост опухолевых клеток (биотерапия). В настоящее время единственным официально разрешенным препаратом является сорафениб. Этот препарат рекомендуется только тем пациентам, чье состояние оценивается как стадия А по Чайлд-Пью.
Эффективность этого метода при раке печени пока не доказана.
Зачастую в ходе операции не удаётся удалить все раковые клетки, например, когда некоторые из них через лимфатические и кровеносные сосуды успели попасть в другие части тела, или если раковая опухоль уже дала отдалённые метастазы. В этом случае назначается химиотерапия.
В ходе химиотерапии разрушаются быстро делящиеся клетки. Медикаменты (цитостатические средства), используемые для этого вида терапии, препятствуют их делению, таким образом предотвращая дальнейшее разрастание опухоли. Кровь распределяет медикаменты по всему организму (системная терапия). Но у этого метода есть недостаток — разрушаются и здоровые быстро делящиеся клетки. К ним относятся, например, клетки слизистых оболочек и волосяных луковиц.
Для лечения рака печени химиотерапия применяется очень редко. Она эффективна только для лечения редкого вида опухоли печени, фиброламеллярной карциномы, при условии отсутствия цирроза печени.
Новые подходы к лечению рака печени с помощью химиотерапии находятся в настоящее время в процессе разработки.
На поздних стадиях, когда состояние пациента оценивается как стадия C по Чайлд-Пью, применение лечения считается нецелесообразным, так как существующие методы терапии не дают положительных результатов и тяжело переносятся пациентами. В таком случае принимается совместное решение врача и пациента о дальнейших действиях, с учетом их преимуществ и недостатков.

Цель генной терапии — встроить в опухолевые клетки такую генетическую информацию, которая приведёт к их гибели.
Например, в ДНК раковых клеток помещаются такие вещества, которые влияют на выработку определённых белков. Эти белки, в свою очередь, могут подавить рост раковой опухоли.
Кроме того, генная терапия подразумевает использование так называемых костимуляторов, благодаря которым иммунная система начинает активно бороться с опухолевыми клетками.
Активация иммунной системы для борьбы против опухоли возможна также при помощи специальной вакцины. Данный метод существует только в рамках исследований и ещё не применялся для лечения людей.
При раке желчных протоков оперативное лечение — единственный шанс на полное выздоровление.
Зачастую опухоль расположена так, что требуется не только удаление самой опухоли, но и удаление значительной части печени. Поэтому оперирование рака желчных протоков — это, как правило, очень обширное вмешательство. Чтобы его перенести, пациент должен находиться в хорошем общем состоянии.
Хирургическое лечение имеет смысл только в том случае, если опухоль резектабельна, то есть если её с технической точки зрения можно полностью удалить. Поэтому на поздних стадиях и при наличии метастазов оперативное вмешательство нецелесообразно.
Иногда перед операцией необходимо выполнить дренирование желчных протоков или эмболизацию (закупорку) сосудов печени, снабжающих опухоль кровью. При местно распространённой опухоли желчных протоков в большинстве случаев требуется расширенная гемигепатэктомия, подразумевающая удаление шести из восьми сегментов печени. Оставшейся части печени обычно достаточно, чтобы этот орган нормально функционировал. Затем удаляется часть желчных протоков и желчный пузырь. Оставшийся желчный проток (правый или левый) соединяется с тонкой кишкой.
Иногда действительный размер опухоли можно оценить только в ходе операции. Поэтому в некоторых случаях, если хирург понимает, что опухоль слишком большая и полностью удалить её не удастся, операцию останавливают.
Раковая опухоль желчных путей и желчного пузыря может привести к их закупорке, в результате чего возникает воспаление желчных протоков. Поэтому пациентам, страдающим от желтухи, необходимо восстановить отток желчи. Это требуется как перед оперативным вмешательством, так и в том случае, когда операция невозможна.
Дренирование обычно проводят в ходе эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) — в желчные протоки устанавливаются специальные трубочки (стенты). Стенты бывают пластиковыми — их необходимо заменять каждые три месяца, и металлическими — их заменять не требуется.
Иногда установки стента бывает недостаточно для восстановления нормального оттока желчи. В этом случае применяется дренирование наружным способом (через печень и кожу). Установка такого дренажа происходит под рентгеновским контролем.
После такого дренирования необходим постоянный контроль дренажной трубки. Ее закупорка очень быстро приводит к воспалению желчных протоков.
На ранних стадиях опухоли желчных протоков обычно относительно небольшого размера, однако в некоторых случаях их расположение не позволяет провести удаление оперативным путём. В этом случае применяется фотодинамическая терапия с использованием лазера.
Фотодинамическая терапия проводится в 2 этапа. На первом этапе, который длится один-два дня, пациенту в форме инъекции вводится специальное вещество (фотосенсибилизатор), которое накапливается в опухоли и делает её восприимчивой к лазерному излучению. На втором этапе в рамках эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) в желчный проток вводят эндоскоп с закреплённым на нём источником лазерного излучения, разрушающего раковые клетки. В здоровой ткани фотосенсибилизатор почти не накапливается, поэтому лазер её не повреждает или повреждает очень незначительно.
Побочным эффектом этого метода лечения является повышенная светочувствительность кожи в течение месяца после лечения.
Эффективность данного вида терапии также изучена не до конца.

Лучевая терапия (радиотерапия) является одним из важнейших методов в лечении рака. Ионизирующее излучение воздействует на ядро клетки, разрушая её генетическую информацию (ДНК), в результате чего клетка больше не может делиться. В то время как здоровые клетки в большинстве случаев восстанавливаются после таких изменений, раковые клетки не могут справиться с повреждениями, нанесёнными излучением, и поэтому погибают. Излучение, используемое при лучевой терапии, аналогично рентгеновскому, но намного сильнее.
В некоторых случаях для симптоматического лечения рекомендуется местная брахитерапия, которая заключается в том, что облучение опухоли производится изнутри. Для этого при помощи гибкой трубки в область опухоли доставляется радиоактивный источник. Брахитерапия уменьшает риск закупорки желчных протоков и, следовательно, возникновения желтухи. Зачастую она проводится в сочетании с фотодинамической терапией.
В некоторых случаях брахитерапия применяется для лечения метастазов.
Для лечения рака желчных протоков химиотерапия применяется только в том случае, если опухоль невозможно удалить оперативным путём, а также, если желчные протоки проходимы. Тем самым замедляется рост новообразования и продлевается жизнь пациента.
В рамках клинических исследований химиотерапия применяется в сочетании с лучевой терапией, после чего проводится трансплантация печени.
Во многих случаях на поздних стадиях рак желчных протоков не поддаётся лечению. В этом случае применяется паллиативная терапия, задача которой заключается в повышении качества жизни больного.
Читайте также:

