Давыдов м и рак желудка
Informo, ergo sum!

Московского
Онкологического
Общества
| №1 (574) 2011 ЯНВАРЬ |
ЗАСЕДАНИЕ 574
состоится во вторник 27 января 2011 г. в 17:00
в конференц-зале клиники Российского онкологического
научного центра им. Н.Н. Блохина
Президиум: проф. А.И. Пачес, академик РАН и РАМН,
проф. М.И. Давыдов
ОДНОМОМЕНТНЫЕ ЭЗОФАГОГАСТРЭКТОМИИ
ОДНОМОМЕНТНАЯ ЭЗОФАГОГАСТРЭКТОМИЯ В ОНКОЛОГИИ
Давыдов М.М., Туркин И.Н.
(Российский онкологический научный центр им. Н.Н. Блохина)
Фиксированные выступления в прениях
Вашакмадзе Л.А., Мамонтов А.С. (МНИОИ им. П.А. Герцена)
Мазурин В.С., Аллахвердян А.С. (МОНИКИ им. М.Ф. Владимирского)
ЭНЦИКЛОПЕДИЯ ХИРУРГИИ РАКА ЖЕЛУДКА
Давыдов М.И., Туркин И.Н., Давыдов М.М.
В 2011 г. выходит в свет книга, основанная на многолетнем опыте хирургии рака желудка, опыте, которым располагает отдел торако-абдоминальной онкологии Российского онкологического научного центра им. Н.Н. Блохина:
М.И. Давыдов, И.Н. Туркин, М.М. Давыдов
ЭНЦИКЛОПЕДИЯ ХИРУРГИИ РАКА ЖЕЛУДКА.
Книга создана как иллюстрированное практическое руководство с акцентом на технические нюансы хирургических вмешательств. Ее главная цель – представить идеологию хирургического лечения больных раком желудка, помочь освоить современную хирургию рака желудка.
Представленная работа будет востребованной и полезной хирургам, занимающимся лечением больных раком желудка.
PROCEEDINGS OF THE MOSCOW CANCER SOCIETY
№ 574 (January 27, 2011)
ONE-STEP ESOPHAGO-GASTRECTOMIES IN ONCOLOGY
Report: ONE-STEP ESOPHAGO-GASTRECTOMIES FOR CANCER LESIONS OF ESOPHAGUS AND STOMACK. By Dr. M.M. Davydov, Prof. I. Turkin, et al. (The N.N. Blokhin Russian Cancer Research Center).
Discussion: Prof. L. Vashakmadze et al. (The P.A. Hertzen Moscow Research Institute of Oncology).
Prof. V. Mazurin et al. (The M.V. Vladimirsky Moscow Region Research Clinical Institute).
Book-presentation: ENCYCLOPEDIA OF GASTRIC CANCER SURGERY. By Prof. M.I. Davydov, Prof. I.N. Turkin, Dr. M.M. Davydov (The N.N. Blokhin Russian Cancer Research Center).
ОДНОМОМЕНТНАЯ ЭЗОФАГОГАСТРЭКТОМИЯ В ОНКОЛОГИИ
Давыдов М.М., Туркин И.Н.
(Российский онкологический научный центр им. Н.Н. Блохина)
Публикации, посвященные одномоментной гастрэктомии и трансторакальной субтотальной резекции пищевода в онкологии, выполняемой по вынужденным показаниям, единичны. Одна из причин – высокий риск и сложность этих вмешательств, из-за чего у подавляющей части пациентов лечение ограничивается паллиативными мерами. Лишь в немногих работах авторы демонстрируют отдельные успешные случаи, причем большинство таких операций не сопровождаются полноценной забрюшинной и медиастинальной лимфодиссекцией.
Одним из наиболее частых показаний к одномоментной эзофагогастрэктомии является синхронный рак желудка и грудного отдела пищевода – редкая, но отнюдь не казуистическая сочетанная патология (рис. 1А). Частота ее составляет от 3,9 до 4,6%.
Не всегда вторую опухоль возможно выявить на дооперационном этапе: при стенозирующем раке пищевода синхронный рак желудка часто оказывается интраоперационной находкой, что требует от хирурга принять ответственное решение – значительно расширить объем вмешательства, либо признать случай иноперабельным и ограничиться симптоматическими мерами.
Высокое распространение рака желудка на пищевод и наличие отсевов в стенке пищевода также является одним из показаний к одномоментной эзофагогастрэктомии (рис. 1Б). Наличие отсевов свидетельствует о подслизистом распространении опухоли по типу ракового лимфангоита, граница которого всегда выше визуально и пальпаторно определяемой.
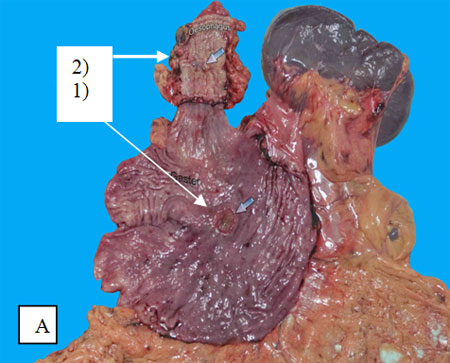
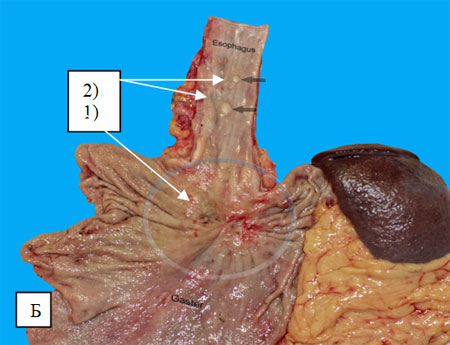
Рис. 1. Макропрепараты после одномоментной эзофагогастрэктомии.
А) Синхронный рак тела желудка (1) и грудного отдела пищевода (2).
Б) Кардио-эзофагеальный рак (1) с отсевами в стенке пищевода (2).
На наш взгляд эта стратегия имеет существенные недостатки:
Для пластического замещения пищевода нами использовалась ободочная кишка. Предоперационное обследование всегда включало колоноскопию для исключения первично- множественного поражения и лапароскопию для исключения перитонеальной диссеминации. Ангиография, как метод изучения особенностей ангиоархитектоники ободочной кишки, не применялась (являясь инвазивной методикой, она не дает исчерпывающей информации о функциональных особенностях сосудистой системы ободочной кишки. Предоперационная пероральная деконтаминация толстой кишки антибиотиками, по нашим данным, не влияет на частоту послеоперационных осложнений. При подготовке к операции ограничиваемся механической очисткой кишечника (прием фортранса / очистительные клизмы).
При планировании эзофагогастрэктомии мы отдаем предпочтение изоперистальтической пластике левой половиной ободочной кишки, которая показала хорошие функциональные результаты. Реже использовался антиперистальтический трансплантат на средних ободочных сосудах. Во всех случаях нам удавалось выкроить достаточный по длине, адекватно кровоснабжаемый трансплантат.
С 1980 по 2010 гг. в РОНЦ выполнено 38 эзофагогастрэктомий, из них 21 по поводу синхронного рака желудка и грудного отдела пищевода и 14 – по поводу рака желудка с распространением на пищевод. Кроме того, трижды нам приходилось использовать этот вид вмешательства в ургентных ситуациях у больных раком желудка на фоне перфорации пищевода. В одном наблюдении перфорация на уровне ретроперикардиального сегмента с развитием медиастинита носила ятрогенный характер и возникла при выполнении эзофагогастроскопии. Во втором, при стенозирующей опухоли проксимального отдела и тела желудка перфорация на уровне ретроперикардиального сегмента с развитием медиастинита была спонтанной. В третьем наблюдении медиастинит и эмпиема плевры справа на фоне пищеводно-плеврального свища были связаны с перфорацией дивертикула грудного отдела пищевода.
В 34 случаях операция выполнялась из двух последовательных доступов – срединной лапаротомии и боковой торакотомии справа по V межреберью в положении больного на левом боку. Лишь у четырех больных вмешательство выполнялось в три этапа, когда операция начиналась с торакотомии в связи с тем, что данные дооперационного обследования не позволяли окончательно оценить резектабельность опухоли пищевода. Между тем, в литературе описаны наблюдения выполнения эзофагогастрэктомии в 4 и даже в 7 этапов (Карачун А.М., 2003):
- Лапаротомия. Ревизия. Опухоль желудка удалима. Толстая кишка без патологии.
- Переднебоковая торакотомия в V межреберье справа. В бифуркационном сегменте пищевода ограниченно смещаемая инфильтративная опухоль протяженностью примерно 7–8 см, прораставшая все слои стенки органа.
- Абдоминальный этап. Мобилизован абдоминальный сегмент пищевода, прошит двумя аппаратами и пересечен между ними. Края лапаротомной раны сведены зажимами.
- Торакотомный этап. Трахеальный сегмент пищевода мобилизован с окружающей клетчаткой, прошит аппаратами и пересечен между ними. Поэтапно пищевод острым путем мобилизован и резецирован. Часть опухоли в связи с врастанием в левый главный бронх оставлена.
- Абдоминальный этап. Учитывая паллиативный характер резекции пищевода от выполнения забрюшинной лимфодиссекции решено отказаться. Гастрэктомия без спленэктомии. Сформирован изоперистальтический толстокишечный трансплантат из правой половины ободочной кишки на средней толстокишечной артерии, аппендэктомия. При оценке кровоснабжения орального конца трансплантата кровоток в сосудах подвздошной кишки признан недостаточным. Подвздошная кишка резецирована.
- Торакальный этап. Трансплантат проведен в плевральную полость. Сформирован эзофагоцекоанастомоз двухрядным узловым швом в куполе правого гемиторакса.
- Абдоминальный этап. Поперечная ободочная кишка пересечена в средней трети, аборальный конец толстокишечного трансплантата анастомозирован с тощей кишкой. Межкишечный анастомоз по Брауну, илео-трансверзоанастомоз.
Оптимальная последовательность этапов, по нашему мнению, должна быть тщательно продумана до вмешательства – это позволяет сократить время операции и минимизировать операционную травму.
ТЕХНИКА ЭЗОФАГОГАСТРЭКТОМИИ. МЕТОДИКА РОНЦ им. Н.Н. БЛОХИНА
Абдоминальный этап. Типично выполняется экстирпация желудка либо надпривратниковая гастрэктомия с D2-лимфодиссекцией. Надпривратниковая гастрэктомия как альтернатива экстирпации желудка выполняется при раке проксимального отдела локализованного типа, если субпилорические лимфоузлы интактны, а отступ от края опухоли составляет не менее 10 см (рис. 2А). Остающаяся часть желудка представлена только привратником.




Частичная диафрагмотомия выполняется всегда – не только с целью иссечения внутридиафрагмальных и наддиафрагмальных лимфатических узлов, но и для предотвращения удавливания толстокишечного трансплантата после перемещения его в плевральную полость.
Подготовка толстокишечного трансплантата. При эзофагогастрэктомии чаще всего применяется пластика левой половиной ободочной кишки. Ободочную кишку мобилизуют на всем протяжении.
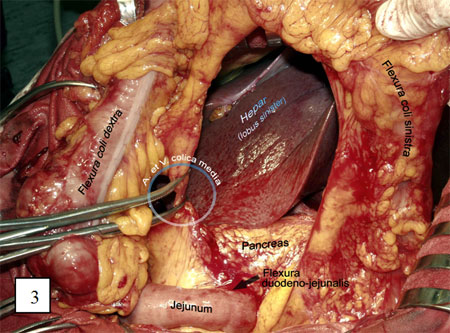
Рис. 3. Выделение и пересечение средних ободочных сосудов.
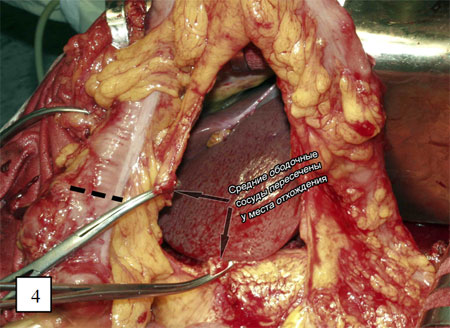
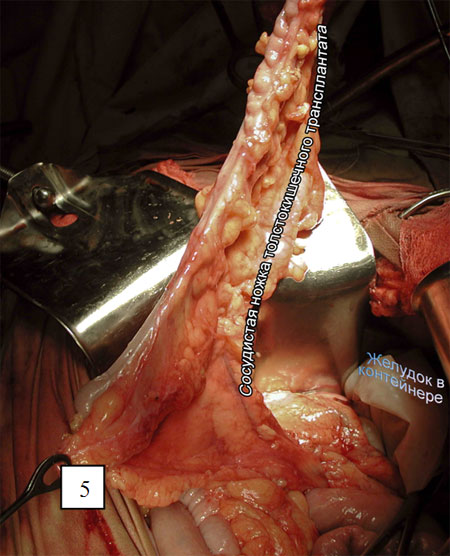
Рис. 4 и 5. Пересечение ободочной кишки в проксимальном направлении.
Выделяют начальный отдел средних ободочных сосудов, лигируя и пересекая их у места отхождения (рис. 3). Ободочную кишку и сосудистую аркаду пересекают в проксимальном направлении с таким расчетом, чтобы оральный конец трансплантата свободно достигал яремной вырезки грудины (рисунки 4 и 5).
Дистально толстую кишку пересекают на границе нисходящего отдела и сигмовидной кишки, сохраняя аркаду и прямые сосуды. Кровоснабжение трансплантата осуществляется из левых ободочных сосудов (рис. 6). Пластика левой половиной ободочной кишки на средних ободочных сосудах предпочтительна только в случаях когда калибр левой ободочной артерии значительно уступает калибру средней (рис. 7).
Трансплантат укладывают, ориентируя его верхушку в диафрагмальном окне, таким образом, чтобы не допустить его перекрута вокруг оси при перемещении в правую плевральную полость на торакальном этапе.

Рис. 6. Схема формирования изоперистальтического трансплантата из поперечно-ободочной кишки с кровоснабжением из левой ободочной артерии.
Рис. 7. Схема формирования антиперистальтического трансплантата из левой половины ободочной кишки с кровоснабжением из средней ободочной артерии.

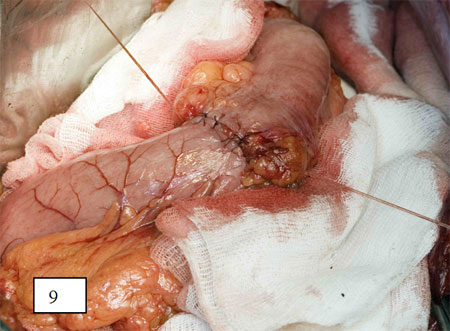
Рис. 9. Формирование толстокишечно-желудочного анастомоза после надпривратниковой гастрэктомии.
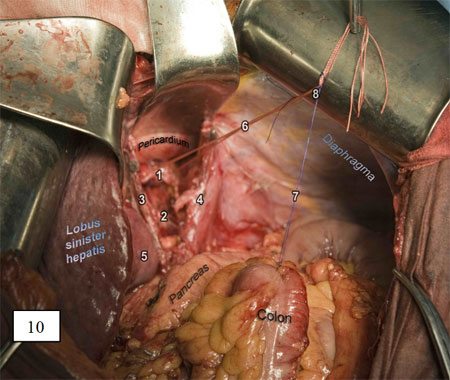
Рис. 10. Нити, фиксирующие толстокишечный трансплантат и пищевод, связаны. Они играют роль проводника при перемещении толстой кишки в плевральную полость.
Торакальный этап. Выполняется боковая торакотомия по V межреберью. После окончания мобилизации пищевода с медиастинальной лимфодиссекцией рассекают пищеводно-диафрагмальную связку, после чего толстокишечный трансплантат за нить-проводник выводят в правую плевральную полость через диафрагмальное окно, не допуская его перекрута по оси.
Пищевод пересекают на уровне трахеального сегмента, оставляя небольшой избыток слизистой. Окончательный вид операционного поля после типичной трансторакальной резекции грудного отдела пищевода представлен на рис. 11.

Рис. 11. Вид операционного поля после резекции грудного отдела пищевода с билатеральной медиастинальной лимфодиссекцией.
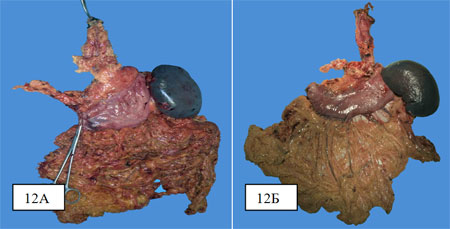
На рис. 12 представлены препараты после надпривратниковой гастрэктомии с резекцией грудного отдела пищевода (12А) и после тотальной гастрэктомии с резекцией грудного отдела пищевода (рис. 12Б).
Непосредственные результаты. В группе из 38 оперированных частота послеоперационных осложнений составила 28,9%; умерли 3 (7,9%) больных – от гнойно-септических осложнений вследствие некроза толстокишечного трансплантата, деструктивной двухсторонней пневмонии, острой печеночной недостаточности.
ЭНЦИКЛОПЕДИЯ ХИРУРГИИ РАКА ЖЕЛУДКА
Давыдов М.И., Туркин И.Н., Давыдов М.М.
Из предисловия: Ситуация, отражающая состояние диагностики и лечения рака жeлyдкa в России драматична: одногодичная летальность этой категории больных составляет 57%. Выявление рака в ранних стадиях, с учетом возможностей современной онкологии, было бы идеальным решением проблемы, однако, как показал мировой опыт, массовый скрининг, за исключением Японии, не привел к желаемым результатам.
Не оправдываются пока надежды, возлагаемые онкологами на различные схемы мультимодальной терапии.
Отдаленное метастазирование обусловлено биологическими особенностями опухоли и относится к хирургически неконтролируемым факторам прогноза. Проблема же локорегионарного рецидивирования находится в пределах досягаемости хирургического метода и в значительной степени определяет место и принципы этого метода в онкологии.
На сегодняшний день объем хирургического вмешательства, набор технических приемов и их последовательность в различных хирургических клиниках весьма вариабельны, что делает невозможным корректное сравнение как непосредственных, так и отдаленных результатов оперативного лечения рака желудка. В связи с этим назрела острая необходимость стандартизации операций при раке желудка. Главные ее задачи – обеспечение онкологической адекватности и технической безопасности вмешательства, а также профилактика послеоперационных хирургических осложнений и максимально возможная функциональность.
Настоящая книга построена не по принципу классического научного труда. Она задумана как иллюстрированное практическое руководство с акцентом на технические нюансы хирургических вмешательств.
Ее главная цель – представить идеологию хирургического лечения рака желудка в РОНЦ им. Н.Н. Блохина, сформировать у читателя философию хирурга-онколога, помочь освоить современную хирургию рака желудка. Хирургию в том виде, в каком она должна быть с точки зрения хирурга-онколога: агрессивная, носящая примерно в половине наблюдений комбинированный характер, сопровождающаяся широкой превентивной лимфодиссекцией.
Представленные методологические приемы операций основаны на многолетнем опыте отдела торако-абдоминальной онкологии Российского онкологического научного центра им. Н.Н. Блохина (зав. – академик РАН и РАМН, проф. М.И. Давыдов). Их использование позволит хирургам избежать многих интра- и послеоперационных осложнений, а также минимизировать вероятность местного рецидива.
Большое внимание в книге уделено многочисленным вариантам сосудистой системы желудка, значению лимфогенного метастазирования, сравнительной характеристике применяемых в настоящее время классификаций рака желудка.
Коллективом отделения эндоскопии РОНЦ им. Н.Н. Блохина (зав. – проф. Г.В. Унгиадзе) представлен опыт, касающийся радикальных эндохирургических вмешательств при раннем раке желудка.
Из представленных в настоящем руководстве 1038 фотографий и схематических изображений 1009 являются оригинальными. Рисунки выполнены К.В. Телициной и Т.А. Красавиной. Единичные иллюстрации заимствованы из современных отечественных и зарубежных руководств по хирургии рака желудка. Гистологическая классификация рака желудка и фотографии гистологических препаратов представлены отделом патологической анатомии опухолей человека РОНЦ им. Н.Н. Блохина (зав. – проф. А.И. Карселадзе). Рентгенограммы представлены отделом лучевой диагностики и рентгенохирургических методов диагностики и лечения (зав. – чл.-корр. РАМН, проф. Б.И. Долгушин).
Раздел по анатомии лимфатической системы основан на результатах исследований нашего соотечественника, пионера лимфологии профессора Д.А. Жданова, работы которого по настоящее время являются основополагающими в понимании механизмов лимфогенного метастазирования рака желудка.
Мы надеемся, что представленная работа окажется востребованной и полезной для хирургов, занимающихся лечением больных раком желудка.
Лауреат Государственной премии РФ в области науки и техники (2002), Заслуженный деятель науки РФ. Главный онколог медицинского центра Управления делами Президента РФ, заведующий кафедрой онкологии Первого Московского Государственного Медицинского университета им. И.М.Сеченова. Член Европейского и Американского общества хирургов, член Международного общества хирургов, член Нью-Йоркской академии наук.
В 2003 году принят действительным членом в Российскую академию наук, в 2004 году — в Российскую академию медицинских наук. В 2006 году избран президентом РАМН. Занимал этот пост до 1 марта 2011 года.
Научная и практическая деятельность академика Давыдова посвящена разработке новых и совершенствованию существующих методов оперативного лечения опухолей лёгкого, пищевода, желудка, средостения. Он разработал принципиально новую методику внутриплевральных желудочно-пищеводных и пищеводно-кишечных анастомозов, отличающуюся оригинальностью технического выполнения, безопасностью и высокой физиологичностью. За счёт применения медиастинальной и ретроперитонеальной лимфодиссекции улучшены результаты лечения рака пищевода, лёгкого, желудка.
М.И. Давыдов первым в онкохирургии стал проводить операции с пластикой полой вены, лёгочной артерии, аорты. Им разработан метод комбинированной резекции пищевода с циркулярной резекцией и пластикой трахеи при раке пищевода, осложнённом пищеводно-трахеальным свищом.
М.И. Давыдовым создана школа онкологов-хирургов, занимающихся вопросами уточненной диагностики и совершенствования лечения злокачественных опухолей с привлечением самых современных достижений различных направлений экспериментальной и практической онкологии. Под его руководством защищено 53 докторских и 50 кандидатских диссертации. Он является автором и соавтором более 900 научных работ, включая 34 монографии и 9 научно-методических фильмов.
Деятельность Михаила Давыдова отмечена Государственной премией РФ и званием Заслуженного деятеля науки Российской Федерации.
1997 год – заслуженный деятель науки РФ.
2001 год – присуждена премия имени Т.И.Ерошевского за лучшую медицинскую работу в области медицинской геронтологии и гериатрии.
2002 год – награжден Орденом Почета.
2008 год – лауреат премии "Триумф-наука" в области наук о жизни и медицины.
2013 год – Почетный член академии художеств России (постановление Президиума академии художеств России от 24.12.2013г).
2014 год – лауреат российской премии Людвига Нобеля.
2015 год – Главный онколог МЗ РФ, академик РАН Михаил Иванович Давыдов избран Почетным доктором Института экспериментальной медицины за выдающиеся достижения в онкологии.
Наименование работы
Название издательства, год издания
Соавторы
Современные принципы выбора лечебной тактики и возможности хирургического лечения немелкококлеточного рака легкого
В кн.: Новое в терапии рака легкого gпод. ред. Н.И. Переводчиковой (терапия рака легкого начала ХХI века), Москва, 2003, с. 41-53
Внутриплевральная колоэзофагопластика в лечении больных раком пищевода
Рак желудка [С16]
Энциклопедия клинической онкологии: Руководство для практических врачей. РЛС, стр. 223 - 237
Хирургическое лечение солитарных и единичных метастазов рака почки в легкие
Хирургическое лечение рака почки с опухолевым тромбозом почечной и нижней полой вен
Хирургическое лечение местного рецидива рака почки после нефрэктомии
Перспективы адоптивной иммунотерапии радикально оперированного рака желудка
Киселевский М.В. Титов К.С.
Эволюция представлений о хирургии рака легкого от эпохи проф. Б.Е.Петерсона до наших дней.
Полоцкий Б.Е. Волков С..М.
Организация онкологической помощи в России и распространенность злокачественных новообразований среди взрослых
Место видеохирургии в диагностике объемных образований органов грудной клетки
Комов Д.В. Комаров И.Г.
Санкт-Петербург, 2013, ISBN 978-5-93929-234-4
Informo, ergo sum!

Московского
Онкологического
Общества
| №1 (574) 2011 ЯНВАРЬ |
ЗАСЕДАНИЕ 574
состоится во вторник 27 января 2011 г. в 17:00
в конференц-зале клиники Российского онкологического
научного центра им. Н.Н. Блохина
Президиум: проф. А.И. Пачес, академик РАН и РАМН,
проф. М.И. Давыдов
ОДНОМОМЕНТНЫЕ ЭЗОФАГОГАСТРЭКТОМИИ
ОДНОМОМЕНТНАЯ ЭЗОФАГОГАСТРЭКТОМИЯ В ОНКОЛОГИИ
Давыдов М.М., Туркин И.Н.
(Российский онкологический научный центр им. Н.Н. Блохина)
Фиксированные выступления в прениях
Вашакмадзе Л.А., Мамонтов А.С. (МНИОИ им. П.А. Герцена)
Мазурин В.С., Аллахвердян А.С. (МОНИКИ им. М.Ф. Владимирского)
ЭНЦИКЛОПЕДИЯ ХИРУРГИИ РАКА ЖЕЛУДКА
Давыдов М.И., Туркин И.Н., Давыдов М.М.

В 2011 г. выходит в свет книга, основанная на многолетнем опыте хирургии рака желудка, опыте, которым располагает отдел торако-абдоминальной онкологии Российского онкологического научного центра им. Н.Н. Блохина:
М.И. Давыдов, И.Н. Туркин, М.М. Давыдов
ЭНЦИКЛОПЕДИЯ ХИРУРГИИ РАКА ЖЕЛУДКА.
Книга создана как иллюстрированное практическое руководство с акцентом на технические нюансы хирургических вмешательств. Ее главная цель – представить идеологию хирургического лечения больных раком желудка, помочь освоить современную хирургию рака желудка.
Представленная работа будет востребованной и полезной хирургам, занимающимся лечением больных раком желудка.
PROCEEDINGS OF THE MOSCOW CANCER SOCIETY
№ 574 (January 27, 2011)
ONE-STEP ESOPHAGO-GASTRECTOMIES IN ONCOLOGY
Report: ONE-STEP ESOPHAGO-GASTRECTOMIES FOR CANCER LESIONS OF ESOPHAGUS AND STOMACK. By Dr. M.M. Davydov, Prof. I. Turkin, et al. (The N.N. Blokhin Russian Cancer Research Center).
Discussion: Prof. L. Vashakmadze et al. (The P.A. Hertzen Moscow Research Institute of Oncology).
Prof. V. Mazurin et al. (The M.V. Vladimirsky Moscow Region Research Clinical Institute).
Book-presentation: ENCYCLOPEDIA OF GASTRIC CANCER SURGERY. By Prof. M.I. Davydov, Prof. I.N. Turkin, Dr. M.M. Davydov (The N.N. Blokhin Russian Cancer Research Center).
ОДНОМОМЕНТНАЯ ЭЗОФАГОГАСТРЭКТОМИЯ В ОНКОЛОГИИ
Давыдов М.М., Туркин И.Н.
(Российский онкологический научный центр им. Н.Н. Блохина)
Публикации, посвященные одномоментной гастрэктомии и трансторакальной субтотальной резекции пищевода в онкологии, выполняемой по вынужденным показаниям, единичны. Одна из причин – высокий риск и сложность этих вмешательств, из-за чего у подавляющей части пациентов лечение ограничивается паллиативными мерами. Лишь в немногих работах авторы демонстрируют отдельные успешные случаи, причем большинство таких операций не сопровождаются полноценной забрюшинной и медиастинальной лимфодиссекцией.
Одним из наиболее частых показаний к одномоментной эзофагогастрэктомии является синхронный рак желудка и грудного отдела пищевода – редкая, но отнюдь не казуистическая сочетанная патология (рис. 1А). Частота ее составляет от 3,9 до 4,6%.
Не всегда вторую опухоль возможно выявить на дооперационном этапе: при стенозирующем раке пищевода синхронный рак желудка часто оказывается интраоперационной находкой, что требует от хирурга принять ответственное решение – значительно расширить объем вмешательства, либо признать случай иноперабельным и ограничиться симптоматическими мерами.
Высокое распространение рака желудка на пищевод и наличие отсевов в стенке пищевода также является одним из показаний к одномоментной эзофагогастрэктомии (рис. 1Б). Наличие отсевов свидетельствует о подслизистом распространении опухоли по типу ракового лимфангоита, граница которого всегда выше визуально и пальпаторно определяемой.


Рис. 1. Макропрепараты после одномоментной эзофагогастрэктомии.
А) Синхронный рак тела желудка (1) и грудного отдела пищевода (2).
Б) Кардио-эзофагеальный рак (1) с отсевами в стенке пищевода (2).
На наш взгляд эта стратегия имеет существенные недостатки:
Для пластического замещения пищевода нами использовалась ободочная кишка. Предоперационное обследование всегда включало колоноскопию для исключения первично- множественного поражения и лапароскопию для исключения перитонеальной диссеминации. Ангиография, как метод изучения особенностей ангиоархитектоники ободочной кишки, не применялась (являясь инвазивной методикой, она не дает исчерпывающей информации о функциональных особенностях сосудистой системы ободочной кишки. Предоперационная пероральная деконтаминация толстой кишки антибиотиками, по нашим данным, не влияет на частоту послеоперационных осложнений. При подготовке к операции ограничиваемся механической очисткой кишечника (прием фортранса / очистительные клизмы).
При планировании эзофагогастрэктомии мы отдаем предпочтение изоперистальтической пластике левой половиной ободочной кишки, которая показала хорошие функциональные результаты. Реже использовался антиперистальтический трансплантат на средних ободочных сосудах. Во всех случаях нам удавалось выкроить достаточный по длине, адекватно кровоснабжаемый трансплантат.
С 1980 по 2010 гг. в РОНЦ выполнено 38 эзофагогастрэктомий, из них 21 по поводу синхронного рака желудка и грудного отдела пищевода и 14 – по поводу рака желудка с распространением на пищевод. Кроме того, трижды нам приходилось использовать этот вид вмешательства в ургентных ситуациях у больных раком желудка на фоне перфорации пищевода. В одном наблюдении перфорация на уровне ретроперикардиального сегмента с развитием медиастинита носила ятрогенный характер и возникла при выполнении эзофагогастроскопии. Во втором, при стенозирующей опухоли проксимального отдела и тела желудка перфорация на уровне ретроперикардиального сегмента с развитием медиастинита была спонтанной. В третьем наблюдении медиастинит и эмпиема плевры справа на фоне пищеводно-плеврального свища были связаны с перфорацией дивертикула грудного отдела пищевода.
В 34 случаях операция выполнялась из двух последовательных доступов – срединной лапаротомии и боковой торакотомии справа по V межреберью в положении больного на левом боку. Лишь у четырех больных вмешательство выполнялось в три этапа, когда операция начиналась с торакотомии в связи с тем, что данные дооперационного обследования не позволяли окончательно оценить резектабельность опухоли пищевода. Между тем, в литературе описаны наблюдения выполнения эзофагогастрэктомии в 4 и даже в 7 этапов (Карачун А.М., 2003):
- Лапаротомия. Ревизия. Опухоль желудка удалима. Толстая кишка без патологии.
- Переднебоковая торакотомия в V межреберье справа. В бифуркационном сегменте пищевода ограниченно смещаемая инфильтративная опухоль протяженностью примерно 7–8 см, прораставшая все слои стенки органа.
- Абдоминальный этап. Мобилизован абдоминальный сегмент пищевода, прошит двумя аппаратами и пересечен между ними. Края лапаротомной раны сведены зажимами.
- Торакотомный этап. Трахеальный сегмент пищевода мобилизован с окружающей клетчаткой, прошит аппаратами и пересечен между ними. Поэтапно пищевод острым путем мобилизован и резецирован. Часть опухоли в связи с врастанием в левый главный бронх оставлена.
- Абдоминальный этап. Учитывая паллиативный характер резекции пищевода от выполнения забрюшинной лимфодиссекции решено отказаться. Гастрэктомия без спленэктомии. Сформирован изоперистальтический толстокишечный трансплантат из правой половины ободочной кишки на средней толстокишечной артерии, аппендэктомия. При оценке кровоснабжения орального конца трансплантата кровоток в сосудах подвздошной кишки признан недостаточным. Подвздошная кишка резецирована.
- Торакальный этап. Трансплантат проведен в плевральную полость. Сформирован эзофагоцекоанастомоз двухрядным узловым швом в куполе правого гемиторакса.
- Абдоминальный этап. Поперечная ободочная кишка пересечена в средней трети, аборальный конец толстокишечного трансплантата анастомозирован с тощей кишкой. Межкишечный анастомоз по Брауну, илео-трансверзоанастомоз.
Оптимальная последовательность этапов, по нашему мнению, должна быть тщательно продумана до вмешательства – это позволяет сократить время операции и минимизировать операционную травму.
ТЕХНИКА ЭЗОФАГОГАСТРЭКТОМИИ. МЕТОДИКА РОНЦ им. Н.Н. БЛОХИНА
Абдоминальный этап. Типично выполняется экстирпация желудка либо надпривратниковая гастрэктомия с D2-лимфодиссекцией. Надпривратниковая гастрэктомия как альтернатива экстирпации желудка выполняется при раке проксимального отдела локализованного типа, если субпилорические лимфоузлы интактны, а отступ от края опухоли составляет не менее 10 см (рис. 2А). Остающаяся часть желудка представлена только привратником.




Частичная диафрагмотомия выполняется всегда – не только с целью иссечения внутридиафрагмальных и наддиафрагмальных лимфатических узлов, но и для предотвращения удавливания толстокишечного трансплантата после перемещения его в плевральную полость.
Подготовка толстокишечного трансплантата. При эзофагогастрэктомии чаще всего применяется пластика левой половиной ободочной кишки. Ободочную кишку мобилизуют на всем протяжении.

Рис. 3. Выделение и пересечение средних ободочных сосудов.


Рис. 4 и 5. Пересечение ободочной кишки в проксимальном направлении.
Выделяют начальный отдел средних ободочных сосудов, лигируя и пересекая их у места отхождения (рис. 3). Ободочную кишку и сосудистую аркаду пересекают в проксимальном направлении с таким расчетом, чтобы оральный конец трансплантата свободно достигал яремной вырезки грудины (рисунки 4 и 5).
Дистально толстую кишку пересекают на границе нисходящего отдела и сигмовидной кишки, сохраняя аркаду и прямые сосуды. Кровоснабжение трансплантата осуществляется из левых ободочных сосудов (рис. 6). Пластика левой половиной ободочной кишки на средних ободочных сосудах предпочтительна только в случаях когда калибр левой ободочной артерии значительно уступает калибру средней (рис. 7).
Трансплантат укладывают, ориентируя его верхушку в диафрагмальном окне, таким образом, чтобы не допустить его перекрута вокруг оси при перемещении в правую плевральную полость на торакальном этапе.

Рис. 6. Схема формирования изоперистальтического трансплантата из поперечно-ободочной кишки с кровоснабжением из левой ободочной артерии.
Рис. 7. Схема формирования антиперистальтического трансплантата из левой половины ободочной кишки с кровоснабжением из средней ободочной артерии.


Рис. 9. Формирование толстокишечно-желудочного анастомоза после надпривратниковой гастрэктомии.

Рис. 10. Нити, фиксирующие толстокишечный трансплантат и пищевод, связаны. Они играют роль проводника при перемещении толстой кишки в плевральную полость.
Торакальный этап. Выполняется боковая торакотомия по V межреберью. После окончания мобилизации пищевода с медиастинальной лимфодиссекцией рассекают пищеводно-диафрагмальную связку, после чего толстокишечный трансплантат за нить-проводник выводят в правую плевральную полость через диафрагмальное окно, не допуская его перекрута по оси.
Пищевод пересекают на уровне трахеального сегмента, оставляя небольшой избыток слизистой. Окончательный вид операционного поля после типичной трансторакальной резекции грудного отдела пищевода представлен на рис. 11.

Рис. 11. Вид операционного поля после резекции грудного отдела пищевода с билатеральной медиастинальной лимфодиссекцией.
На рис. 12 представлены препараты после надпривратниковой гастрэктомии с резекцией грудного отдела пищевода (12А) и после тотальной гастрэктомии с резекцией грудного отдела пищевода (рис. 12Б).

Непосредственные результаты. В группе из 38 оперированных частота послеоперационных осложнений составила 28,9%; умерли 3 (7,9%) больных – от гнойно-септических осложнений вследствие некроза толстокишечного трансплантата, деструктивной двухсторонней пневмонии, острой печеночной недостаточности.
ЭНЦИКЛОПЕДИЯ ХИРУРГИИ РАКА ЖЕЛУДКА
Давыдов М.И., Туркин И.Н., Давыдов М.М.
Из предисловия: Ситуация, отражающая состояние диагностики и лечения рака жeлyдкa в России драматична: одногодичная летальность этой категории больных составляет 57%. Выявление рака в ранних стадиях, с учетом возможностей современной онкологии, было бы идеальным решением проблемы, однако, как показал мировой опыт, массовый скрининг, за исключением Японии, не привел к желаемым результатам.
Не оправдываются пока надежды, возлагаемые онкологами на различные схемы мультимодальной терапии.
Отдаленное метастазирование обусловлено биологическими особенностями опухоли и относится к хирургически неконтролируемым факторам прогноза. Проблема же локорегионарного рецидивирования находится в пределах досягаемости хирургического метода и в значительной степени определяет место и принципы этого метода в онкологии.
На сегодняшний день объем хирургического вмешательства, набор технических приемов и их последовательность в различных хирургических клиниках весьма вариабельны, что делает невозможным корректное сравнение как непосредственных, так и отдаленных результатов оперативного лечения рака желудка. В связи с этим назрела острая необходимость стандартизации операций при раке желудка. Главные ее задачи – обеспечение онкологической адекватности и технической безопасности вмешательства, а также профилактика послеоперационных хирургических осложнений и максимально возможная функциональность.
Настоящая книга построена не по принципу классического научного труда. Она задумана как иллюстрированное практическое руководство с акцентом на технические нюансы хирургических вмешательств.
Ее главная цель – представить идеологию хирургического лечения рака желудка в РОНЦ им. Н.Н. Блохина, сформировать у читателя философию хирурга-онколога, помочь освоить современную хирургию рака желудка. Хирургию в том виде, в каком она должна быть с точки зрения хирурга-онколога: агрессивная, носящая примерно в половине наблюдений комбинированный характер, сопровождающаяся широкой превентивной лимфодиссекцией.
Представленные методологические приемы операций основаны на многолетнем опыте отдела торако-абдоминальной онкологии Российского онкологического научного центра им. Н.Н. Блохина (зав. – академик РАН и РАМН, проф. М.И. Давыдов). Их использование позволит хирургам избежать многих интра- и послеоперационных осложнений, а также минимизировать вероятность местного рецидива.
Большое внимание в книге уделено многочисленным вариантам сосудистой системы желудка, значению лимфогенного метастазирования, сравнительной характеристике применяемых в настоящее время классификаций рака желудка.
Коллективом отделения эндоскопии РОНЦ им. Н.Н. Блохина (зав. – проф. Г.В. Унгиадзе) представлен опыт, касающийся радикальных эндохирургических вмешательств при раннем раке желудка.
Из представленных в настоящем руководстве 1038 фотографий и схематических изображений 1009 являются оригинальными. Рисунки выполнены К.В. Телициной и Т.А. Красавиной. Единичные иллюстрации заимствованы из современных отечественных и зарубежных руководств по хирургии рака желудка. Гистологическая классификация рака желудка и фотографии гистологических препаратов представлены отделом патологической анатомии опухолей человека РОНЦ им. Н.Н. Блохина (зав. – проф. А.И. Карселадзе). Рентгенограммы представлены отделом лучевой диагностики и рентгенохирургических методов диагностики и лечения (зав. – чл.-корр. РАМН, проф. Б.И. Долгушин).
Раздел по анатомии лимфатической системы основан на результатах исследований нашего соотечественника, пионера лимфологии профессора Д.А. Жданова, работы которого по настоящее время являются основополагающими в понимании механизмов лимфогенного метастазирования рака желудка.
Мы надеемся, что представленная работа окажется востребованной и полезной для хирургов, занимающихся лечением больных раком желудка.
Читайте также:

