Цитостатики при раке яичников
В.И. Борисов
Рак яичников представляет особую форму злокачественных опухолей, так как более чем у 70 % больных к моменту диагностики опухоли развивается асцит. Данная клиническая ситуация обусловлена тем, что диссеминация происходит в результате эксфолиации опухолевых клеток с поверхности пораженного опухолью яичника с током внутрибрюшной жидкости по всей брюшной полости и таким образом, поражает париетальную и висцеральную брюшину, сальник, диафрагму и капсулу печени. Кроме того, при распространенном раке яичников довольно часть имеет место поражение забрюшинного лимфатического коллектора.
У больных с канцероматозно-измененной брюшиной развивается асцит, а в дальнейшем присоединяется и плеврит. Гематогенное метастазирование наблюдается редко, не более чем у 3% больных с поражением печени, костей, головного мозга (1,5).
По данным Чиссова В.И. и сотр. (2) диагноз рака яичников в 2001 году в России был поставлен у 11 788 женщин. Из них у 64,1 % больных была диагностирована опухоль в III-IV стадиях. Одногодичная летальность составила – 33,1 %. Лекарственная терапия была проведена в 12,2 %, а в сочетании с различными видами оперативных вмешательств в 70,7 % случаев.
Сегодня, большинство исследователей клиницистов считают, что химиотерапию можно не назначать только при IA стадии, высокой степени дифференцировки опухоли и настойчивом желании больной сохранить фертильность (1,4). Однако, число подобных больных слишком мало, чтобы повлиять на общую тенденцию назначения химиотерапии при раке яичников, так как более 95 % пациенток должны получать лекарственное противоопухолевое лечение (3,5,6).
Внедрение в клиническую практику новых весьма активных противоопухолевых препаратов, в том числе и при новообразованиях яичников, позволило добиться значительного непосредственного эффекта у 80 %, при этом полная ремиссия отмечалась у 50 % пациенток (7,12,13). Следует признать, что, несмотря на наличие активных цитостатиков и различных схем полихимиотерапии у значительного числа женщин, в различные сроки отмечается рецидив болезни.
Более того, в 15-20 % случаев рака яичников имеет место первичная лекарственная резистентность, в этих случаях не удается достичь лечебного эффекта при использовании схем первой линии химиотерапии. Кроме того, все пациентки, у которых развивается рецидив болезни, становятся резистентными к стандартной химиотерапии (14,15).
Проведенный анализ эффективности химиотерапии в зависимости от времени возникновения рецидива показал, что данный фактор существенно влияет на результаты применения лекарственной терапии в режиме 2 и 3 линий химиотерапии.
Несмотря на применение наиболее активной схемы химиотерапии в качестве первой линии у больных с распространенным раком яичников в значительном проценте случаев возникает рецидив болезни.
В последние годы ведется активное изучение эффективности различных противоопухолевых препаратов в качестве средств 2 и 3 линий химиотерапии у больных с резистентным раком яичников. Для больных чувствительных к препаратам платины, при сроках возобновления роста опухоли 6-12 месяцев и более показано назначение первичной схемы лечения.
В работе Rose и соавт. (16) 25 больным у которых через 6 и более месяцев был зарегистрирован рецидив опухоли после полной клинической ремиссии в результате первоначального лечения Паклитакселом (Таксолом) и платиной была снова назначена терапия Паклитакселом (Таксолом) 135 мг/м 2 в виде 24 часовой инфузии и Карбоплатином (АUC 5-6) каждый 21 день. Среди 20 больных с измеряемыми и подлежащими оценке опрухолями полная регрессия отмечена у 14 (70 %) случаев, у 4 (20 %) отмечалась частичная регрессия опухоли. Медиана времени без прогрессирования болезни составила 9+ месяцев (от 2 до 15+ месяцев). Среди больных пригодных для оценки эффекта это время составило 7+ месяцев. Общая выживаемость в этой группе равнялась 10+ месяцев (от 2 до 21+ месяца).
В другом исследовании (17) из 244 больных леченых по поводу рецидива болезни 84 пациентки получали в качестве 2-ой линии повторно Карбоплатин и Паклитаксел (Таксол). У 66 из 84 больных рецидив был диагностирован при компьютерном обследовании и оценке онкомаркера СА-125. Карбоплатин применялся в дозе АUC 5-6 и Паклитаксел (Таксол) 135 мг/м 2 каждые 3 недели или 60-80 мг/м 2 раз в неделю.
Из 66 оцененных больных у 28 (42,4 %) достигнута полная ремиссия, а у 18 больных (27,3 %) наблюдался частичный эффект.
Таким образом, лечебный эффект у больных с рецидивом опухоли, чувствительных к первичному лечению, был отмечен в 69,7% случаев.
Непосредственный лечебный эффект зависел от времени возникновения рецидива болезни. Так в группе больных, у которых рецидив отмечен в интервале 6-11 месяцев он составил 67 %, а в группе со сроками 12-24 месяца он отмечался у 79 % пациенток. Общая трехлетняя выживаемость составила 72 %. В группе больных, где рецидив зарегистрирован в сроки от 6 до 11 месяцев выживаемость составляла 42 %. В сроки возникновения рецидива 12-24 месяца она составляла 63 %, а при рецидиве болезни в сроке более чем 24 месяца она наблюдалась у 84 % больных.
Трехлетняя выживаемость не различалась у больных, которым выполнялась операция после выявления рецидива болезни. У 7 (8,3 %) отмечены токсические реакции в виде сенсорной нейропатии, у 5 имели место аллергические реакции, у 1 больной анафилактический шок, смертельных случаев не зарегистрировано.
В аналогичном исследовании (18) из 241 больной раком яичников подвергнутых терапии Карбоплатином и Таксолом у 43 отмечен рецидив болезни. Больные были подвергнуты повторному лечению Карбоплатином в дозе AUC 5 и Таксолом 175 мг/м 2 (трехчасовая инфузия). В среднем проведено 6 циклов (от 3 до 9 циклов).
Противоопухолевый эффект был оценен у 37 больных. Из них полный ответ отмечен у 21 (57 %) случаев, частичный у 10 (27 %). Общая эффективность составила 84 %. При полной ремиссии медиана времени без прогрессии составила 10,2 месяца, а общая выживаемость 13,2 месяца. При частичном эффекте эти цифры составляли 8,0 и 14,9 месяца соответственно.
Из токсических проявлений наиболее часто отмечалась миелотоксичность. Доза препаратов была снижена, в связи с нейтропенией у 6 больных, а у 4 отмечено нарушение функции почек.
Несомненный интерес представляют данные об использовании в качестве 2-ой линии монохимиотерапии Таксолом при рецидиве у больных, получавших в качестве 1-й линии Таксол, Карбоплатин или Цисплатин (19).
34 больным с рецидивом рака яичников проводилась монотерапия Таксолом в дозе 135-175 мг/м 2 в виде трехчасовой инфузии. Циклы повторялись каждые 3 недели.
У 15 (44 %) был достигнут лечебный эффект. У больных резистентных к платине этот эффект был зарегистрирован у 5 (33 %) при опухолях, чувствительных к препаратам платины в 10 (53 %) случаях. Медиана безрецидивного течения болезни составила 8,5 месяца. Медиана выживаемости у больных без эффекта лечения равнялась 9 месяцам, в группе больных с лечебным эффектом она была 17 месяцев, то есть в 2 раза выше.
Из токсических проявлений наиболее часто встречалась сенсорная нейропатия (у 13 больных), причем вторая степень была отмечена в 5 случаях. Нейтропения 2 и 3 степени отмечалась у 3 пациенток.
Таким образом, у больных, опухоли которых были чувствительны к Таксолу и препаратам платины при первичном лечении, и если рецидив болезни развивался в поздние сроки, целесообразно проводить терапию теми же препаратами, так как результаты повторного лечения довольно выразительны.
У больных чувствительных к препаратам платины в первой линии химиотерапии оказались активными в монотерапии и другие цитостатики.
В представленной Таблице 1 показаны сводные данные по непосредственной эффективности различных противоопухолевых препаратов в качестве 2-й линии химиотерапии.
Таблица 1. Эффективность монохимиотерапии в качестве 2 линии у больных раком яичников чувствительных к препаратам платины
Противоопухолевый препарат
Доза и режим
Лечебный
эффект (%)
175 мг/м 2
– 24 часовая инфузия
50 мг/м 2
– 21 день
1,5 мг/м 2
– 5 дней
1 мг/м 2
– 1, 8 и 15 дни каждые 28 дней
130 мг/м 2
– двухчасовая инфузия каждый 21 день
110 мг/м 2
– инфузия каждый 21 день
200 мг/м 2
– инфузия каждый 21 день
3,5 мг/м 2
– инфузия каждый 21 день
Липосомальный Доксорубицин (Доксил)
50 мг/м 2
– раз в 21 день
Учитывая эффективность новых цитостатиков при их использовании в монорежиме при резистентном раке яичников, были предприняты попытки разработки и клинической апробации различных схем полихимиотерапии. Многообещающие результаты были получены в клинических исследованиях при применении Гемцитабина в комбинации и препаратов платины. Эффективность Гемцитабина в комбинации с препаратами платины у больных с резистентным раком яичников представлена в Таблице 2
Таблица 2. Непосредственный эффект Гемцитабина и препаратов платины при резистентном раке яичников к препаратам платины
Автор, год
Число б-х
Гемцитабин, доза
Цисплатин, доза
Лечебный эффект (%)
Общий
Полная
регрессия
Kunkеl et al, 1998 (20)
1000 мг/м 2
– 1, 8, 15 дни, каждые 28 дней
30 мг/м 2
– в 1 день
Safra et al, 1999 (21)
1000 мг/м 2
– 1 и 8 дни, каждые 28 дней
30 мг/м 2
– 1 и 8 дни
Nagourney et al, 2000 (22)
750 мг/м 2
– 1 и 8 дни, каждые 28 дней
30 мг/м 2
– 1 и 8 дни
Следует еще раз подчеркнуть, что у такой неблагоприятной категории больных, при использовании Гемцитабина в сочетании с Цисплатином удалось достигнуть не только высокого непосредственного эффекта, но и полной регрессии опухоли в 9–29 % случаев, что говорит о высокой противоопухолевой активности данной комбинации цитостатиков.
С целью снижения нейротоксичности Цисплатин был заменен на Карбоплатин.
Было показано, что эта схема является также высокоэффективной и общий эффект колебался в пределах 62-69 %. В Таблице 3 показаны результаты применения схемы Гемцитабин плюс Карбоплатин у больных раком яичников резистентных к Цисплатину.
Таблица 3. Результаты применения схемы Гемцитабин плюс Карбоплатин у больных раком яичников резистентных к Цисплатину
Автор, год
Число б-х
Гемцитабин, доза
Карбоплатин доза
Лечебный эффект (%)
Общий
Полная
регрессия
Orlando et al, 2000 (23)
1 г/м2 – 1, 8, 15 дни, каждые 28 дней
Du Bois et al, 2000 (24)
1 г/м2 – 1 и 8 дни, каждый 21 день
Jackisch et al, 2001 (25)
1 г/м2 – 1 и 8 дни, каждый 21 день
Гемцитабин с Карбоплатином оказался более активным, чем в сочетании с Цисплатином. Это может быть объяснено тем, что существует синергизм между этими препаратами. Также известно, что механизм развития резистентности опухолевых клеток к препаратам платины обусловлен повышенной репаративной способностью ДНК, а Гемцитабин в силу биохимических особенностей взаимодействия с ДНК препятствует этому процессу. Кроме того, профиль токсичности у этих препаратов различен, что является немаловажным фактором в клинической онкологии (8).
Учитывая высокую эффективность Гемцитабина при резистентных формах рака яичников к препаратам платины были изучены схемы полихимиотерапии с включением Паклитаксела (Таксола). Эффективность Гемцитабина и Паклитаксела (Таксола) представлена в Таблице 4.
Таблица 4. Лечебная эффективность Гемцитабина и Паклитаксела (Таксола)
Автор, год
Число б-х
Гемцитабин
Таксол
Общий
лечебный
эффект (%)
Полная
регрессия
(%)
Poole C. et al, 1998 (26)
1 мг/м 2 – 1, 8, 15 дни
135 мг/м 2 – 8 день
Roman L. et al, 2001 (27)
1 мг/м 2 – 1, 8 и 15 дни
80 мг/м 2 – 1, 8 и 15 дни
Представленные данные указывают, что комбинация Гемцитабина с Паклитакселом (Таксолом) по своей эффективности не уступает схеме с препаратами платины и может быть рекомендована больным с нарушением функции почек.
В последние годы большое внимание уделяется изучению активности нового, оригинального противоопухолевого препарата Гикамтина (Топотекана). Уникальность Гикамтина заключается в его механизме действия, он является ингибитором топоизомеразы 1, фермента участвующего в репликации ДНК.
В начальных исследованиях (9, 28, 29) по изучению противоопухолевой эффективности Гикамтина в качестве препарата 2 линии у больных чувствительных к препаратам платины она колебалась в пределах 33-38 %, со средней длительностью ремиссии 8-11 месяцев.
В другом исследовании (30) сравнивалась непосредственная эффективность Гикамтина и Паклитаксела (Таксола) у 226 больных раком яичников в качестве 2-й линии после применения препаратов платины. Гикамтин применялся в стандартном режиме 1,5 мг/м 2 х 5 дней, а Паклитаксел (175 мг/м 2 ) в виде трехчасовой инфузии.
Общий лечебный эффект в виде полной и частичной ремиссии был достигнут в 20,5 % и 13 % случаев соответственно.
Следует подчеркнуть, что эффективность Гикамтина, как и других цитостатиков, зависит от результатов предшествующего лечения.
При его использовании у 111 больных резистентных к препаратам платины непосредственный эффект зарегистрирован у 5,9% больных, при частичной резистентности к платине этот эффект отмечен у 17,8 % женщин.
При опухолях, чувствительных к препаратам платины, если рецидив диагностирован более чем через 6-12 месяцев с момента завершения лечения, Гикамтин был эффективен у 26,6 % больных.
Имеется незначительный клинический опыт по применению различных комбинаций Гикамтина с другими активными цитостатиками при раке яичников. 36 больным раком яичников, из которых у 19 был выявлен ранний рецидив опухоли до 6 месяцев после окончания химиотерапии 1 линии препаратами платины и таксанами, была применена комбинация Гикамтина в дозе 1,25 мг/м 2 внутривенно в 1-3 дня и Циклофосфана 600 мг/м 2 в 1 день. Курсы повторяли каждые 3 недели. Лечебный эффект наблюдался у 25 %, средняя продолжительность ремиссии более 5 месяцев.
Полученный результат следует признать высоким, так как более половины больных были с неблагоприятным прогнозом, то есть с ранним рецидивом болезни.
Наиболее грозным осложнением в этой группе больных была нейтропения IV степени, которая имела место в 68,8 % случаев, фебрильная нейтропения развилась у 7,1 %. Тромбоцитопения III степени наблюдалась в 18 % случаев (31).
В другом клиническом исследовании (32) Топотекан вводился в дозе 0,5 мг/м 2 х 5 дней, а Гемзар применяли в дозах 800 мг/м 2 в 1 день и 600 мг/м 2 в 8 день. Из 10 больных в 5 случаях отмечен лечебный эффект и у одной больной получена полная регрессия опухоли.
Основной лимитирующей токсичностью Гикамтина является нейтропения III-IV степени. Пик снижения лейкоцитов регистрируется к 7-9 дню от момента завершения лечения.
В семидесятых годах прошлого столетия в терапии рака яичников широко использовался противоопухолевый препарат Гексаметилмеламин (Гексален, Алтретамин), который по механизму действия является алкилирующим агентом.
Отличительной особенностью данного препарата является то, что при приеме внутрь до 90 % подвергается всасыванию, при этом пик концентрации препарата в плазме нас тупает в сроки от одного часа до трех часов (10).
Эффективность Гексалена у больных раком яичников, резистентных к препаратам платины, колебалась от 14 до 21 % (11).
Авторы представили клинические результаты применения схемы Гексален в комбинации с Гемзаром у 8 больных и Гексалена в сочетании с Вепезидом в 10 случаях. Гексален применялся в дозе 160 мг/м 2 в сутки с 1 по 14 день и Гемзар 800 мг/м 2 в 1, 8 и 15 день. В другой схеме Гексален использовали в аналогичном режиме, а Вепезид в дозе 90-60 мг/м 2 применяли внутрь с 1-14 дни.
При использовании Гексалена и Гемзара у 4 больных отмечена частичная регрессия опухоли и стабилизация процесса в 2 случаях. Наиболее частыми проявлениями токсичности были тошнота, рвота и периферическая нейротоксичность I-II степени у 4 больных.
При назначении Гексалена и Вепезида непосредственный эффект зарегистрирован у 5 больных, из них в 2 случаях наблюдалась полная регрессия опухоли.
Наиболее часто в этой группе встречался стоматит в 5 случаях, нейротоксичность имела место в 2 случаях.
Таким образом, авторам удалось достичь непосредственного эффекта при использовании Гексалена и Вепезида у 50 % больных, что является несомненным успехом при использовании схем 2-й линии химиотерапии.
Таким образом, следует еще раз подчеркнуть, что постулирование схем лечения 2-й и 3-й линии химиотерапии является в какой-то степени условным. Сегодня ясно, что схемой первой линии химиотерапии рака яичников является комбинация таксанов и платины, так как ее непосредственная эффективность составляет более 80 %.
В связи с этим необходима дальнейшая разработка новых подходов с использованием биотерапии, вакцин, препаратов, влияющих на различные этапы молекулярной трансформации нормальных клеток в опухолевые, фотодинамической терапии.
Онкологические заболевания , это самые опасные для жизни человека патологические состояния, которые нередко заканчиваются летальным исходом. Главное их коварство заключается в первичном скрытом течении, образовании метастаз, поражающих другие органы. Сегодня участились случаи онкологических заболеваний женской репродуктивной системы. Химиотерапия при раке яичников считается основным методом лечения.
Эффективность и достоинства терапии
Такой метод лечения применяется практически всегда. Однако на некоторых этапах он может быть не совсем эффективным. Например, 4 стадия рака яичников может уже не поддаваться воздействию медикаментозных препаратов. Также на эффективность процедуры влияет место расположения новообразования, возраст пациентки, наличие хронических заболеваний и другие индивидуальные особенности ее организма.
Несмотря на то, что химиотерапия полностью убивает иммунитет человека, она имеет определенные достоинства:
- обеспечивает отмирание злокачественных клеток (частичное или полное),
- позволяет осуществлять мониторинг процесса лечения, так как дает возможность контролировать разрастание пораженных тканей,
- обеспечивает своевременное устранение метастаз,
- уменьшает клинические проявления болезни,
- сочетается с другими методами терапии, хотя часто проводится самостоятельно.
То, насколько хорошо подействуют препараты, зависит от своевременности обнаружения опухоли, реакции организма на лекарства. Если пройти химиотерапию на ранних стадиях развития патологии, то шансы на успех увеличиваются.
Показания и противопоказания к использованию
Если у женщины обнаружился рак яичника, ей может быть назначена операция. Однако и после нее, и до нее пациентке придется принимать сильные химические препараты. Существуют такие показания к их применению:
- Рак 1-3 стадии, который подтвержден результатами цитологического и гистологического исследования.
- Замедление роста опухоли 3-4 степени развития, если она была удалена частично.
- Радикальное удаление новообразования для предупреждения появления метастаз.
- Паллиативная операция на яичниках, проводящаяся для облегчения состояния женщины.
- Подготовка к хирургическому вмешательству с целью повышения его эффективности.
После операции больные проходят как минимум 3 курса химиотерапии. Лечение проводится сразу после удаления, через 40-60 и 90-120 дней после него. Дальнейшая необходимость терапии определяется врачом.
Однако такое лечение используется не всегда. Существуют некоторые противопоказания к применению химических препаратов:
- нарушения работы печени и органов кроветворения,
- тяжелые сопутствующие патологии, которые могут осложниться после приема химических препаратов,
- нарушения функциональности нервной системы,
- психические расстройства.
Вообще, химическая терапия при раке яичников предназначается для торможения роста опухоли, предупреждения метастазирования и рецидивов после операции, увеличения продолжительности жизни.
Виды химиотерапии
Лечение пораженного яичника при помощи химических препаратов бывает адъювантным и неадъювантным. В первом случае лекарства используются после оперативного удаления новообразования. Во втором случае препараты назначаются для уменьшения размеров опухоли перед хирургическим вмешательством.
Также химиотерапия при раке яичников бывает внутривенная и внутрибрюшная. В первом случае применяются цитостатики. Они вводятся в вену и перемещаются вместе с током крови. Каждая такая процедура длится 3-4 часа в условиях амбулатории. Длительность цикла терапии составляет 3 недели. Таких курсов нужно пройти как минимум 6.
При необходимости препараты могут вводиться прямо в брюшную полость посредством катетера. Этот вид лечения способен улучшить выживаемость пациентки при раке яичников. Однако риск побочных эффектов увеличивается.
Техника проведения лечения: самые распространенные схемы
Большинство современных препаратов не вызывают таких негативных последствий, как лекарства первого поколения, однако, все они угнетают иммунитет со всеми вытекающими из этого последствиями. Естественно, лучше бороться со злокачественной опухолью комплексно. В каждом индивидуальном случае используется своя схема лечения:
Лечение постоянно должен контролировать лечащий онколог.
Возможные побочные эффекты и осложнения
Лечить женщину, страдающую раком яичников, химическими препаратами можно на любом этапе развития болезни. Однако при 3-4-й стадии без оперативного вмешательства не обойтись (удаляется матка вместе с придатками). Химиотерапия , это серьезный удар по женскому организму. Длительный прием токсичных лекарств провоцирует такие побочные эффекты:
- потеря волос (потом они отрастают заново),
- нарушение функциональности ЖКТ, проявляющееся тошнотой и рвотой,
- головокружение,
- диарея,
- отсутствие аппетита и потеря веса на фоне этого,
- появление ран и язв во рту,
- сыпь на коже.
Сильные препараты также вызывают серьезные осложнения. У больной угнетается функциональность системы кроветворения. Количество лейкоцитов и эритроцитов уменьшается, наступает анемия. Возможно развитие почечной недостаточности.
Какие лекарства применяются
Лечение рака яичников надо начинать как можно раньше. Но терапия должна быть максимально эффективной. Среди препаратов для химиотерапии, которые используются при раке яичников, можно выделить такие:
- Авастин,
- Циспластин,
- Карбопластин (используется только для внутривенного введения),
- Цитоксан,
- Циклофосфамид (применяется, если необходимо обеспечить приживание трансплантата, снизить активность иммунитета),
- Гемзар,
- Олапариб,
- Тиотепа,
- Таксол,
- Платинол,
- Циспластин (вызывает уменьшение опухоли),
- Паклитаксил (имеет растительную основу),
- Доцетаксил (полусинтетическое лекарство, произведенное из иголок тиса европейского),
- Оксапиплатин (применяется при метастазировании опухоли, является препаратом второй линии).
Чаще всего применяется политерапия, так как использование только одного препарата будет неэффективным.
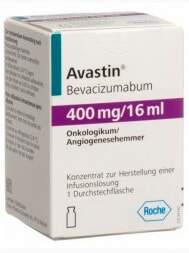
Чаще всего для химиотерапии рака яичников используется препарат «,Авастин»,
Все лекарства можно разделить на 3 группы:
- средства, оказывающие влияние на клеточный цикл,
- препараты, используемые на какой-то определенной стадии,
- цитостатики (угнетающие иммунитет).
Если все возможности для химиотерапии исчерпаны, производится оперативное вмешательство. Эффективность действия лекарств постоянно контролируется. Для этого применяется анализ крови, определяющий уровень белка СА125, а также УЗИ. В первом случае указанное вещество вырабатывается некоторыми злокачественными клетками, а потом начинает циркулировать в кровотоке.
Если пациентка, прошедшая химиотерапию, после обследования узнает, что уровень белка не снизился, значит, лечение не дало результата. Однако этот анализ не всегда полезен. Если изначально уровень белка не был высоким, то использовать его для мониторинга в дальнейшем не имеет смысла.
Также для контроля используется процедура УЗИ. Оно проводится до начала терапии, а также после ее завершения. При успешном лечении размеры новообразования должны уменьшиться.
Терапия при рецидиве и восстановление пациентки
После того как лечение уже прошло и было успешным, болезнь может вернуться снова. Если рецидив рака яичников после химиотерапии случился через 6 месяцев после завершения лечебных мероприятий, то пациентке будет назначен Карбоплатин и Паклитаксел. Если патология появилась снова гораздо раньше, то тут необходима комбинированная терапия, включающая прием таких средств:
- Паклитаксела (еженедельно),
- Доксорубицина,
- Циклофосфамида.
Каждый препарат для химиотерапии подбирается в индивидуальном порядке. Даже речи о самолечении быть не должно. Противораковые средства продаются только по рецепту и имеют чрезвычайно высокую стоимость.
Естественно, после такого испытания защитные силы организма существенно снижаются. Любая инфекция может причинить женщине сильный вред. Патология оказывает негативное воздействие не только на физическое, но и на психическое здоровье. Для реабилитации пациентке придется помощь опытных специалистов.
Следить женщине нужно будет не только за своим физическим состоянием. Важно иметь положительный эмоциональный настрой. Депрессия или апатия только усугубит состояние пациентки. Для того чтобы восстановиться, женщине лучше отправиться в специализированный санаторий. Курс реабилитации включает в себя:
- покой и правильный распорядок дня (после лечения женщине важно много отдыхать, однако посильная нагрузка должна присутствовать),
- укрепление защитных сил (употребление витаминов),
- лечебную физкультуру, а также ванны, занятия плаваньем,
- ароматическую терапию (масла способны укрепить иммунитет),
- нормализацию работы кишечника.
Женщине необходимо наладить свое питание. Пища должна содержать все необходимые витамины, минералы и другие полезные вещества. Однако перегружать желудок нельзя.
Если химиотерапия при раке яичников была начата вовремя, а препараты назначены правильно, то шанс побороть патологию возрастает. Уровень выживаемости также зависит от своевременности оперативного вмешательства. Только правильная и квалифицированная работа врачей обеспечит положительный результат.


- Что такое цитостатики?
- Классификация цитостатиков
- Как действуют цитостатики?
- Область применения цитостатиков
- Показания и противопоказания к применению цитостатиков
- Побочные эффекты цитостатиков
- Механизм действия цитостатиков
- Какие цитостатики назначают чаще всего?
Что такое цитостатики?
Цитостатики повреждают все быстро делящиеся клетки — любые злокачественные и нормальные клетки крови, костного мозга и половых желез. Со временем клеточные клоны вырабатывают устойчивость к цитостатикам, снижая результативность химиотерапии.
Классификация цитостатиков
Все цитостатические препараты разделены на 4 больших группы по механизму действия или происхождению:
- алкилирующие цитостатики, которые запутывают нити ДНК образованием внеплановых связок с ними;
- антиметаболиты внешне очень схожи с человеческими белковыми веществами, участвующими в клеточной жизнедеятельности, но в отличии от естественных, вмешательством своим приводят к клеточной гибели;
- противоопухолевые антибиотики по химическому происхождению такие же антибактериальные препараты, что мы используем для борьбы с воспалением и инфекциями, но на бактериальную флору они не влияют, зато убивают раковые клетки;
- цитостатики растительного происхождения имеют схожесть механизмов повреждения клеточных структур, но главное объединяющее начало — первоначальное их получение из растительного сырья, теперь большинство лабораторно синтезируется.
Гормоны никакого отношения к цитостатикам не имеют, поскольку их действие заключается в антагонизме с натуральными половыми гормонами либо в прямой или косвенной блокаде их выработки. Недостаток гормонов или подмена их антигормоном тоже приводит к клеточной гибели.
Как действуют цитостатики?
В конечном итоге все способы цитостатического воздействия приводят к одному — клеточному апоптозу. Апоптоз закономерный этап клеточной жизни, в отличии гибели при воспалении, инфицировании, некрозе. Это запрограммированная гибель, к ней приходит в своё время каждая клетка, а цитостатики приводят к ней вне программы. Каждый день в организме человека апоптозу подвергается 100 миллиардов клеток, можно считать, что каждые два года клеточный состав организма полностью обновляется. В упрощенном виде апоптоз представляется так:
Область применения цитостатиков
Цитостатики применяются при всех злокачественных опухолях, не исключая заболевания крови и лимфатической ткани, опухоли мозга и половых желез. Циклофосфан и антиметаболиты в несоизмеримо меньших дозах, нежели в онкологии, используются в ревматологии.
У каждого цитостатического препарата свой спектр противоопухолевой активности, к примеру, доксорубицин и фторурацил отлично работают при раке молочной железы, но неэффективны при мелкоклеточном раке легкого. Без фторурацила не обходится химиотерапия карцином кишечника, а доксорубицин бесполезен при них.
Показания и противопоказания к применению цитостатиков
Нельзя применять препараты при заведомой их неэффективности — вне спектра активности.
Временное противопоказание: воспалительные и инфекционные заболевания, остаточные осложнения после предыдущего курса лечения.
Сегодня выбор противоопухолевых средств настолько широк, что не составляет большого труда подобрать оптимальный препарат и даже комбинацию. Тем не менее, при неэффективности, как минимум, двух линий терапии и прогрессивном ухудшении состояния третий вариант химиотерапии не всегда целесообразен.
Побочные эффекты цитостатиков
Токсические реакции обусловлены повреждением нормальных тканей, как правило, очень чувствительны к цитостатикам:
- клетки крови, что клинически проявляется изменением в анализах, чаще всего лейкопенией и нейтропенией, тромбоцитопенией и много реже — анемией;
- костный мозг постепенно замедляет скорость восстановления ростков кроветворения, активная ткань замещается соединительной и жировой, а в анализах крови снижается уровень всех форменных элементов;
- слизистые оболочки реагируют некрозом с отторжением, что проявляется стоматитом, колитом, энтеритом, пневмонитом и воспалением венозного эндотелия;
- половые железы отвечают нарушением сперматогенеза и прекращением менструаций;
- придатки кожи — волосы выпадают, ногти грубеют и меняют свою структуру.
У препарата могут быть не только общие, но и индивидуальные токсические проявления, при которых избирательно погибают нервные клетки или почечные канальцы, гепатоциты или мышечные волокна сердца. Чувствительность к лекарствам очень индивидуальна, спектр и выраженность побочных реакций тоже разняться.
Механизм действия цитостатиков
Два ведущих механизма:
- изменение строения ДНК, в том числе аномальные скручивания, мешающие расходится нитям во время деления, а также нарушения репарации — восстановления непрерывности нити при повреждении;
- разлад клеточного деления — типичное для растительных препаратов нарушение формирования клеточного веретена, разводящего хромосомы в дочерние клетки.
Не только каждая группа, но и каждый цитостатик имеет собственный механизм противоопухолевого действия, а вернее, несколько механизмов повреждения, большая часть из которых неизвестна.
Какие цитостатики назначают чаще всего?
Назначаются только активно работающие при этой злокачественной нозологии и оптимальные в конкретном клиническом случае. Самый широкий диапазон активности у антибиотика доксорубицина, алкилирующих платиновых производных и циклофосфана, растительных таксанов и антиметаболитов фторурацила и метотрексата.
Клинические рекомендации предлагают использовать самые эффективные комбинации лекарств с оптимальным соотношением эффективности и токсичности. В нашей клинике мы подбираем цитостатическую терапию индивидуально — по чувствительности раковой опухоли. Мы не гарантируем отсутствия токсичности, но умеем минимизировать её проявления и ускорять восстановление нормальных тканей.
Читайте также:

