Что за опухоль у таси

Нога в голове: к чему приводит тератома
Находя в телах пациентов опухоли с зубами, волосами и даже отдельными сформировавшимися органами, хирурги далекого прошлого могли запросто обвинить больных в ведьмовстве и сговоре с дьяволом. Сегодня уже давно известно, что такие опухоли — тератомы — возникают из-за нарушения развития половых клеток.
Заболевание протекает бессимптомно в 60% случаев. Проблемы начинаются только тогда, когда тератомы увеличиваются в размерах настолько, что начинают давить на окружающие органы. Беременность считается одним из факторов риска их активизации, они же могут привести к осложнениям при родах.
Наиболее часто встречаются тератомы яичников, также от опухолей страдают дети — у них тератомы образовываются обычно в области головы. В подавляющем большинстве случаев тератомы доброкачественны. Однако, несмотря на изученность, их содержимое не перестает удивлять.
В 2008 году в Колорадо врачи прооперировали малыша всего трех дней от роду. В его мозге была обнаружена маленькая опухоль, от которой было необходимо избавиться. Однако во время операции хирургов ждал сюрприз: в мозге ребенка они обнаружили две ступни, одна из которых была сформирована полностью, а другая частично, а также частично сформированную кисть руки.
в животе мальчика двух недель от роду они обнаружили покрытое волосами новообразование, в котором смогли выделить две ступни, две руки, 15-сантиметровый кишечник, ткани мозга и даже половой член с яичками.
Еще одна опухоль была обнаружена в 1997 году в Германии еще до рождения ребенка, во время УЗИ. Выявив гигантское новообразование в области крестца, врачи пришли к выводу, что для девочки безопаснее будет провести кесарево сечение и операцию по удалению опухоли, чем дожидаться родов. Малышка появилась на свет всего на 29 неделе развития. Масса опухоли составила 4,5 кг, в то время как сама девочка весила всего 950 г.
В тканях опухоли хирурги обнаружили фрагменты костной и хрящевой ткани, полосатых и гладких мышц, сосудов, кишечной оболочки.
Но наиболее поразившей их находкой стал полностью сформировавшийся глаз.
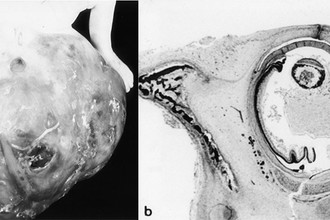
Опухоль была диагностирована как сакрококцигеальная (крестцово-копчиковая) тератома. Среди новорожденных частота заболевания составляет один случай на 35 тыс. детей.
Девочка родилась живой. Но во время операции по удалению опухоли у нее развилась брадикардия и в итоге малышка погибла от сердечной недостаточности.
Опухоль была удалена полностью, после операции вызванные ее давлением на мозг симптомы пропали.
В 2015 году в Бразилии 25-летняя женщина обратилась к врачу с жалобами на боль в нижней части спины, мучившую ее уже два месяца. Первичный осмотр не выявил никаких патологий, в вот УЗИ органов таза показало крупное, 10,3×9,2×8,6 см, образование в области яичника.
После удаления врачи установили, что оно состояло в основном из жировой ткани, но также в опухоли содержались волосы и зубы.
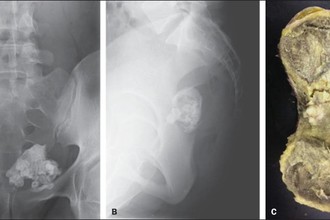
Зубы — не редкость для тератом яичника, они обнаруживаются более чем в трети случаев. Периодически они попадаются даже в археологических находках — так, фрагменты новообразования были найдены среди тазовых костей женщины древнеримской эпохи в Испании. В небольшом шарике среди тазовых костей древней римлянки оказались четыре зуба и кусок кости.
Еще одна тератома яичника с зубами была обнаружена в останках женщины, умершей в XV веке в Португалии. 45-летняя женщина, по всей видимости, умерла от болезни и была похоронена на кладбище в Лиссабоне. Ее останки археологи обнаружили во время раскопок 2010-2011 годов. Наткнувшись на небольшую, 4,3 см в длину, опухоль, исследователи предположили, что это мог быть неразвившийся плод.
Однако более тщательный анализ показал, что опухоль содержит пять почти полностью развившихся зубов — четыре моляра и клык.
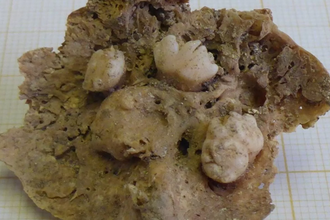
Не похоже, чтобы женщина страдала от опухоли, отмечают исследователи. Судя по тому, что ее скелет не был деформирован, тератома не причиняла ей никаких неудобств.
Тератомы составляют 24-36% от общего количества опухолей у детей и 2,7-7% - у взрослых. Тератомы яичника — одни из самых распространенных, они встречаются в трети случаев, как и тератомы, развившиеся в области крестца. 10-15% опухолей развиваются в забрюшинном пространстве, 5-7% - в яичках, столько же — в области прямой кишки, около 5% — в грудной полости. Тератомы мозга наиболее редки.
- Брюшная полость и брюшина — что это такое?
- Виды рака брюшной полости
- Симптомы
- Осложнения
- Диагностика рака брюшной полости
- Лечение
- Прогноз и профилактика
Брюшная полость и брюшина — что это такое?
Брюшная полость — это пространство в животе, заполненное кишечником и другими внутренними органами. Сверху она ограничена диафрагмой, снизу — тазом, по бокам и спереди — мышцами брюшного пресса, сзади — позвоночником и поясничными мышцами.
Изнутри полость живота выстилает тонкая пленка из соединительной ткани — брюшина. Ее висцеральный листок, покрывает внутренние органы, париетальный — стенки брюшной полости. Между листками брюшины находится замкнутое щелевидное пространство, а в нем — минимальное количество жидкости, выполняющей функцию смазки и обеспечивающей свободное скольжение органов. В некоторых местах брюшина образует складки: брыжейки, на которых подвешены органы, сальники.
Внутренние органы могут быть расположены по отношению к брюшине по-разному:
- Интраперитонеально — покрыты брюшиной со всех сторон.
- Мезоперитонеально — покрыты частично.
- Ретроперитонеально (забрюшинно) — покрыты только с одной стороны.
Виды рака брюшной полости
Первичные опухоли брюшной полости встречаются редко. Они бывают разных типов: мезотелиальные, эпителиальные, гладкомышечные неопределенные. Особая разновидность злокачественных опухолей брюшины — псевдомиксома. Она развивается из клеток, которые продуцируют большое количество желеобразной жидкости. Чаще всего такие опухоли распространяются на брюшину из аппендикса.
Зачастую первичные злокачественные опухоли брюшной полости имеют строение и ведут себя, как рак яичников. Они вызывают сходные симптомы, и врачи применяют для борьбы с ними примерно одни и те же методы лечения.
Известно, что в целом вероятность развития первичного рака брюшной полости выше у женщин, чем у мужчин. Риски повышаются с возрастом. Есть связь между вероятностью развития заболевания и изменениями в генах BRCA1, BRCA2.
При разных типах рака на поздних стадиях опухолевые клетки отделяются от первичного новообразования, распространяются по организму и образуют новые очаги в различных органах, в том числе в брюшной полости. Этот процесс называется метастазированием. Чаще всего в брюшину метастазирует рак толстой и прямой кишки (в 15% случаев), желудка (в 50% случаев), яичника (в 60% случаев), поджелудочной железы. Иногда метастазы распространяются из органов, которые находятся за пределами брюшной полости: молочной железы, плевры (пленки из соединительной ткани, покрывающей легкие и выстилающей стенки грудной полости), легкого.

Симптомы
Зачастую в течение длительного времени симптомы при раке брюшной полости отсутствуют, поэтому нередко его диагностируют на поздних стадиях. Проявления патологии неспецифичны, их можно легко принять за признаки других заболеваний:
- Дискомфорт, спазмы, вздутие живота.
- Повышенное газообразование в кишечнике.
- Жидкий стул.
- Запоры.
- Тошнота.
- Снижение аппетита.
- Частые мочеиспускания.
- Одышка.
- Быстрый набор или потеря массы.
- Кровотечения из прямой кишки, у женщин — из влагалища.
Если канцероматоз брюшины возник в результате метастазирования злокачественной опухоли из другого органа, сильно ухудшается прогноз. Противоопухолевая терапия начинает работать хуже, потому что многие препараты плохо проникают через брюшину.
Осложнения
Главное осложнение данного заболевания — асцит. Этим термином называют состояние, при котором в животе скапливается жидкость. В норме между листками брюшины ежедневно вырабатывается и всасывается около 1,5 жидкости. При канцероматозе нарушается отток лимфы, и жидкость всасывается хуже. Она начинает скапливаться внутри живота.
Пока жидкости немного, больной не испытывает каких-либо симптомов. Затем начинают беспокоить тяжесть, тупые боли в нижней части живота. Затрудняется дыхание, возникает одышка. Из-за того что жидкость сдавливает органы, больной жалуется на отрыжку, тошноту, проблемы со стулом и мочеиспусканием. Живот увеличивается в размерах, может возникать пупочная грыжа. При выраженном асците развивается сердечная недостаточность, отеки.
Диагностика рака брюшной полости
Злокачественную опухоль помогают выявить следующие методы диагностики:
- Ультразвуковое исследование. Зачастую его назначают в первую очередь, как простой, доступный, безопасный и в то же время информативный метод диагностики.
- Компьютерная и магнитно-резонансная томография помогают оценить состояние брюшины и внутренних органов, выявить патологические образования, оценить степень распространения рака.
- ПЭТ-сканирование в настоящее время является золотым стандартом для поиска отдаленных метастазов.
- Биопсия — самый точный метод диагностики злокачественных опухолей. Врач может получить образец опухолевой ткани во время диагностической лапароскопии — процедуры, во время которой через проколы в брюшной стенке в живот вводят миниатюрную видеокамеру и специальные инструменты. Образец отправляют в лабораторию, проводят его гистологическое, цитологическое исследование, молекулярно-генетический анализ. Это помогает не только диагностировать рак, но и установить природу опухолевых клеток, разобраться, какими препаратами с ними лучше бороться.
- Рентгеноконтрастные исследования помогают оценить состояние пищеварительного тракта, выявить опухолевые очаги и другие патологии.
- Анализ на онкомаркер CA-125 (углеводный антиген 125). Уровень этого вещества повышается в крови при раке брюшины и яичников. Но для диагностики этих заболеваний данный анализ недостаточно точен. Как правило, его применяют для контроля течения рака и эффективности лечения.
- Женщины должны пройти осмотр у гинеколога.
Обычно врачи-онкологи устанавливают диагноз на основании таких признаков, как асцит, утолщение брюшины, появление на ней узелков, смещение, сдавление петель кишки, патологические изменения со стороны печени и складок брюшины — сальников.

Лечение
Выбор тактики лечения зависит от локализации, размеров, стадии злокачественной опухоли, количества узлов. Врач также должен учитывать общее состояние больного, его возраст, наличие сопутствующих заболеваний.
Зачастую при поражении брюшины опухолевых очагов очень много, многие из них мелкие, и полностью их удалить невозможно. Хирургическое лечение направлено на удаление как можно большего числа очагов, как правило, оно предшествует химиотерапии. Обычно удаляют матку, яичники, участки кишечника, — словом, всё, что поражено злокачественной опухолью. Если злокачественное новообразование вызывает кишечную непроходимость или другие осложнения, проводят паллиативные хирургические вмешательства.
Для того чтобы уничтожить опухолевые клетки при первичном раке в полости живота, применяют химиопрепараты, зачастую те же, что при раке яичников. Лекарства вводят внутривенно или в брюшную полость — такая химиотерапия называется интраперитонеальной (внутрибрюшинной).
С 2018 года врачи Европейской клиники практикуют инновационный метод лечения канцероматоза брюшины — гипертермическую интраперитонеальную химиотерапию (HIPEC). Суть ее заключается в том, что хирург удаляет все достаточно крупные опухолевые очаги, а затем промывает полость живота подогретым раствором химиопрепарата. Это помогает уничтожить максимальное количество опухолевых клеток и существенно продлить жизнь больного.
При асците наши доктора проводят лапароцентез (прокол в брюшной стенке и выведение жидкости), устанавливают перитонеальные катетеры для постоянного оттока, проводят хирургические вмешательства, которые препятствуют дальнейшему накоплению асцитической жидкости.
На поздних стадиях проводится паллиативное лечение, которое помогает уменьшить симптомы и продлить жизнь больного.

Прогноз и профилактика
Прогноз при первичном раке брюшины напрямую зависит от того, удалось ли удалить все опухолевые очаги во время хирургического вмешательства. К сожалению, зачастую заболевание диагностируют на поздней стадии, поэтому после лечения часто развиваются рецидивы. Обычно пациентам требуется более одного хирургического вмешательства, курса химиотерапии.
Канцероматоз брюшины при метастазах других типов рака резко ухудшает прогноз. Обычно продолжительность жизни таких больных измеряется месяцами. Но HIPEC может ее существенно продлить, до нескольких лет — в случае, если проведение такого лечения возможно у конкретного пациента.
Специальных мер профилактики данного заболевания не существует. Нужно в целом вести здоровый образ жизни, женщинам — регулярно проходить осмотры у гинеколога. Мера профилактики метастазов в брюшину — своевременная диагностика и лечение злокачественных опухолей.
Гепатоцеллюлярная карцинома (ГЦК) занимает примерно 5-е место в структуре всех злокачественных опухолей, а среди злокачественных новообразований печени на ее долю приходится до90%. Поданным 2011 г., заболеваемость ГЦК в Казахстане составляет 5,6 на 100 тыс. населения (до 850 новых случаев в год). Прогноз при данном заболевании весьма неблагоприятный: излечение и выживаемость очень низкие, около 15–20%.
Оснащение клиник Казахстана аппаратами КТ, МРТ, современной УЗИ-аппаратурой за последние 5–7 лет привело к более детальному изучению патологии печени. В связи с введением скрининга на злокачественные новообразования среди лиц с фиброзом/циррозом печени в ближайшее время следует ожидать увеличение количества вновь выявленных случаев рака печени.
Единственным методом, позволяющим добиться длительной выживаемости при ГЦК, является хирургическая резекция или трансплантация печени. К сожалению, по данным онкологического диспансера ЮКО, количество больных с опухолями, поддающимися хирургическому лечению, очень мало: к моменту диагностики радикальное удаление опухоли возможно лишь у 5–15% больных, остальные пациенты подлежат паллиативному лечению. Вероятность развития рецидива опухоли в течение 3–5 лет после радикальной резекции печени очень высока – до 70–90%. Из этого числа пациентов повторную резекцию удается выполнить не более чем в 10% случаев. Таким образом, в настоящее время очевидно, что паллиативная противоопухолевая терапия требуется более чем 80% больных с первичной ГЦК.
Принятая Европейской ассоциацией по изучению печени (EASL) Барселонская классификация по определению стадий и принципов лечения ГЦК представлена на рис. 1. В данной статье рассмотрены аспекты такого действенного, малоинвазивного и эффективного метода локальной терапии при неоперабельной ГЦК, как трансартериальная химиоэмболизация (ТАСЕ). Метод состоит во введении химиопрепарата с эмболизирующим материалом и в устранении притока крови к опухоли путем эмболизации питающего ее кровеносного сосуда. По результатам клинических исследований, уменьшение размеров опухоли после проведения данной процедуры наблюдается у 35–40% пациентов.

Вопрос о количестве процедур ТАСЕ в каждом конкретном случае весьма дискутабелен. Эта проблема обсуждалась, в частности, на одном из недавних конгрессов Европейской ассоциации по изучению печени, и многие авторы склоняются к мнению, что ТАСЕ в процессе лечения больного должна проводиться не менее 3 раз. После проведения первой процедуры проводится оценка онкомаркеров, и при падении их уровня ведется наблюдение за изменениями размера очага при помощи КТ с контрастным усилением. Изменение опухоли в размерах – сигнал для повторного проведения ТАСЕ. Время между процедурами – весьма индивидуальный показатель и зависит от течения заболевания и состояния пациента, в среднем 8 недель.
– паллиативная терапия злокачественной опухоли с целью продлить жизнь больного;
– улучшение качества жизни пациента: купирование болевого синдрома и других симптомов (гормональных кризов, карциноидного синдрома), связанных с новообразованием;
– экстренная эмболизация, когда опухоль осложняется разрывом и кровотечением;
– лечение резектабельного рака у больных, не операбельных в связи с тяжелой сопутствующей патологией;
– химиоэмболизация с целью временного торможения роста опухоли (достижение стабилизации) для продления времени в листе ожидания при подготовке пациента к трасплантации печени.
Противопоказаниями для проведения ТАСЕ являются отсутствие морфологического подтверждения злокачественного поражения, генерализованное распространение опухоли, недостаточные функциональные резервы печени, почек (объем опухоли по данным КТ составляет более 50–70% объема органа, рак на фоне тяжелого сопутствующего цирроза, тромбоз ствола или основных ветвей воротной вены, асцит, желтуха, высокий уровень щелочной фосфатазы и др.).
Все эндоваскулярные вмешательства при лечении новообразований печени делятся на 2 группы: применяемые в комбинации с хирургическим лечением и паллиативные (рис. 2).

ХИПА – химиоинфузия печеночной артерии
ХЭПА – химиоэмболизация печеночной артерии
ХЭВВ – химиоэмболизация воротной вены
ПХЭПА – предоперационная химиоэмболизация печеночной артерии
ПЭВВ – предоперационная эмболизация воротной вены
МХЭПА – масляная химиоэмболизация печеночной артерии
МХЭВВ – масляная химиоэмболизация воротной вены
Метод ХИПА используется для создания кратковременной высокой концентрации химиопрепарата в опухоли с одновременным снижением системной токсичности.
ХЭПА применяется для создания пролонгированной высокой концентрации химиопрепарата и эффекта ишемии в зоне опухоли.
Метод ХЭВВ является дополнением к ХЭПА при необходимости усиления противоопухолевого эффекта.
На сегодняшний день при проведении эндоваскулярных вмешательств хирурги используют 2 основных типа доступа: катетеризация бедренной артерии по Сельдингеру или же доступ через плечевую артерию (рис. 3).

Эмболизирующих материалов существует огромное множество: используют частицы поливинилалкоголя, гемостатическую губку, металлические спирали, липиодол (линойодол), эмбосферы, радиоэмболизацию иттрием-90, различные химиопрепараты. Сегодня широко распространено применение самонасыщаемых гепасфер, имеющих ряд преимуществ при эмболизации: в отличие от масла, которое рассасывается в течение 45 дней, они рассасываются 60–70 дней, обеспечивая пролонгированный эффект от процедуры.
– ХИПА, затем ЭПА;
– смесь химиопрепарата с эмболизатом;
– включение цитостатика в микросферы;
– МХЭПА.
На рис. 4 представлена КТ-картина результатов ТАСЕ. Использование контраста вместе с химиоэмболизатором позволяет длительное время отслеживать размер опухоли. Стойкое невымывание контраста в опухоли является маркером эффективности и точности проведенной химиоэмболизации.

– печеночная и мультиорганная недостаточность;
– нагноение опухоли;
– абсцесс печени;
– острый холангит;
– острый холецистит.
– гастродуоденит;
– панкреатит;?
– окклюзия печеночной артерии;
– инфаркт селезенки.
Частота развития перечисленных осложнений зависит от квалификации, подготовленности и мастерства хирурга: при четких действиях и соблюдении верной технологии осложнения, как правило, не возникают. Гораздо чаще встречается другое осложнение – постэмболизационый синдром, проявляющийся характерным симптомокомплексом: боль в области эмболизации первые 2 суток за счет ишемии, гипертермия и интоксикация вследствие некроза опухоли. Данные симптомы лечатся симптоматически, инфузионной терапией, и в течение 3–5 дней купируются на 100%.
При метастазах колоректального рака наиболее целесообразным и эффективным считается сочетанное использование методов ХЭПА и ХЭВВ, дополняющих друг друга за счет особенностей кровообращения (питания опухоли через воротную вену). Процедура проводится в 2 этапа: венозная эмболизация проводится через 2 недели после артериальной. Доступ к воротной вене осуществляется под контролем УЗИ. Результаты сочетанной терапии представлены на рис. 5, 6.

Обоснование адъювантной (послеоперационной) химиотерапии
Наиболее эффективным методом регионарной терапии при ГЦК и нейроэндокринных метастазах считается МХЭПА, при метастазах колоректального рака – длительная ХИПА и ХЭПА + ХЭВВ, при метастазах рака желудка – ХИПА, ХЭПА.
Среди эффективных методов комбинированного лечения – ПЭВВ как подготовка к радикальной правосторонней гемигепатэктомии и адъювантная химиоэмболизация после радикальных операций с целью повышения выживаемости.
Результаты лечения больных раком печени в Областном онкологическом диспансере ЮКО
За 5 лет (2008–2013 гг.) в нашей клинике с применением ТАСЕ пролечено более 250 пациентов с ГЦК III–IV стадии в возрасте от 32 до 76 лет. Из них проанализированы результаты у 92 больных (пролеченных в 2008–2011 гг.). ТАСЕ проводили стандартно с использованием липиодола и доксорубицина 50–100 мг. Интервал между курсами ТАСЕ составлял 1,5–2 мес.
Частичная регрессия опухоли после 3–6 курсов ХЭПА наблюдалась у 26% пациентов, стабилизация опухоли – в 46% случаев. Прогрессирование ГЦК в процессе лечения с летальным исходом (в течение 6–8 мес) зафиксировано в 28% наблюдений.
Показатели 12-месячной выживаемости больных (все пациенты) составили 60,5%. Показатели 3-летней выживаемости больных класса В по Child-Pugh, стадия А–В по Барселонской классификации, составили 36,9%, класса С по Child–Pugh (ранняя стадия С) – 21,7% (р
Не совсем рак
- Артисты стараются вести здоровый образ жизни, занимаются спортом, отказываются от вредных привычек. И все равно заболевают!
- То, что болеют артисты, просто совпадение. С точки зрения науки нет каких-то профессионально значимых факторов риска развития опухолей, кроме, пожалуй, радиации - в больших дозах.

Алексей Кащеев. Фото: neurology.ru
- Почему вообще появляется глиобластома?
- К этому приводят генетические поломки. То, что выявлять глиобластому стали чаще, связано и с развитием уровня диагностики, и с экологией. Вокруг нас довольно много канцерогенных веществ: в почве, в воде, пище - существует вероятность, что это влияет на развитие опухолей.
Глиома - это опухоль нервной системы, или глиальной ткани. Самый злокачественный вариант глиомы - глиобластома. Глиобластома в отличие от других опухолей (таких, например, как невринома, менингиома) не имеет четких границ. Их не видно на снимках и во время операции. И тотально удалить эту опухоль невозможно. Способа излечиться от нее пока нет.
- Говорят, Анастасии Заворотнюк сделали одну операцию по удалении опухоли в Германии, потом в России - вторую.
- При глиобластоме используются все методы лечения - и хирургию, и химиотерапию, и лучевую терапию. Обычно в комплексе.
- Но если удалили опухоль, почему же болезнь не ушла?
- При глиобластоме генетическая поломка есть в большом количестве клеток. Все клетки мозга так или иначе поражены. И полностью остановить рост пораженных клеток невозможно.

Близкие Анастасии Заворотнюк не говорят о ее диагнозе. Однако, судя по утечкам информации в СМИ, у актрисы именно глиобластома. Фото: Руслан РОЩУПКИН
Тревожные симптомы
- Каковы симптомы глиобластомы?
- Головная боль, симптомы отека мозга - тошнота, рвота, прогрессирующее снижение зрения, нарушение сознания, памяти. Плюс симптомы, связанные с поражением какого-то отдела, когда опухоль давит на жизненно важные центры. В итоге - слабость в конечностях, нарушение речи, функции глотания, потеря сознания. Невролог при появлении таких симптомов, как правило, оправляет пациента на МРТ головного мозга. К счастью, глиобластома - не единственная опухоль центральной нервной системы. Есть много доброкачественных, которые могут быть полностью излечены.
- Известно, что у Монтсеррат Кабалье была опухоль мозга. Но она еще долгие годы выступала.
- Значит, у нее такая была опухоль, которая поддавалась лечению. Она умерла от инсульта и в довольно пожилом возрасте. Онкологические заболевания - вторая по частоте причина смерти после сердечно-сосудистой патологии в России . (В год от всех видов рака в России умирает около 300 тысяч человек, а от болезней, связанных с сосудами и сердцем, - около миллиона. - Ред.)
- Может ли рост опухоли быть связан со стрессами?
- Есть исследования, которые говорят о том, что склонность к канцерогенезу увеличивается при хроническом стрессе. Но нет достоверных данных, доказывающих, что глиобластома растет от стрессов.
Известно, что хронический стресс приводит к развитию целого ряда заболеваний - гипертонии, ишемической болезни сердца, депрессиям, неврозам. В отдельных случаях исследователи связывают рак с перенесенными шоковыми состояниями. Но, с другой стороны, порой стресс и полезен, потому что это тренировка организма.
Диеты и ЭКО
- Читала об исследованиях: мол, люди, которые активно занимаются физкультурой, реже заболевают и чаще излечиваются от рака.
- Если человек уже заболел, его лечение связано не со спортом, а с хирургией, лучевой терапией, химиотерапий. Другое дело, что в принципе здоровый образ жизни, в том числе регулярные занятия физкультурой, могут несколько уменьшать вероятность развития каких-либо онкологических заболеваний. Здоровый образ жизни улучшает общее состояние человека, повышает иммунитет.
- Заворотнюк следила за фигурой. Сидела на диетах. Это влияет?
- Влияют пищевые привычки. Факторы риска рака - это алкоголь, красное мясо, жирная, жареная пища. Эти канцерогены нередко вызывают рак прямой кишки, колоректальный рак (злокачественная опухоль толстого кишечника), рак желудка. Красное мясо рекомендуют есть не чаще раза в неделю.
- Заворотнюк сделала ЭКО, чтобы родить в 47 лет. ЭКО может провоцировать рак?
- Достоверных сведений, что ЭКО влияет на глиобластому, нет. Но ряд врачей полагают, что оно может ускорить развитие рака, если он уже был на какой-то начальной стадии.
Регулярный медосмотр
- Что можно посоветовать людям, чтобы избежать рака?
- Во-первых, вести здоровый образ жизни. Это отказ от курения (или его минимизация), сокращение употребление алкоголя, отказ от употребления большого количества красного мяса, жареных продуктов, регулярные физические упражнения, полноценный отдых и сон.
Во-вторых, регулярно проверять состояние здоровья, сдавать анализы. Для женщин от 40 - 45 лет - регулярный, раз в год, осмотр гинеколога, маммолога . Мужчинам рекомендуют регулярные исследования ПСА маркера рака (в первую очередь предстательной железы). При появлении каких-то новообразований на коже, опухолей, язв (если кожа начала кровить, вести себя необычно), надо сразу обращаться к специалисту.

В ТЕМУ
А может, виноваты травмы головы.
- Задорнов упал во время спуска на горнолыжном курорте и получил сотрясение мозга. На Жанну Фриске напали - ударили по голове (тоже было сотрясение мозга). Хворостовский дрался в молодости. Заворотнюк бил бывший муж. Удары по голове могли спровоцировать опухоль мозга?
- Нет. Опухоли мозга не вызываются черепно-мозговой травмой, - говорит Алексей Кащеев . - От черепно-мозговых травм много других проблем, но рак не входит в их число.
- Заворотнюк сделала не одну пластическую операцию. Пластические операции увеличивают риск заболеть раком?
- Пластические операции никак не влияют на онкозаболевания. Связи рака и применения стволовых клеток тоже не выявлено.
- Но при пластических операциях применяется общий наркоз, говорят, очень вредный, мозгу в том числе.
- Современный наркоз более щадящий, чем тот, который применяли раньше. Современный наркоз безопасен и эффективен. Другой вопрос, что у любой медицинской манипуляции есть осложнения и риски.
- Когда Жанна Фриске болела, ей вводили экспериментальную вакцину.
- Такие вакцины реально продлевают жизнь. Они способствуют контролю над опухолью. Но, повторю, не излечивают полностью.
ГИПОТЕЗА
Угрожает интеллектуалам
У людей с высшим образованием более высок риск развития глиомы (первичной опухоли головного мозга) по сравнению с теми, кто только окончил школу. К такому выводу пришли шведские ученые под руководством Марии Фейхтинг из Института экологической медицины в Стокгольме . Данные своего исследования они опубликовали в издании The Journal of Epidemiology & Community Health.
Медики подсчитали: у мужчин, которые учились в вузе минимум три года, риск развития глиомы на 19 процентов больше, чем у тех, кто после девяти классов не продолжил образование. Этот показатель для женщин составил 23 процента.
Мало того, для мужчин, занятых интеллектуальным трудом, вероятность развития акустической невриномы (вялотекущая доброкачественная опухоль) повышалась на 50 процентов по сравнению с теми, кто занят физическим трудом. А высокий уровень доходов у мужчин увеличивал риск заболеть глиомой на 14%.
Ученые не смогли объяснить причин наблюдаемой ими связи.
- Андрей Львович, неужели опухоль мозга - болезнь умных?
- Я в это не верю. Никаких достоверных сведений на сей счет нет. Это заболевание встречается у людей всех профессий.
- Есть огромное количество других заболевших людей, о которых вы просто не знаете. А знаменитости на слуху, вот и кажется, что они больше подвержены этому недугу.
А КАК У НИХ?
В 2015 году бывший президент США Джимми Картер публично объявил об излечении от рака мозга. Как оказалось, у него была не глиобластома, а опухоль, вызванная метастазами меланомы, затронувшей также печень. Опухоль в печени была удалена, а от опухоли мозга Картера лечили с помощью иммунотерапии. Картер до сих пор жив, ему 94 года.
Алексей Кащеев - врач-нейрохирург отделения нейрохирургии ФГБНУ НЦН (Научный центр неврологии). Преподаватель кафедры нервных болезней и нейрохирургии медицинского факультета Российского университета дружбы народов. Кандидат медицинских наук. Автор 22 научных работ, статей, одного патента на изобретение.
Читайте также:

