Что такое линейный ускоритель в онкологии
Линейный ускоритель – это радиотерапевтический комплекс, который используется для проведения облучения злокачественных новообразований. Системы визуализации и синхронизации с дыханием пациента дают возможность точного дозирования радиации в центре злокачественной опухоли. Инновационные технологии позволяют минимизировать повреждение здоровых тканей, сократить длительность лечения и значительно уменьшить время воздействия облучения.
Линейные ускорители: ощутите разницу
Чем отличается лечение на линейном ускорителе от обычной лучевой терапии? При проведении лучевого облучения на традиционных аппаратах, используется мощное гамма-излучение, которое эффективно разрушает опухоль. Существенным недостатком устаревшей технологии является неуправляемое излучение, которое поражает здоровые ткани и органы, что ведет к инвалидизации и снижению качества жизни онкобольных.
Современные линейные ускорители отличает отсутствие в них радиоактивных элементов. Облучение осуществляется узконаправленными лучами, в месте пересечения которых образуется высокая концентрация радиации на область новообразования. Также различаются способы определения формы и расположения опухоли. Инновационные технологии позволяют формировать участок облучения по форме пораженных тканей, что дает возможность использовать линейные ускорители для лечения онкологии подвижных новообразований при естественном изменении их положения.
Что лечат?
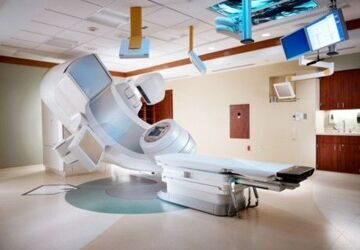
Высокая эффективность методики лучевой терапии доказана в ведущих онкологических центрах Европы, Израиля и России. Лечение линейным ускорителем показано в следующих случаях:
- новообразования молочной железы;
- злокачественные опухоли кишечника и прямой кишки;
- новообразования органов малого таза и поджелудочной железы;
- при лечении опухолей головного мозга;
- злокачественные поражения простаты;
- рак легкого;
- при лечении некоторых видов неопухолевых заболеваний.
Краткий обзор линейных медицинских ускорителей
Линейный ускоритель в медицине – настоящая панацея и дает надежду на выздоровление и улучшение качества жизни более чем 80% больным онкологией. Медико-биологические комплексы радиационной терапии отличаются надежностью и многоуровневыми системами автоматизации:
- Линейные ускорители Varian Clinac производства США в разных модификациях являются основным лечебным оборудованием в ведущих онкологических клиниках мира. На сегодняшний день линейный ускоритель clinac truebeam (True Beam) является безальтернативным по скорости и точности. Это единственная модификация линейного ускорителя, облучение которым позволяет уничтожить новообразование за один сеанс.
- Линейный ускоритель Еlekta Synergy – высокотехнологичный комплекс последнего поколения, позволяющий проводить облучение фотонами и электронами разных энергий. Укомплектован системой 3D визуализации и инновационным программным обеспечением, что помогает точно задать контуры новообразования и оптимизировать размещение пациента до начала лучевой терапии. Радиотерапевтический линейный ускоритель synergy s – это повышенная механическая прочность и точность движущихся систем установки, а также расширенные возможности системы рентгеновской визуализации.
- Линейный ускоритель Primus производства компании Siemens – наиболее технологичное оборудование с компактным дизайном. Сочетает в себе точность терапии, простоту в использовании и непревзойденную надежность. Ускорители Primus являются многофункциональным радиотерапевтическим оборудованием, что позволяет решать различные клинические задачи с учетом финансовых возможностей пациента.
Стоимость лучевой терапии
Линейный ускоритель – цена сопоставима с лечением по устаревшим технологиям. Например, стоимость курса лучевой терапии (10 – 15 процедур) на линейном ускорителе Вариан (Varian) начинается от 100 000 рублей. Цена варьируется в зависимости от объемов подготовительного этапа, стадии заболевания, локализации и формы опухоли.
Радиотерапия - один из основных методов борьбы с целым рядом онкологических заболеваний. Она наносит переродившимся раковым клеткам повреждения, ведущие либо к их немедленной гибели, либо к последующему уничтожению иммунной системой. "В советское время выпускались радиотерапевтические установки типа "Рокус", "Агат" и др. Есть примеры, когда эти устройства эксплуатируется до сих пор. В 80-е годы в СССР начались попытки создания современной ускорительной и др. техники, эти проекты включались в планы НИИ и т.д., однако ничего существенного в итоге не произошло", - сообщил председатель совета директоров "МСМ – Медимпэкс", заведующий кафедры истории медицины Первого МГМУ им. И.М. Сеченова, д. м.н., др. ист.н., профессор Дмитрий Балалыкин.
Дальнейшие события в отечественной онкологии можно назвать драмой (хотя слово трагедия подходит лучше): в 90-е годы отечественная промышленность разваливается, и закупки зарубежной техники становятся мизерными, такая ситуация продолжалась более 10 лет…
Статистика говорит сама за себя
В 2009 г., когда стартовала НОП "Мероприятия по совершенствованию медицинской помощи онкологическим больным" (до 2015 года), смертность от онкологических заболеваний в РФ занимала второе месте, а на учете в онкологических учреждениях состояло 1,8% населения; прирост же заболеваемости раком за истекшее десятилетие – превысил 14%.
"C 60-х годов отечественные онкологи начали оценивать тенденцию заболеваемости, она постепенно растет, причем попытаться как-то увязать это с увеличением продолжительности жизни проблематично", - сообщил руководитель отделения высоких технологий лучевой терапии МНИОИ им. П.А. Герцена, президент российской ассоциации терапевтических радиационных онкологов (РАТРО), д.м.н., проф. Андрей Черниченко.

Андрей Черниченко: Онкозаболеваемость в России постепенно растет, начиная с 60-х годов
Российские цифры выглядят особенно удручающе на фоне статистики в развитых странах: например, с 2001 по 2005 заболеваемость раком у мужчин в США ежегодно снижалась на 1,8% (по данным American Cancer Society).
Заметим, что 2/3 онкологических больных в США проходят сеансы радиотерапии.
Сфокусированное определенным образом невидимое излучение во время сеанса лучевой терапии или радиохирургии проникает вглубь тела пациента. В качестве некой аналогии можно привести оптические приборы, которые фокусируют дневной свет, однако в случае с радиоволнами точка фокуса находится не на поверхности, а в глубине тела пациента – на опухоли.
В процедуру с применением ускорителя или гамма-ножа входит снятие реперных точек на томографе, проверка на фантоме перед началом сеанса, а так же использование в ряде случаев специальной стереотаксической системы для повышения точности координат мишени и мн.др. Ко всему же процессу, в принципе, вполне применимы понятия workflow или "технологическая цепочка".
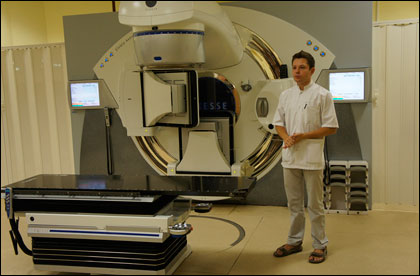
Руслан Шафиулин: Врачи и медицинские физики работают с линейным ускорителем только совместно
Линейный ускоритель отличается от описанного ранее гамма-ножа типом используемого излучения: он разгоняет и направляет поток электронов, сталкивающихся на конце своего пути с промежуточной (технологической) мишенью, в результате чего генерируется рентгеновское излучение. Помимо точной фокусировки в точке опухоли, прецизионного механического вращения рентгеновского излучателя и др. мер, для защиты здоровых тканей применяют регулируемый мультилепестковый коллиматор (лепестки задерживают часть излучения), системы контроля за качеством и количеством излучения во время сеанса и др. Другое характерное отличие от гамма-ножа – более широкая сфера применения ускорителя, то есть его универсальность. Например, Elekta Axesse позволяет проводить как сеансы, лучевой терапии так и радиохирургии, причем различных органов и систем.
Чтобы не вдаваться в технические подробности, разницу между современным прецизионным медицинским ускорителем (со всей необходимой инфраструктурой) и примитивным рентгеновским устройством из прошлого века можно описать как разницу между телегой с лошадью и космической ракетой (хотя, в принципе, и то и другое можно формально отнести к "средствам передвижения"). Она заключается не в конкретных параметрах и общих принципах работы, а в технической реализации устройства, степени соответствия требованиям медиков, технологичности и точности. "Существует мнение, что разница между хорошей и плохой лучевой терапией составляет 2 мм", – считает Дмитрий Балалыкин.
В России должно быть больше техники
Поставляемые в РФ Gamma Knife и Elekta Axesse – это примеры современной онкологической техники среди длинного перечня устройств с разными принципами действия и назначением, разработанных различными производителями (Siemens, Varian, Elekta и др.) и используемых, преимущественно, в развитых странах. Помимо прочего, есть также и некий опыт применения для лечения опухолей ускорителей, используемых в физических экспериментах и др. К 2015 году для реализации НОП современной техникой планируется оснастить все государственные онкологические учреждения. Приказ № 944н Министерства здравоохранения и социального развития РФ от 3 декабря 2009 г. позволяет рассчитать нормативы: в частности, из расчета на 300 тыс. населения должен приходится один аппарат для дистанционной лучевой терапии: линейный ускоритель или кобальтовый источник ионизирующего излучения и т.д. Необходимо заметить, что эти нормативы во много раз меньше, чем в некоторых западных странах, таких, например, как Нидерланды. Тем не менее, "закупка современной техники позволит быстро изменить ситуацию с точки зрения пациентов, решить вопрос доступности современной медицинской помощи", – справедливо полагает Дмитрий Балалыкин.
Другая сторона проблемы – качество. "В рамках НОП мы подготовили стандарты для всех онкологических заболеваний – часть из них утверждена, часть – находится на согласовании" - сообщил Андрей Черниченко. "Стандарты привязаны к реальным текущим возможностям отечественных лечебных учреждений, дифференцированы, в частности, в зависимости от вида оказываемой ими медицинской помощи – высокотехнологичной (ВМП) или специализированной (СМП). Сегодня – это необходимая мера. К примеру, в ряде случаев рак носоглотки в развитых странах лечат исключительно методом IMRT (радиационная терапия модулированной интенсивности). Это подход, однако если ему следовать и запретить использовать устаревшее оборудование 60-ых и 70-ых годов, то придется закрыть примерно половину онкологических отделений и в стране останется около 5-ти медучреждений, которые смогут реализовать) такой стандарт. Действуя же последовательно, можно в итоге добиться того, что вся медицинская помощь у нас станет высокотехнологичной, и можно будет ликвидировать само понятие ВМП".

Дмитрий Балалыкин: Из опыта западных стран можно уже сегодня позаимствовать практику создания частных центров лучевой терапии
"Из опыта западных стран можно уже сегодня позаимствовать практику создания частных центров лучевой терапии. Еще 5 лет назад это казалось немыслимо. Сегодня уже есть 2-3 таких центра, причем очень хорошо оснащенных. В одном из них (в Москве) операция с использованием гамма-ножа обойдется в 250 тыс. руб. Комитет по здравоохранению мэрии Санкт-Петербурга проводит тендеры на оказание услуг по направлению лучевая терапия. В этой форме размещаются заказы в петербургской частной клинике. В форме, помимо прочего, есть гамма-нож и другая современная аппаратура, например, кибер-нож", - рассказывает Дмитрий Балалыкин.
5 сеансов из 10-ти возможных
Высокотехнологичное оборудование отличается тем, что ежедневное число пациентов, которые могут пройти на нем сеанс лечения, относительно невысокое, при этом общее количество современных устройств в РФ явно недостаточно. Например, в России сегодня имеется только один "государственный" кибер-нож и работает всего 6 комплексов Elekta Axesse. Один из которых установлен в МНИОИ им. П.А. Герцена, на нем проводится в среднем 5-6 сеансов в день по направлениям ("квотам") Минздрава, хотя его пропускная способность - 10-15 онкологических больных. Тому есть ряд причин, одна из которых… нехватка пациентов.
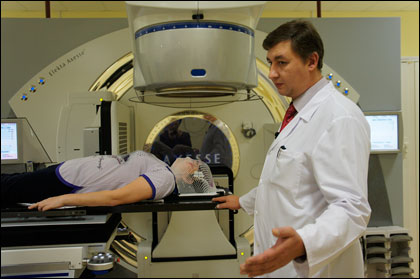
В России есть 6 аппаратов Elekta Axesse, во всем мире их около 30
Одно из применений Elekta Axesse – радиохирургическое. "Она показана 10% больных, нуждающихся в онкологической помощи. Чтобы подвести однократно высокую дозу и моментально излечить больного, мишень должна быть в районе 2-3 см. В ряде случаев помочь больному с помощью Elekta Axesse бывает невозможно", – описал плюсы и минусы Elekta Axesse Андрей Черниченко. Согласно статистике, до начала НОП больше половины больных поступали в учреждения с диагнозом: рак 3-й или 4-ой стадии. Это означает, что шансы на излечение у таких больных не выше 30%. Улучшение оснащенности аппаратурой онкологических учреждений в РФ позволит сократить время до лечения, а ранняя диагностика позволит эффективно задействовать и полностью загрузить выскотехнологичное оборудование.
"Прежде чем территория вступит в программу НОП, она должна наладить диспансеризацию и маршрутизацию пациента, которая начинается с уровня районных больниц, фельдшерско-акушерских пунктов, участковых терапевтов, стоматологов и т.д. Это организационная часть НОП, и она, в ряде случаев, не требует капитальных вложений. Кроме того, поставлена задача повысить степень онкологической настороженности всех медицинских работников для диагностики опухолевых заболеваний на ранних стадиях, когда до 90-95% больных еще могут быть излечены", – сообщил Андрей Черниченко.
Специалисты нового поколения
"В нашей компании сегодня работает 20 медицинских физиков, а это больше, чем во всех федеральных НИИ вместе взятых. Мы участвуем в подготовке таких специалистов совместно с профильной кафедрой физфака МГУ им.М.В.Ломоносова, 4 выпускника этой кафедры работают сегодня в МНИОИ им. П.А.Герцена" – сообщил Дмитрий Балалыкин.
РАТОР выделяет гранты для поддержки исследований и написания кандидатских диссертаций. В апреле этого года (примерно через 100 лет после открытия лучей рентгена) в России выделена новая специальность) – радиотерапия. "31 мая у нас была создана первая в России кафедра онкологии и радиотерапии. Готовится открытие соответствующих направлений в регионах, имеющих соответствующую техническую и научно-практическую базу для обучения; помимо федеральных центров, в рамках НОП оснащены окружные онкодиспансеры в Челябинске, Хабаровске и других городах", – сообщил Андрей Черниченко.
Решением накопившихся в отечественной онкологии проблем (является) не только закупка оборудования, но и организация его полноценной сервисной поддержки на территории РФ (а для этого нужны специализированные инженерные компании), установка, настройка и тестирование перед каждым сеансом, соблюдение регламентов технической поддержки и многое другое. Только наличие квалифицированных кадров позволит оказать высокотехнологичную медицинскую помощь в массовом порядке, повысить пропускную способность имеющегося оборудования и важно для производства современной медицинской техники на территории РФ. "Уровень жизни (крайне дефицитного) российского медицинского физика сопоставим с тем уровнем, который он получит, если уедет работать, допустим, в США или Германию. Если разницы нет, то зачем туда ехать?" – спрашивает Дмитрий Балалыкин.
"В России насчитывается порядка 1200-1300 радиотерапевтов, 65% из них - пенсионеры. Если мы хотим выполнить к 2015 г. НОП, их число надо, как минимум, удвоить", – осветил другую часть кадровой проблемы Андрей Черниченко.

Дмитрий Балалыкин: "Уровень жизни российского медицинского физика сопоставим с тем, который он получит в США или Германии
Подготовка кадров, налаживание массового своевременного онкологического скрининга, возрождение отечественной медицинской промышленности, закупка оборудования для диагностики и лечения (а также всей требующейся для его работы инфраструктуры) в необходимых для оснащения всех регионов к 2015 г. количествах, выделение в этих целях помещений и создание новых центров, выполнение других условий НОП, а также удаление коррупционной "опухоли" из экономики позволит сократить отставание России от западных стран в ближайшие годы, сделать первый шаг на пути, по которому уже давно идут многие страны.
Конкретные же результаты НОП можно будет попытаться оценить, например, посмотрев через несколько лет на аналогичный с приведенным ранее график с российской статистикой онкологических заболеваний.
![]()
НМИЦ онкологии им. Петрова: Из-за рака пациенты теряют лицо![]()
Петербургский врач: Польза МРТ с контрастом превышает вред от возможных осложнений![]()
Пороки клапанов сердца: классические подходы и новые альтернативы
В комплексной терапии онкологических заболеваний используются 4 метода лечения: хирургия, химиотерапия, лучевая терапия, иммунотерапия. Сейчас самое большое финансирование и все внимание брошены на лекарственную терапию. Но со следующего года грядут изменения и в лучевой. А это для Петербурга – самое больное место.
Как говорит профессор Сергей Новиков, заведующий отделением лучевой терапии НМИЦ онкологии им Петрова, за последнее десятилетие лучевая терапия сделала большой рывок и ее стремительное развитие не останавливается. Появились новые аппараты, новые технологии, а с ними — новая идеология лучевой терапии.
- Сергей Николаевич, правда ли, что новые технологии в лучевой терапии когда-то заменят хирургию?
- Во многих случаях это уже происходит. Например, только что мы составляли план лечения пациента с ранним немелкоклеточным раком легкого. У него нет изменений в лимфоузлах, нет метастазирования. Но его невозможно прооперировать из-за сопутствующих заболеваний (перенес инфаркт, инсульт), так что операция угрожает жизни. В этой фактически патовой ситуации лучевая терапия позволяет провести радикальное лечение - мы можем подвести чрезвычайно высокую дозу излучения на очень маленький объем тканей. И это приведет не к продлению жизни, а именно к излечению. Опухоли объемом 1-5 см мы можем облучить, избежав при этом серьезного повреждения окружающих тканей. Это называется стереотаксическая лучевая терапия или радиохирургия.
- Вы имеете в виду лечение с помощью гамма-ножа и кибер-ножа?
- Эти технологии тоже относятся к стереотаксической лучевой терапии — гамма-нож применяют для лечения новообразований на головном мозге, а кибер-нож - для направленного радиотерапевтического воздействия на экстракраниальные опухоли (расположенные вне головного мозга). Но сейчас активно развиваются технологии радиохирургии и стереотаксической лучевой терапии на линейных ускорителях. Их преимущество в том, что это универсальные приборы: на одном аппарате может выполняться - стерео-, радио- или классическая лучевая терапия с избирательным воздействием на опухоль (обычная или 3D-конформная). У нас уже три таких аппарата, каждый из них имеет свои преимущества, а в целом умеют все.
- Для лечения какого вида рака они предназначаются, что умеют?
- Легче перечислить, что не умеют — не умеют облучать очень много очагов в головном мозге одномоментно, в отличие от гамма ножа. Но такая ситуация — редкость, а главное, пока нет доказательств целесообразности такой агрессивной терапии, она не продлевает жизнь.
С другой стороны, эти аппараты могут делать все в области высокотехнологичного облучения, когда требуется радиохирургия: используются в комплексном лечении новообразований в головном мозге, локализованных процессах в легких (немелкоклеточный рак), метастатических поражений легких, печени, надпочечников, костей, мягких тканей и т. д. Благодаря высокой точности направления воздействия, они незаменимы в лечении злокачественных новообразований головы и шеи. Например, опухоль языка — очень тяжелая патология, лечить ее хирургически или невозможно, или очень сложно. После операции пациента берем мы. Активно используем методы брахитерапии и стереотаксической лучевой терапии при раке предстательной железы.
Онкологи сегодня говорят, что иммунотерапия перевернула наше сознание в лечении некоторых видов рака. Но забывают упомянуть, что сочетание иммунотерапии с некоторыми видами лучевой терапии увеличивает эффективность практически в два раза. Поэтому трудно встретить протоколы лечения, в которых рекомендована иммунотерапия без лучевой терапии.
— Да, но для ослабленных и пожилых пациентов мы используем стереотаксис, потому что это неинвазивное - щадящее лечение. С моей точки зрения, пациенты с этим диагнозом должны получать прежде всего лучевую терапию, хотя на протяжении многих лет считалось, что главный способ лечения рака предстательной железы – хирургия. Но простатэктомия сопряжена с риском для жизни, с осложнениями — каждый пятый после хирургического вмешательства страдает недержанием мочи, у 70% перенесших операцию возникает нарушение эректильной функции. Эффективность хирургии, брахитерапии и стереотаксической лучевой терапии с точки зрения борьбы с опухолью одинаковая, в некоторых случаях лучевое лечение даже более результативно. Но недержание мочи после него – редкость, всего 1-2% случаев в сравнении с 20% после хирургического удаления предстательной железы и тут даже использование роботизированных хирургических методов не помогает улучшить результаты. Эректильная дисфункция, к сожалению, может возникнуть и после проведения лучевого лечения - у 30-40% пациентов мы отмечаем снижение эректильной функции. Но, к счастью, это существенно меньше 70-80% после хирургического лечения.
- Однако по-прежнему распространен миф о том, что лучевая терапия опасна, потому что может спровоцировать развитие лучевой болезни.
- Если под лучевой болезнью мы подразумеваем то, что происходит с организмом человека, оказавшегося в эпицентре взрыва ядерной бомбы, то даже в 1970 годы лучевая терапия ее не провоцировала. Другое дело, что когда использовали большие поля для облучения, это вызывало разного рода токсичность — развивались осложнения со стороны органов дыхательной или кроветворной системы, например. Я начал работать в 1980-е, и уже тогда были разработаны методы, которые позволяли избегать фатальной или очень серьезной токсичности. Хотя какие-то неприятности от лучевой терапии были, есть и будут. Например, если мы подводим очень высокие дозы в область опухоли предстательной железы, мы можем вызвать повреждения прямой кишки, если облучаем опухоль в легких, — повреждения легких, в мозге — здоровые ткани мозга. И иногда вынуждены рисковать, потому что понимаем: другой возможности спасти человека нет. Да, бывает, лучевая терапия балансирует между добром и злом, но зачастую альтернативы нет. Например, при метастазах в головном мозге — это пациенты, которым часто нейрохирурги уже помочь не могут, возможности химиотерапии, нередко, исчерпаны. А лучевая терапия у таких пациентов ассоциируется с 20-30% риском возникновения лучевого некроза. Но в оставшихся 70-80% случаев есть шанс, что мы поможем пациенту преодолеть на определенное время его проблемы.
- Стереотаксическая лучевая терапия – не самая распространенная технология в Петербурге, возможности для ее применения есть только у двух федеральных специализированных клиник и у одной негосударственной. Часто ли она востребована?
- Когда у нас только появился первый аппарат для стереотаксиса, мы пролечили всего 12 пациентов. Это была, можно сказать, эксклюзивная методика - все отделение собиралось смотреть. А в этом году стереотаксическую лучевую терапию получили уже 350 пациентов, то есть около 20% получивших лучевое лечение в НМИЦ онкологии им. Н.Н. Петрова.
- Парадокс: при том, что в Петербурге можно получить самые современные виды лучевой терапии, петербуржцев направляют на лучевое лечение в клиники, в которых их нет. Более того, на 2020 год из средств петербургского фонда ОМС выделяется 1 млрд рублей на 3D-конформную терапию, выполнять которую в городских специализированных клиниках, можно сказать, не на чем.
- Только кто и на каком оборудовании будет ее проводить? В городских медицинских учреждениях нет современных ускорителей. Да и старые регулярно выходят из строя.
- Мы сражаемся за то, чтобы петербуржцы могли получать современное эффективное лучевое лечение. Но НМИЦ им. Петрова не может принять всех, хотя пока мы никому не отказывали.
Что касается стереотаксической лучевой терапии, которая есть в единичных клиниках Петербурга, мы примерно на 30% увеличиваем объемы ежегодно. И готовы взять на себя столько пациентов, сколько нужно. Поскольку у нас стереотаксическая лучевая терапия проводится на тех же аппаратах, на которых проводится и классическая, чтобы освободить их от загрузки стандартной 3D-конформной лучевой терапией, мы приобрели еще один линейный ускоритель, на котором и будем ее выполнять.
- В Городском онкологическом центре в Песочном и в Городском онкологическом диспансере недостаточно современных линейных ускорителей, на которых можно проводить 3D-конформную лучевую терапию. И мне кажется, что на аппаратах, которые там есть, невозможно использовать сложные технологии, например, радиохирургическое лечение и стереотаксическую лучевую терапию. Поэтому важно, чтобы руководители городской онкологической службы наладили сотрудничество с федеральными учреждениями, частными клиниками, которые готовы и могут помочь петербуржцам.
Конечно, нужно обновлять парк оборудования. Потому что на аппаратах 2001-2005 года, которые морально устарели, а многие уже сняты с производства, можно выполнять паллиативную лучевую терапию, использовать простые методики облучения, но современные достижения радиационной онкологии на них недоступны.
У городских клиник есть рентген-терапия, которой, кстати, у нас нет, в онкодиспансере есть интраоперационный ускоритель, которого больше нет ни у кого в нашем городе.
Задача - дать пациентам возможность получать все существующие на сегодня виды лучевой терапии по показаниям: простую, когда ее достаточно, сложную, когда она необходима. Понимаете, если у мужчины выявили рак предстательной железы, и он попадает в учреждение, где нет аппаратов для проведения стереотаксической лучевой терапии, нет брахитерапии, то, на мой взгляд, он адекватной помощи в этих учреждениях получить не сможет. Потому что если будут подведены достаточно большие дозы на устаревших линейных ускорителях, серьезно вырастут осложнения, если дозы будут меньше, чем необходимы для борьбы с опухолью, то лечение не будет эффективным. Да, часть пациентов выздоровеет, но меньше, чем тот процент, который мог бы и должен был выздороветь. А пациенты, которым можно провести более простую лучевую терапию, должны лечиться там, где она есть, - нет смысла направлять их в НМИЦ онкологии.
То есть Петербургу нужна грамотная маршрутизация. Но это очень болезненный вопрос для городских властей. Тут все должны понимать, что его нужно решать, и мы к этому готовы.
- До сих пор федеральные клиники лечили, конечно, петербуржцев, но – по федеральным квотам. И объясняли это тем, что тарифы ОМС на лучевую терапию слишком малы. А количество квот всегда ограничено.
- Те тарифы, что действуют в системе ОМС сейчас, рассчитаны на ту простую лучевую терапию, что есть в городских клиниках. Мы работаем в рамках программы ВМП, потому что используем технологии, которых нет в городских медучреждениях. Программа ВМП рассчитана на то, что люди могут получить помощь там, где ее могут оказать. И ее финансирование было достаточным, чтобы применять в лечении сложные технологии: закупать дорогие расходники, заниматься техническим обслуживанием оборудования. Теперь, насколько я знаю, запланированные на 2020 год тарифы петербургского фонда ОМС эквивалентны тарифам, действующим в программе ВМП.
- На 1 миллиард рублей запланировано 4 тысячи курсов 3Д-конформной терапии. 4 тысячи пациентов ее получат – это много или мало?
- Немало, но 4 тысячи курсов это не 4 тысячи пациентов. Потому что некоторым приходится проводить их повторно. Например, прошла женщина курс терапии по поводу опухоли в молочной железе, но обнаружился метастаз в лимфоузле или в другом месте, его тоже нужно облучать. Я думаю, что это 3-3,5 тысячи пациентов.
Для сравнения: в НМИЦ онкологии в год лучевую терапию получают 2 тысячи пациентов. Приблизительно столько же - РНЦРХТ им. Гранова. Эту помощь могут оказывать в частных клиниках МИБС и есть один современный ускоритель и аппараты для брахитерапии в ПСПбГМУ им. Павлова. То есть в городе можно выполнять лучевую терапию любой сложности. Важно, чтобы средства были потрачены на ее эффективные методы.
- Люди по-прежнему едут за рубеж, чтобы получить лечение радиоактивным йодом. Почему в России оно до сих пор дефицитное, а в Петербурге его и вовсе нет?
- Это не сложная технология, но для ее применения у нас действуют очень строгие требования, вплоть до строительства специальных очистных сооружений. Чтобы выполнить все, что нужно по нормативам, надо выиграть большое сражение, но сначала вложить в его подготовку огромные деньги. Сейчас предпринимаются усилия, чтобы сделать наше законодательство более демократичным — смягчить требования для применения этой технологии. А мы уже фактически готовы к тому, чтобы использовать ее, даже обсуждаем возможность открытия коек для пациентов, нуждающихся в терапии радиоактивными источниками. Эта терапия — это огромная перспектива на будущее.
Сегодня это, в первую очередь, радиойодотерапия или паллиативная терапия при метастазах в кости - она позволяет сделать комфортной жизнь человека, страдающего от болевого синдрома. Это то, к чему мы уже сегодня готовы. Но есть еще много методик использования радиоактивных источников. Например, лечение препаратами, мечеными лютецием, — это широкий круг препаратов, которые избирательно накапливаются в опухоли и уничтожают ее. То есть это один из вариантов целенаправленной терапии.
- Магической пули, которая бьет только в цель пока нет. И при таргетной терапии избирательность условная, и при стереотаксическом — какая-то доза облучения все же приходится на здоровые ткани и они могут пострадать. Но все же воздействие современных лучей и химиотерапии, действительно, выигрывает в эффективности и точности направленного действия.
- Что нужно сделать, чтобы в лучевой терапии новые технологии появлялись не только в федеральных клиниках? Закупать новые аппараты?
- Я счастлив, что лучевая терапия в нашей стране начала осознано развиваться. Но это огромная машина, она не сдвинется с места мгновенно. Чтобы ее раскрутить, нужно потратить много сил и времени, грамотно использовать финансовые вложения.
То есть миллиарды сначала должны вкладываться не в оборудование, а в людей. Их нужно учить, в том числе за границей, нужно обеспечить их достойным заработком. А когда будут люди, способные работать на современном оборудовании, тогда и нужно его покупать.
- Сколько всего аппаратов для лучевой терапии работают у вас?
- Четыре ускорителя - от самого простого до самого сложного, и еще два аппарата – для брахитерапии. Плюс много компьютерных планирующих систем, задача которых сделать лучевую терапию максимально точной.
Читайте также: