Что такое химиотерапия при остеогенной саркоме
Остеосаркома (или остеогенная саркома), которую еще иногда не совсем правильно называют раком кости, — самая распространенная злокачественная опухоль костной системы.
Некоторые цифры и факты:
- В большинстве случаев остеосаркому диагностируют в молодом возрасте — от 10 до 30 лет.
- Наиболее высока распространенность заболевания среди подростков, но это не означает, что не могут заболеть люди другого возраста.
- Каждый десятый случай остеогенной саркомы встречается у людей старше 60 лет.
- Среди прочих онкологических заболеваний остеосаркома встречается редко. У детей она составляет 2% от всех видов рака, у взрослых — еще меньше.
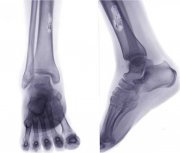
Чаще всего остеосаркома встречается там, где находятся зоны роста — ближе к концам длинных трубчатых костей. Излюбленные места локализации опухоли: область колена (нижний конец бедренной и верхний конец большеберцовой кости), верхняя часть плечевой кости. Намного реже встречаются поражения других костей: таза, челюстей и др. Редкие локализации в большинстве случаев обнаруживают у людей старшего возраста.
Почему возникает остеосаркома?
Точные причины возникновения опухоли не известны. Но существуют некоторые факторы риска:
- Возраст. В группе максимально высокого риска подростки и молодые люди, у которых кости интенсивно растут.
- Рост. Обычно люди, у которых возникает саркома, имеют рост выше среднего.
- Облучение костей. Риски повышены у людей, которые перенесли курс лучевой терапии высокими дозами, особенно если это было в детстве. Влияние рентгенографии и компьютерной томографии не доказано.
- Некоторые заболевания костей: болезнь Педжета, множественная наследственная остеохондрома.
- Некоторые наследственные патологии: наследственная ретинобластома, синдром Ли-Фраумени, синдром Ротмунда-Томсона, синдром Блума, синдром Вернера.
Среди факторов риска для многих онкозаболеваний большое значение имеют особенности образа жизни: масса тела, вредные привычки, характер питания, физическая активность. Можно сказать, что остеосаркома — в данном случае исключение. Для того чтобы образ жизни внёс свою лепту в возникновение злокачественной опухоли, должны пройти десятилетия, а рак костей, как мы уже знаем, наиболее распространен среди молодых людей.
Симптомы остеосаркомы
Чаще всего встречается остеогенная саркома бедренной и большой берцовой кости — в области коленного сустава. Типичный симптом заболевания — упорные боли в суставе, кости. Иногда они постоянные, а иногда то стихают, то нарастают. Болевые ощущения могут усиливаться по ночам, во время физической активности (при ходьбе, беге, занятиях спортом). Если поражена нога, человек начинает хромать.
Дети, особенно маленькие, физически активны, они часто падают, ударяются, поэтому у них первые симптомы остеосаркомы легко спутать с травмой. У взрослого человека, особенно если он не занимается спортом и тяжелым физическим трудом, подобные проявления сразу должны насторожить и стать причиной для визита к врачу.
Какие выделяют стадии остеосаркомы?
Существуют разные классификации, чаще всего врачи определяют стадию остеосаркомы в соответствии с системой MSTS. Учитывают три показателя:
- G — степень озлокачествления. Может быть низкой (G1), когда ткань опухоли похожа на нормальную, и более агрессивной высокой (G2), в которой клетки практически полностью утратили первоначальные черты.
- T — степень распространения опухоли. Она может находиться в пределах кости (T1) или прорастать в соседние ткани (T2).
- M — наличие метастазов. M0 — метастазов нет, M1 — есть.
Другая классификация — AJCC, она учитывает распространение первичной опухоли (T), метастазы в ближайших лимфатических узлах (N), метастазы в других частях тела (M) и степень озлокачествления (G).
Методы диагностики
По симптомам можно только заподозрить рак кости или другое заболевание. Для того чтобы получить точный диагноз, врач назначит обследование, которое может включать:
- Рентгенографию. Быстрый и простой метод диагностики, в некоторых случаях помогает сразу констатировать опухоль. Если есть подозрение на метастазы в легких, проводят рентген грудной клетки.
- Магнитно-резонансная томография (МРТ) и компьютерная томография (КТ) помогают более детально рассмотреть опухоль, обнаружить прорастание в соседние ткани.
- Позитронно-эмиссионная томография. В организм вводят слабое радиоактивное вещество в безопасных дозах, которое сильнее всего накапливается в опухолевых клетках. Затем делают снимки. Это позволяет не только рассмотреть основную опухоль, но и обнаружить метастазы в разных частях тела.
- Общий и биохимический анализы крови. Применяют как дополнительный метод диагностики, чтобы оценить общее состояние человека. Также они могут косвенно указывать на степень агрессивности опухоли.
- Биопсия. Самый точный метод диагностики. Её применяют всегда, даже если другие исследования уже убедительно показывают, что у пациента есть рак кости. Биопсия помогает установить окончательный диагноз, отличить остеосаркому от других опухолей, определить степень озлокачествления. Врач может взять образец ткани при помощи иглы или через разрез.

Как проводят лечение остеосаркомы?
Лечение остеосаркомы состоит из трех этапов.
Начинают с курса предоперационной, или неоадъювантной, химиотерапии. В среднем он продолжается 10 недель. Назначают комбинацию нескольких препаратов — это помогает усилить эффект. Задачи неоадъювантной химиотерапии: уменьшить размер остеосаркомы и уничтожить метастазы. Благодаря предоперационной химиотерапии и современным химиопрепаратам, выживаемость при остеосаркоме в последние годы значительно улучшилась.
Затем следует хирургическое лечение. В прошлом единственным выходом была ампутация пораженной руки или ноги. Современные хирурги чаще всего могут обойтись удалением части кости или сустава. Их можно заменить на специальный протез и практически полностью восстановить функцию конечности. Операции при остеосаркоме стали более щадящими.
Послеоперационный курс химиотерапии (адъювантная) нужен для того, чтобы удалить раковые клетки, которые могли остаться в организме после хирургического вмешательства. В среднем он продолжается 18 недель, иногда дольше.
Как лечить рецидив остеогенной саркомы? В целом схема лечения примерно та же — операция, курс химиотерапии. После рецидива прогноз намного хуже, но все еще есть шанс на выздоровление.
Прогноз при остеосаркоме
Прогнозы для онкобольных выстраивают на основе особого показателя — пятилетней выживаемости. Он обозначает процент пациентов, которые остались живы в течение пяти лет с момента установления диагноза. Конечно, многие живут и дольше. Пять лет — условный рубеж, после которого можно с достаточно высокой вероятностью предполагать, что человек выздоровел.

Наиболее благоприятен прогноз в случаях, когда опухоль локализованная — то есть не успела распространиться по организму и может быть полностью удалена во время операции. Пятилетняя выживаемость составляет 60–80%, а если опухоль чувствительна к современным таргетным препаратам — до 90%.
Если есть метастазы остеосаркомы, прогноз сильно ухудшается. Пятилетняя выживаемость падает до 15–30%. Но она может быть выше, в пределах 40%, если:
- рак успел распространиться только в легкие;
- все метастазы можно обнаружить и удалить.
Метастазы остеосаркомы чаще всего обнаруживают в легких, реже в костях, головном мозге и других местах.
Зачастую прогноз ухудшается из-за того, что человек не обратил внимания на первые симптомы и не посетил вовремя врача. Если есть хотя бы малейшее подозрение на рак, если возникли любые необычные симптомы — лучше сразу перестраховаться и пройти обследование. Иногда от этого зависит жизнь. Запишитесь на прием к врачу-онкологу, звоните:
Химиотерапия – это лечение лекарственными препаратами, направленное на уничтожение раковых клеток. У пациентов с ранней стадией остеосаркомы целью химиотерапии является уменьшение размеров опухоли определяемой радиологическими методами, ее уничтожение, уменьшение риска рецидива заболевания, который может произойти в результате попадания в легкие или другие органы раковых клеток, оторвавшихся от первичной опухоли. У пациентов с поздней стадией остеосаркомы (метастатической) целью химиотерапии скорее является не спасение, а регресс заболевания и увеличение продолжительности жизни.
И хотя при низкой степени остеосаркомы химиотерапия у некоторых пациентов считается не нужной, у большинства пациентов она входит в состав лечения. Химиотерапия, как правило, проводится до операции (до 12 недель) и после (почти год).
Еще до начала химиотерапии доктор может порекомендовать установку венозного порта в центральную вену для того, чтобы в последующем брать на анализы кровь и внутривенно вводить лекарственные препараты через катетер порта, а не использовать каждый раз периферическую вену.
При больших размерах опухоли, делающих ее неоперабельной, применяют химиотерапию, направленную на уменьшение размеров (неоадъювантная химиотерапия). В большинстве случаев лечение проводится в следующем виде: четыре разных препарата вводятся одновременно и несколько препаратов вводятся последовательно. Предпочтение отдают, так называемой схеме Т10, содержащей высокие дозы метотрексата. На двенадцатой неделе этого лечения, как правило, планируют операцию. Это лечение проводят как с целью уменьшения размеров опухоли, а значит и облегчения ее хирургического удаления, так и с целью уничтожения клеток, которые могли попасть в удаленные части организма, а значит уменьшения риска рецидивов. В большинстве случаев после хирургического лечения еще в течение одного года продолжают химиотерапию (особенно при получении хорошего ответа на лечение, оцениваемого по результатам патоморфологического исследования операционного материала). Главным фактором, определяющим успешность лечения является количество живых опухолевых клеток. Если содержание живых клеток менее 10%, то риск рецидива очень низкий.
Другим вариантом является лечение цисплатином и адриамицином, когда часть химиопрепаратов вводят с помощью специального радиологического метода (ангиографии) через артерию, питающую опухоль, а другую часть – внутривенно. Подобное лечение может проводиться с центрах имеющих большой опыт в этой области командой врачей, имеющей схожую профессиональную философию. В работах, проведенных после 2000-х г.г. были получены в высшей степени обнадеживающие результаты в отношении интраартериальной химиотерапии.
В одной из статей, опубликованных в Журнале Ортопедического Общества, было показано, что интраартериальная химиотерапия, применяемая до хирургического лечения (напрямую в опухоль через питающую ее артерию) увеличивает продолжительность жизни у молодых пациентов с остеосаркомой.
Остеосаркома – вид рака, исходящий из костной ткани и встречается достаточно редко. В нашей стране по данным статистики остеосаркома встречается также редко. Ежегодно ожидается 150-200 новых случаев у лиц молодого возраста. Как и при большинстве видов раковых заболеваний ранняя постановка диагноза и правильное лечение делает возможным полное выздоровление. Абсолютное большинство пациентов с остеосаркомой лица мужского пола в возрасте от 10 до 25 лет, что является преимуществом в процессе лечения и выздоровления с точки зрения сопротивляемости организма, возраста, переносимости химиотерапии. После установления диагноза остеосаркома стандартную терапию определяют с учетом стадии или распространенности заболевания. В случае локализации рака в конечностях при отсутствии распространения на другие области организма при стандартном подходе химиотерапия, предшествующая хирургическому лечению обеспечивает максимально возможное уменьшение размеров опухоли. Благодаря этой терапии, носящей название неоадъювантной, во время операции становится возможным полное удаление опухоли. Кроме того, это лечение позволяет уничтожить попавшие в отдаленные от первичной опухоли части организма раковые клетки и уменьшить в будущем вероятность распространения рака в другие органы, например, легкие. После операции, до выздоровления пациента, проведение химиотерапии невозможно. В тот период возрастает риск распространения упущенных из виду во время операции единичных раковых клеток по организму, в результате чего возникает риск рецидива заболевания. Поэтому неоадъювантная химиотерапия, проводимая до хирургического лечения играет важную роль в выздоровлении пациента. Кроме того, пациенты, у которых получен полный ответ, а именно в послеоперационном материале которых в результате патоморфологического исследования не найдены раковые клетки, это самые долгоживущие пациенты. Другими словами, у них отсутствует опухоль в месте операции, уничтожены возможно попавшие в другие части организма единичные раковые клеток, которые нельзя было определить с помощью на различных методов визуализации.
Классическая химиотерапия применяется внутривенно. Однако успехи интраартериальной химиотерапии заставили повернуть исследования в этом направлении. Химиотерапия метод лечения, при котором химиотерапевтические препараты из венозного русла распространяются по всему организму и уничтожают раковые клетки. При интраартериальной химиотерапии препараты вводятся через артерию, обеспечивая тем самым лучший доступ химиопрепаратов к раковым клеткам. А это значит, что уничтожается большее количество раковых клеток. Одно из клинических исследований, проведенных в последние годы доказывает положительный эффект данного метода.
Была оценена эффективность неоадъювантной интраартериальной химиотерапии у 62 пациентов в возрасте 22 года и моложе, у которых было локальное заболевание без распространения в другие органы и ткани. Исследование имело обнадеживающие результаты, наблюдающиеся побочные эффекты переносились пациентами хорошо.
В результате этого исследования ученые получили данные о том, что неоадъювантная химиотерапия, применяемая интраартериально увеличивает продолжительность жизни пациентов. Полученные результаты не только демонстрируют онкологическому сообществу прогресс в лечении остесаркомы в виде увеличения продолжительности жизни пациентов, они также дают надежду нашим пациентам.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Лечение саркомы – это комплекс методов, направленных на оказание комплексного терапевтического эффекта.
До недавнего времени, единственным действенным методом лечения саркомы считалось хирургическое лечение. Но, на сегодняшний день существует множество других методов, позволяющих вылечить саркому любой локализации и на любой стадии развития. Давайте рассмотрим основные методы, используемые при лечении саркомы.
Хирургическое лечение саркомы
Методика предполагает удаление новообразования оперативным методом. В зависимости от размеров опухоли и ее локализации, может проводиться полостная операция, резекция или лапароскопия. Так, если саркома находится в головном мозге, врачи проводят трепанацию черепа для удаления саркомы. Если саркома поразила кишечник, то онкологи проводят полостную операцию, удаляя пораженный орган и соседние с ним ткани, которые также могут быть поражены.
Удаление саркомы
Удаление саркомы – это хирургический метод лечения злокачественного новообразования. Различают несколько видов удаления саркомы, которые зависят от локализации новообразования.
Применяется в том случае, если хирург 100% уверен в отсутствии метастазов. После такого лечения, используют химиотерапию и лучевое облучение. Частота рецидивов саркомы после локального удаления, составляет 90%
Хирург иссекает не только саркому, но и соседние ткани, расположенные на расстоянии 3-5 см от опухоли. Рецидивы после такого удаления злокачественного новообразования встречаются в 30-50% случаев.

[1], [2], [3], [4], [5], [6], [7]
Представляет собой удаление саркомы в пределах анатомической области. Подобное лечение сравнивают с ампутацией. После такого лечения, используют протезирование, имплантацию, пластику и резекцию. Послеоперационные дефекты устраняют с помощью аутодермопластики. Рецидивы заболевания возникают в 20% случаев.
Представляет собой тотальное удаление пораженной конечности или органа и окружающих его тканей. Рецидивы возникают в 5-10% случаев.

[8], [9], [10], [11], [12], [13], [14], [15], [16]
Химиотерапия при саркоме
Химиотерапия при саркоме – это один из самых важных этапов в лечении онкологических заболевания. Как правило, химиотерапию используют после хирургического лечения. Лечение с использование препаратов позволяет предупредить метастазирование и полностью уничтожить раковые клетки. В некоторых случаях, химиотерапию могут проводить перед операцией, это позволяет уменьшить объемы саркомы.
Данный метод представляет собой лечение с помощью препаратов. Химиотерапия очень эффективна при остеосаркоме, рабдомиосаркоме и саркоме Юинга. Очень часто онкологи сочетают лучевую терапию и химиотерапию для достижения лучшего лечебного эффекта. Единственные недостаток данного метода в том, что препараты действуют на весь организм, вызывая множество осложнений и ужасных побочных эффектов.
Многих пациентов, которым назначают химиотерапию, пугают возможные побочные эффекты (выпадение волос, рвота, тошнота, развитие лейкопении). Но необходимо понимать, что цена побочных действий – это жизнь и здоровье. В некоторых случаях, побочные эффекты удается уменьшить, а то и вовсе избежать. Для этого, схему лечения применения препаратов для химиотерапии должен составлять опытный онколог. Эффективность химиотерапии саркомы зависит от достоверных сведений о природе злокачественных клеток.

[17], [18], [19], [20], [21], [22], [23], [24]
Данный вид лечения представляет собой направленную химиотерапию. Вводимые препараты влияют только на пораженные раковые клетки. Это довольно эффективный метод, так как позволяет не затрагивать здоровые клетки.
Лучевая терапия
Данные метод лечения саркомы используется через 4-6 недель после хирургического лечения и предполагает лечебный курс в 2-3 месяца. Лучевая терапия представляет собой пучок протонной энергии, которая действует на место локализации опухоли, уничтожая раковые клетки и предупреждая метастазирование.
Лечение саркомы в Израиле
Лечение саркомы в Израиле это популярная практика избавления от онкологических заболеваний и злокачественных новообразований. Израиль – это страна с высокими технологиями и многолетней успешной практикой лечения раковых заболеваний. Давайте рассмотрим основные преимущества лечения саркомы в Израиле.
- Хирургическое лечение саркомы проходит с использованием щадящих методик. Благодаря этому, есть возможность сохранить пораженный орган и восстановить его функции. Особой популярностью пользуется микрохирургия, с помощью которой можно пересадить мышечные ткани, восстановить работу пораженных органов и обеспечить эстетичный вид прооперированной части тела.
- Использование современных методик радиотерапии. Данный метод существенно повышает эффективность лечения любого вида саркомы. Курс радиотерапии может занимать от 2 до 3 месяцев. Лечение проводится как до хирургического вмешательства, так и после него.
- Таргентные методы лечения. Терапия позволяет воздействовать препаратами прямиком на источник поражения и эффективно устранять его. Таргетная терапия намного эффективнее химиотерапии и не оставляет после себя губительных побочных симптомов, что также очень важно.
Успехи лечения злокачественных опухолей в Израиле – это гарантия жизни и здоровья, а также надежда современной онкологии. Израильские клиники принимают на лечение не только своих граждан, но и пациентов с других стран, оказывая лечение на самом высоком уровне.
Лечение саркомы в Германии
Лечение саркомы в Германии отличается высокой эффективность и успешностью. Немецкие онкологические клиники располагают всеми возможными методами точной диагностики, что гарантирует высокую эффективность лечения. В лечении сарком, онкологи используют комбинированные методики, которые позволяют добиться эффективного результата. Преимущества лечения саркомы в Германии:
- Применение высокотехнологичного оборудования и самых эффективных лекарственных препаратов.
- Работа профессионального, квалифицированного персонала.
- Немецкие клиники сотрудничают с ведущими онкологическими центрами по всему миру.
Лечение саркомы в Германии характеризуется комплексным подходом к проблеме. Программу лечения разрабатывает группа профессиональных врачей – хирурги, химиотерапевты, морфологи, специалисты по лучевой терапии. Главное правило, которого придерживаются немецкие онкологические клиники – стремление к надежному результату и применение органосберегающих методов.
Народное лечение саркомы
Народное лечение саркомы – это методы народной медицины, которые складывались на протяжении многих столетий. Народное лечение злокачественных новообразований не имеет ничего общего с общепризнанной медицинской практикой и зарекомендовавшими себя методами лечения. Рецепты народной медицины основаны на лекарственных свойствах трав. Давайте рассмотрим несколько рецептов народного лечения саркомы.
- Из алоэ можно сделать лекарственную настойку, которая будет оказывать лечебное действие на весь организм. Итак, возьмите 5-6 больших листов алоэ и положите на сутки в холодильник. После этого, растение необходимо порезать на небольшие кусочки и залить 500 мл спирта или водки. Настойка должка постоять 14-20 дней, в темном прохладном месте, при этом, каждый день банку с настойкой нужно встряхивать. Принимать настойку по одной ложке перед каждым приемом пищи, но не чаще трех раз в сутки.
- Настойка из прополиса также обладает целебными свойствами, и согласно народной медицине, может помочь вылечить саркому. Для настойки вам понадобится 100 г измельченного прополиса и 300 мл водки. Залейте растение водкой, закройте крышкой и взбалтывайте в течение часа. После этого настойку отправляют на неделю в темное место, ежедневно встряхивая банку. Через неделю настойку необходимо процедить и принимать по 10-15 капель, разбавляя в стакане воды, три раза в сутки.
- Возьмите 20-50 г березовых почек и залейте их 100-150 мл водки. Настойка настаивается 15-20 дней, каждый день ее необходимо встряхивать. Как только лечебная настойка настоялась, ее необходимо процедить. Настойку наносят на марлю и накладывают на пораженный саркомой участок тела 2-3 раза в сутки.
- Приготовьте 15-20 г коры дуба и 1000 мл водки. Залейте кору водкой и поставьте на огонь. Варите 30-40 минут, постепенно добавляя 4 ложки меда. После этого отвар нужно процедить и использовать как средство для смачивания повязок. Повязки нужно наносить на пораженный участок тела, то есть на приблизительное место локализации саркомы.
- Соберите пучок свежих листьев подорожника, хорошенько промойте их и выдавите из них сок. Сок можно пить, а можно смачивать и наносить на повязки, прикладывая к пораженному злокачественной опухолью месту.

[25], [26], [27], [28], [29], [30]
Питание при саркоме
Питание при саркоме играет важную роль. Так как правильное сбалансированное питание позволяет ослабить болезненную симптоматику злокачественной опухоли и укрепить иммунную систему. Больные, которым диагностировали саркому, должны питься дробно, 5-6 раз в день, чтобы поддерживать нормальное функционирование организма.
Читайте более подробно о диете при раке здесь.
При саркоме рекомендуется употреблять:
- Свиную, говяжью и куриную печень, сливочное масло и молочные продукты, овощи и фрукты – данные продукты содержат много витамина А, который является антиоксидантом и ускоряет процесс регенерации клеток.
- Орехи и каши, макароны, свиное мясо – эти продукты обогащают организм витаминами группы В, которые повышают сопротивляемость к инфекциям и нормализуют работу всех органов и систем.
- Плоды шиповника, черной смородины, калины, а также сладкий перец, киви, капуста брокколи, цитрусовые и шпинат – богаты витаминов С. Витамин принимает участие в формировании соединительной ткани, выводит токсины и яды из организма.
Вредные и противопоказанные продукты:
- Мучное, сладкое и высококалорийные блюда должны быть под запретом. Это объясняется тем, что пища, богатая углеводами увеличивает риск онкологических заболеваний.
- Люди, употребляющие жаренную и жирную в пищу, рискуют стать обладателями саркомы.
- Злоупотребление соленой, острой и горячей пищей – это одна из причин саркомы желудка.
Лечение саркомы зависит от размеров опухоли, степени поражения, наличия метастазов, стадии саркомы и общего состояния организма. Все это, в комплексе с лечебными методами, позволяют сделать прогноз, относительно выживаемости больного после саркомы.
Злокачественные опухоли костей в структуре заболеваемости злокачественными новообразованиями занимают менее 1 % у взрослых и 7-10% у детей.
Наиболее часто встречаются саркомы семейства Юинга, остеосаркома, хондросаркома, злокачественная фиброзная гистиоцитома кости.
Первичная опухоль (Т)
ТХ — первичная опухоль не оценена.
Т0 — первичная опухоль отсутствует.
Т1 — опухоль 8 см и менее.
Т2 — опухоль 8 см и более.
ТЗ — первичные множественные опухоли кости.
Регионарные лимфоузлы (N)
NX — лимфоузлы не оценены.
N0 — отсутствие метастазов в регионарных лимфоузлах.
N1 — метастазы в регионарных лимфоузлах.
Отдаленные метастазы (М)
MX — недостаточно данных для оценки отдаленных метастазов.
М0 — нет отдаленных метастазов.
M1 — отдаленные метастазы.
M1а — легкое.
M1b — другие локализации.
Степень дифференцировки (G)
GX — не может быть оценена.
G1 — высокодифференцированная (низкая степень злокачественности).
G2 — умеренно дифференцированная (низкая степень злокачественности).
G3 — низкодифференцированная (высокая степень злокачественности). G4 — недифференцированная (высокая степень злокачественности).
Внимание: саркома Юинга и примитивные нейроэктодермальные опухоли (PNET) всегда G4.
В табл. 9.46 приводится группировка опухолей костей по стадиям.
Таблица 9.46. Группировка злокачественных опухолей костей по стадиям

Остеосаркома
Регистрируется около 700-900 новых случаев в год, отмечается бимодальный пик во зторой-третьей и шестой декадах жизни, встречается в 2 раза чаще у лиц мужского пола и составляет 45 % всех первичных злокачественных опухолей костей.
Локализуется преимущественно в метафизах трубчатых костей — дистальная часть бедренной кости, проксимальная часть большеберцовой кости и проксимальная часть плечевой кости (три наиболее часто встречающиеся локализации, расположены по мере убывания частоты встречаемости), в 90% случаев характеризуется выраженным чягкотканным компонентом.
Первичная причина неизвестна, более чем в 90% отмечается делеция гена Rb, из вторичных необходимо отметить экспозицию радием, предшествующую лучевую терапию, болезнь Педжета, другие доброкачественные опухоли костей.
Для классификации и стадирования используется система, общая для злокачественных опухолей костей, — AJCC (TNM) и MSTS (Enneking).
Диагностика остеосаркомы проводится по следующим характеристикам.
Клинические признаки — возраст, локализация, анамнез и данные объективного осмотра (болевой синдром, горячая, твердая — каменистой плотности опухолевая масса и, редко, патологические переломы).
Рентгенологическая оценка: на этапе обследования целесообразно выполнить рентгенографию пораженной кости, сцинтиграфию костей скелета для выявления костных метастазов, компьютерная томография (КТ) зоны первичной опухоли (для детальной визуализации костных структур), магнитно-резонансная томография (МРТ) для визуализации мягкотканного компонента и костномозговых структур, рентгенографию и КТ грудной клетки для исключения метастатического поражения легких.
Ангиография не используется в качестве метода диагностики, но очень информативна для оценки степени ответа опухоли на предоперационную химиотерапию (XT).
Патоморфологическая верификация: в большинстве случаев толсто игольная биопсия позволяет поставить патоморфологический диагноз, в редких случаях используется трепан- или открытая биопсия. Биопсия должна выполняться в специализированных учреждениях, в которых есть группа по лечению сарком, и в идеале тем же хирургом-ортопедом, который будет впоследствии выполнять хирургический этап лечения. Зона биопсии должна быть удалена вместе с первичной опухолью, что крайне важно и критически влияет на отдаленные результаты всего комплексного лечения.
Ранее 2-летняя выживаемость больных с остеосаркомой, получивших только хирургическое лечение, составляла 5-20%, что связано с очень высоким процентом метастазирования в легкие и кости. Эти данные стимулировали проведение рандомизированных исследований с использованием адъювантной XT, которые показали значительное преимущество по всем онкологическим показателям по сравнению с только хирургическим подходом.
В настоящее время стандартом лечения считается комплексный подход с использованием предоперационной (неоадъювантной) химиотерапии, хирургического лечения и адъювантной химиотерапии. Использование предоперационной XT дает возможность выполнять органосохраняющие операции в 80-90% случаев, при этом можно оценить эффективность режима XT in vivo для правильного выбора схемы адъювантной терапии, что позволяет в 50-80% случаев добиться полного излечения пациентов в результате комплексного лечения.
Xимиотерапию используется на пред- и послеоперационном этапах. При достижении IV степени лечебного патоморфоза (более 90% некротизированных клеток) удается значительно увеличить показатели общей выживаемости. Предоперационная XT проводится, как правило, в течение 3-4 мес. перед хирургическим лечением. Выбор режима послеоперационной XT проводится по данным гистологического исследования удаленного материала.
К наиболее эффективным препаратам относятся цисплатин, доксорубицин, ифосфамид, метотрексат в высоких дозах.
Для лечения остеосарком используются комбинированные режимы химиотерапии или монохимиотерапия в высоких дозах (ифосфамид 14 г/м2).
1. Проведение 3-4 курсов предоперационной XT с использованием следующих режимов. Доксорубицин — 90 мг/м2 96-часовая инфузия по 22,5 мг/м2 в сутки в 1-4-й день. Цисплатин — 120 мг/м2 внутриартериально (только при первичной опухоли) или в/в в 6-й день. Интервал между курсами 28 дней.
2. Через 1 мес. после завершения предоперационной XT выполняется оперативное вмешательство.
3. Оценка степени лечебного патоморфоза и послеоперационная химиотерапия.
Если количество некротизированных клеток в операционном материале составляет 90% и более, рекомендуется проведение еще 3-6 курсов (зависит от достижения кумулятивной дозы доксорубицина 800 мг/м2 при использовании инфузионного варианта введения) послеоперационной XT по прежней схеме. При невозможности дальнейшего использования цисплатина рекомендуется переход на схему: доксорубицин 75 мг/м2 72-часовая инфузия + ифосфамид 2,5 г/м2 3-часовая инфузия в 1-4-й день на фоне месны.
Если количество некротизированных клеток в операционном материале составляет менее 90%, рекомендуется переход на альтернативный режим XT. Альтернирующий режим по следующей схеме.
Высокодозный метотрексат — 12 г/м2 в/в с лейковорином 1 раз в 2 нед. в течение 8 нед. Данный режим введения должен использоваться в соответствии со специально разработанным протоколом введения в специализированныхучреждениях.
Далее через 3 нед. после окончания 2-го курса по схеме:
Ифосфамид — 2 г/м2 3-часовая инфузия + месна 100% по схеме в 1-5-й день.
Доксорубицин — 75 мг/м2 72-часовая инфузия.
Колониестимулирующий фактор (КСФ) (филграстим и т.п.) — 5 мкг/кг п/к в 6-16-й день.
Интервал между курсами 3 нед.
Далее повторение всего цикла (4 курса метотрексата, 2 курса ифосфамида с доксорубицином) и в завершение 4 курса метотрексата.
Проведение этого высокоэффективного комплексного лечения возможно только в специализированных медицинских учреждениях.
Подходы к лечению метастатического процесса существенно отличаются при метастатическом поражении легких и костей. Проявление болезни в костях свидетельствует о крайне плохом прогнозе. При наличии первичной опухоли и метастатического поражения легких у пациентов, ранее не получавших специфического лечения, должна применяться тактика, направленная на излечение, а не с паллиативной целью.
Так, при хорошем ответе на предоперационную химиотерапию возможно выполнение полной метастазэктомии, при этом безрецидивная и общая выживаемость могут составлять более 30%. Таким пациентам должно проводиться комплексное лечение, как и при локализованных формах.
При появлении симптомов болезни более чем через 6 мес. после комплексного лечения возможно повторное использование ранее применявшихся схем.
Большинство пациентов после комбинированного лечения уже получали 4 наиболее эффективных схемы XT, стандартов в лечении диссеминированного процесса нет.
Наилучшие результаты показала схема IE:
Ифосфамид — 1800 мг/м2 в/в 3-часовая инфузия в 1-5-й день + месна 120% по схеме.
Этопозид — 100 мг/м2 в/в в 1-5-й день.
КСФ — 5 мкг/кг п/к в 6-16-й день.
Интервал между курсами 3 нед.
В настоящее время продолжают изучать эффективность комбинации гемцитабина и доцетаксела при диссеминированных остеогенных саркомах. По данным II фазы исследования, эффективность этого режима составляет до 30%.
Гемцитабин — 675 мг/м2 в/в 90-минутная инфузия в 1-й и 8-й дни.
Доцетаксел — 75 мг/м2 в 8-й день.
КСФ — 5 мкг/кг п/к в 9-19-й день.
Интервал между курсами 3 нед. (каждые 21 день).
Хондросаркома
Хондросаркома — вторая по частоте саркома костей.
Большинство пациентов старше 40 лет, только 4% пациентов моложе 20 лет.
Локализация: таз — 30%, бедро — 20% и плечевой пояс — 15%. Хондросаркома — наиболее частая злокачественная опухоль лопатки и грудины.
Основная симптоматика появляется за счет механического сдавления окружающих тканей. При жалобах пациента на болевые ощущения в области образования, которое выглядит как энхондрома, следует предполагать наличие хондросаркомы.
Выделяют три основных подтипа:
Классическая хондросаркома (G1-3)
Классические хондросаркомы химиорезистентны, и единственным методом лечения является хирургический. Они представлены в основном образованиями I-II степени злокачественности. Классические хондросаркомы III степени злокачественности метастазируют в 75 % случаев. В настоящее время эффективных режимов XT для лечения классических хондросарком не существует.
Мезенхимальная хондросаркома
Мезенхимальная хондросаркома характеризуется мелкоклеточным компонентом, химиочувствительна, является редкой, высокозлокачественной опухолью, в основном наблюдается у молодых пациентов, поражает плоские кости, 10-летняя выживаемость составляет 28%. Тактика лечения своеобразная — хирургическое удаление и послеоперационная химиотерапия (режимы, как при саркоме Юинга/PNET). Может отвечать на лучевую терапию.
Дедифференцированная хондросаркома
Дедифференцированная хондросаркома химиочувствительна. Дедифференцированный компонент, как правило, представлен остеосаркомой или злокачественной фиброзной гистиоцитомой, для лечения используются соответствующие режимы полихимиотерапии (ПХТ). Отмечается 100%-е метастазирование в течение 12 мес. после постановки диагноза и практически 100%-я летальность в течение 24 мес. При использовании адъювантной ПХТ 5-летний безрецидивный период, по данным разных авторов, составляет до 45%.
Злокачественная фиброзная гистиоцитома кости
Данный гистологический подтип выделен отдельно в начале 1970-х годов. Нередко является компонентом дедифференцированной хондросаркомы и очень часто компонентом остеосаркомы. Этот подтип относится к высокозлокачественным опухолям костей, и тактика лечения не отличается от остеосарком. При этом более чем в 50% случаев удается добиться некроза опухолевых клеток более 90% после проведения предоперационной XT (медиана выживаемости составляет 66 мес).
Режимы XT при остеосаркоме, мезенхимальной дедифференцированной хондро-саркоме и злокачественной фиброзной гистиоцитоме кости следующие.
Доксорубицин — 90 мг/м2 в/в 96-часовая инфузия по 22,5 мг/м2 в сутки в 1-4-й день.
Цисплатин — 120 мг/м2 внутриартериально (только при первичной опухоли) или в/в в 6-й день.
Интервал между курсами 3 нед.
Высокодозный метотрексат 12 г/м2 в/в с лейковорином 1 раз в 2 нед. в течение 8 нед. Данный режим введения должен использоваться в соответствии со специально разработанным протоколом введения в специализированных учреждениях.
Ифосфамид — 2 г/м2 3-часовая инфузия + месна 120% по схеме в 1-5-й день.
Доксорубицин — 75 мг/м2 72-часовая инфузия.
КСФ (филграстим и т. п.) — 5 мкг/кг п/к в 6-16-й день.
Интервал между курсами 3 нед. (начало следующего курса на 21-й день).
Ифосфамид — 1800 мг/м2 в/в в 1-5-й день + месна 100% по схеме.
Этопозид — 100 мг/м2 в/в в 1-5-й день.
КСФ — п/к в 6-16-й день.
Интервал между курсами 3 нед. (начало следующего курса на 21-й день).
Гемцитабин — 675 мг/м2 в/в 90-минутная инфузия в 1-й и 8-й дни.
Доцетаксел — 75 мг/м2 в 8-й день.
КСФ — п/к в 9-19-й день.
Интервал между курсами 3 нед. (начало следующего курса на 21-й день).
Саркома Юинга и примитивные нейроэктодермальные опухоли
Саркома Юинга — высокозлокачественная мелкокруглоклеточная опухоль костей, составляет 15-20% всех первичных опухолей скелета. Чаще всего наблюдается во второй декаде жизни.
Локализация: таз/крестец — 20%; проксимальные конечности: бедренная кость — 21 %, плечевая кость — 10%; дистальные конечности: большеберцовая кость — 11 %. локтевая кость — 14%; другие локализации: ребра — 7%, позвонки — 5%, лопатка — 4%, другие кости — менее 2%.
До начала эры химиотерапии 5-летняя выживаемость составляла менее 10 % и летальность в течение первого года после постановки диагноза — более 50%.
По определению, это высокозлокачественное (G4) системное заболевание, т.к. в 100% случаев, даже при наличии только первичной опухоли, есть отдаленные микрометастазы.
Классифицируется и стадируется стандартно, по AJCC, хотя для саркомы Юинга аудирование используется редко, при этом выделяется IVA стадия при метастазах в легких и 1VB — при поражении других костей, что связано с гораздо худшим прогнозом. Редко встречаются экстраоссальные формы саркомы Юинга, тактика их лечения не отличается от классических.
Клинически наиболее часто представляет собой мягкотканное образование пораженной зоны, и, как правило, пациенты жалуются на непродолжительный болевой синдром. Часто наблюдается слабость, потеря массы тела, лихорадка (чаще у пациентов с диссеминированным процессом), лейкоцитоз. Диссеминированная стадия встречается в 15-50% случаев на момент обращения.
Диагностические исследования необходимо начинать с рентгенографии грудной клетки для исключения метастатического поражения, рентгенографии первичной опухоли, а также КТ/МРТ первичной опухоли и грудной клетки. Сцинтиграфия костей скелета необходима для исключения костных поражений. Для исключения метастатического поражения костного мозга можно выполнить МРТ позвоночника, т.к. наиболее часто метастазы в костном мозге определяются в телах позвонков.
Положительные факторы прогноза:
■ возраст менее 16 лет;
■ преобладание костного компонента: 5-летняя выживаемость до 87 %, а при преобладании мягкотканного — всего 20%;
■ первичная опухоль дистальных конечностей (длинных трубчатых костей);
■ нормальная активность лактатдегидрогеназы (ЛДГ) в сыворотке крови;
■ отсутствие видимого метастатического поражения; я полный ответ на XT.
В настоящее время используется комплексный подход в лечении этой группы сарком. Один хирургический метод дает не более 10% отдаленных результатов, что связано с исходным наличием микрометастазов. В прошлом десятилетии активно использовалась комбинация лучевой терапии (суммарная очаговая доза (СОД) 50 Гр, выживаемость 16-25% при непосредственной эффективности 44-86%) и XT (непосредственная эффективность 80% при поражении дистальных отделов конечностей, 60-80% — проксимальных отделов и таза).
Сейчас лучевая терапия активно заменяется органосохраняющими операциями, которые в ряде случаев позволяют добиться лучших результатов в комбинации с химиотерапией. Лечение должно проводиться в специализированных лечебных учреждениях, занимающихся лечением данной группы заболеваний, т.к. только при комплексном подходе можно добиться излечения 60-70% пациентов.
У большинства пациентов с метастатическим поражением удается достичь полного ответа, однако практически у всех, и в особенности с наличием костных метастазов, возникнет рецидив заболевания и быстрый смертельный исход. При отсутствии видимого исходно метастатического поражения и первичной локализации опухоли в длинных трубчатых костях удается добиться излечения в 60-70% случаев.
Эффективные препараты в лечении саркомы Юинга (при использовании в монотерапии): циклофосфамид — 50%, доксорубицин — 40%, ифосфамид — 32%, винкристин — 30%, дактиномицин — 33%, этопозид — 30%, цисплатин — 7%.
Наиболее эффективны режимы XT с включением винкристина, доксорубицина и ифосфамида (VAI) или циклофосфамида (VArdiaC) с добавлением дакарбазина (CyVADIC) или без него.
В качестве индукционной (предоперационной) XT используется альтернирующий режим химиотерапии:
Ифосфамид — 1800 мг/м2 в/в в 1-5-й день + месна по схеме.
Этопозид — 100 мг/м2 в/в в 1-5-й день.
Далее через 3 нед. переход на схему:
Циклофосфамид — 1200 мг/м2 в/в в 1-й день.
Доксорубицин — 75 мг/м2 в/в в 1-й день.
Винкристин — 2 мг ЕД в/в в 1-й день.
Интервал 3 нед. и далее снова режим с ифосфамидом.
На предоперационном этапе проводится 4-6 курсов XT по указанной схеме; затем, после оперативного вмешательства, при хорошем лечебном патоморфозе проводится адъювантная XT по этой же схеме. Общая продолжительность лечения составляет до 12 мес.
Режимы химиотерапии при саркоме Юинга/PNET (для нелеченных пациентов)
Ифосфамид — 2,5 г/м2 3-часовая инфузия в 1-4-й день + месна 100% по схеме.
Доксорубицин — 75 мг/м2 72-часовая инфузия.
Винкристин — 2 мг ЕД в/в в 1-й день.
КСФ (филграстим и т. п.) — в 5-15-й день.
Интервал между курсами 3 нед.
Циклофосфамид — 600 мг/м2 в/в в 1-й день.
Винкристин — 1,4 мг/м2 (максимальная доза 2 мг) в/в еженедельно в течение 6 нед., далее в 1-й день каждого цикла.
Доксорубицин — 60 мг/м2 в/в 96-часовая инфузия через центральный венозный катетер (15 мг/м2 в сутки) в 1-4-й день.
Дакарбазин — 1000 мг/м2 в/в 96-часовая инфузия вместе с доксорубицином в одном флаконе (250 мг/м2 в сутки) в 1-4-й день.
Дозы должны быть разделены на четыре 24-часовые инфузии, это связано со стабильностью разведенных растворов. Интервал между курсами 3-4 нед.
Ифосфамид — 1800 мг/м2 в/в в 1-5-й день + месна 100% по схеме.
Этопозид — 100 мг/м2 в/в в 1-5-й день, далее через 3 нед. переход на альтернирующую схему:
Циклофосфамид — 1200 мг/м2 в/в в 1-й день.
Доксорубицин — 75 мг/м2 в/в в 1-й день.
Винкристин — 2 мг ЕД в/в в 1-й день.
Интервал 3 нед., далее снова режим с ифосфамидом.
Режимы XT при саркоме Юинга/PNET (при прогрессировании после комплексного лечения)
При позднем прогрессировании (более 12 мес.) возможно повторное использование ранее применявшихся режимов. Некоторую эффективность показали ингибиторы топоизомеразы I, этопозид, алкилирующие агенты, производные нитрозомочевины и цисплатин.
Также возможно применение доксорубицина в высоких дозах (90 мг/м2) в виде 96-часовой инфузии или ифосфамида 2000 мг/м2 3-часовая инфузия в 1 -7-й день, общая доза 14 г/м2, на фоне месны у пациентов, получавших ранее эти препараты в стандартных дозах, и если не выбрана кумулятивная доза доксорубицина. Однако повторные ответы на XT крайне редки, а продолжительность жизни после рецидива заболевания измеряется неделями.
Читайте также:

