Что образуется при взаимодействии железа с хлором
Реакция взаимодействия железа с хлором.










Уравнение реакции взаимодействия железа с хлором:
Железо взаимодействует с хлором. Реакция взаимодействия железа с хлором представляет собой сгорание железа в атмосфере хлора.
2Fe + 3Cl2 → 2FeCl3 (t = 200-300 °C).
Реакция железа с хлором протекает при условии: при предварительном нагревании железа до температуры 200-300 °C.
В результате реакции происходит образование хлорида железа (III).
В ходе реакции железа с хлором при стандартных условиях выделяется тепловая энергия (теплота) 798,8 кДж .
Термохимическое уравнение этой реакции имеет следующий вид:
2Fe + 3Cl2 = 2FeCl3 + 798,8 кДж; ΔH = -399,4 кДж/моль.
Таким образом, реакция железа с хлором носит экзотермический характер.










- ← Реакция цинка с серой
- Реакция цинка с водой →
- Концепция инновационного развития общественного производства – осуществления Второй индустриализации России на период 2017-2022 гг. (105 890)
- Экономика Второй индустриализации России (101 445)
- Программа искусственного интеллекта ЭЛИС (22 628)
- Метан, получение, свойства, химические реакции (15 890)
- Мотор-колесо Дуюнова (15 099)
- Гидротаран – самодействующий энергонезависимый водяной насос (14 456)
- Природный газ, свойства, химический состав, добыча и применение (13 932)
- Крахмал, свойства, получение и применение (13 498)
- Прямоугольный треугольник, свойства, признаки и формулы (13 057)
- Целлюлоза, свойства, получение и применение (11 903)
- Пропилен (пропен), получение, свойства, химические реакции (11 647)
- Этилен (этен), получение, свойства, химические реакции (11 162)
- Бутан, получение, свойства, химические реакции (9 843)
- Оксид алюминия, свойства, получение, химические реакции (9 362)
- Оксид железа (III), свойства, получение, химические реакции (9 133)
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.

Хлорид железа (III), хлорное железо, также - трихлорид железа. FeCl3 — средняя соль трёхвалентного железа и соляной кислоты.
Содержание
- 1 Физические свойства
- 2 Методы получения
- 3 Химические свойства
- 4 Применение
- 5 Безопасность
Физические свойства

Мерцающие, черно-коричневые, либо темно-красные, либо фиолетовые в проходящем свете, зеленые в отраженном свете листочки с металлическим блеском. Сильно гигроскопичен, на воздухе превращается в гидрат FeCl3· 6H2O — гигроскопичные жёлтые, по другим источникам желто-коричневые кристаллы, хорошо растворимые в воде (при 20 °C в 100 г воды растворяется 91,9 г безводной соли). Tпл 309 °C.
Методы получения
- Самым простым методом получения трихлорида железа является действие на железные опилки или раскалённую железную проволоку газообразным хлором. При этом, в отличие от действия соляной кислоты, образуется соль трёхвалентного железа — выделяется бурый дым из мельчайших её частиц:
- Также трихлорид получается при окислении хлором хлорида железа (II):
- Также существует достаточно интересный метод окисления оксидом серы (IV):
- Другим способом получения трихлорида железа (FeCl3) является взаимодействие
оксида железа(III) с соляной кислотой, сопровождающееся выделением воды и энергии в виде тепла:
Fe2O3 + 6HCl → 2FeCl3 + 3H2O + Q↑ 
Химические свойства
- При нагревании в атмосферном давлении до температуры плавления начинается медленное разложение трихлорида железа с образованием дихлорида и молекулярного хлора:
- За счёт того, что трихлорид железа является сильной кислотой Льюиса, он вступает во взаимодействие с некоторыми другими хлоридами, при этом образуются комплексные соли тетрахлороферратной кислоты:
- При нагревании до 350 °C с оксидом железа(III) образуется оксохлорид железа:
- Соли трёхвалентного железа являются слабыми окислителями, в частности, трихлорид железа хорошо окисляет металлическую медь, переводя её в растворимые хлориды:
- реагирует с иодоводородом:
Применение
Безопасность
Хлорид железа (III) является токсичным, высококоррозионным соединением. Безводная соль служит осушителем.

Свойства железа и его соединений
Железо — химический элемент восьмой группы, четвёртого периода, следовательно, строение его атома можно изобразить схемой:
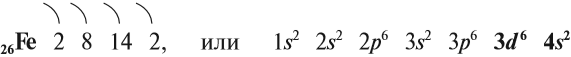
Железо — очень распространённый элемент периодической системы. Среди химических элементов, которые входят в состав Земной коры, оно занимает четвёртое место. В центре Земли имеется массивное железно-никелевое ядро, которое обеспечивает естественный магнетизм Земли.
Хотя атом железа в соединениях может проявлять степени окисления +2, +3, +6, в природе встречаются соединения преимущественно трёхвалентного железа:
- Fe2O3 — гематит (красный железняк);
- Fe2O3 · FeO — магнитный железняк;
- Fe2O3 · Н2О — бурый железняк.
Железо — серебристо-белый пластичный металл. Это металл средней активности, тем не менее оно может реагировать с активными неметаллами (галогены, кислород, сера, углерод), кислотами, а при особых условиях — с водой. При этом если реакция происходит с сильным окислителем, то образуется соединение трёхвалентного железа. Впрочем, если в результате реакции образуется соединение двухвалентного железа, то на воздухе это соединение быстро окисляется до трёхвалентного состояния. Например, с сильным окислителем хлором образуется хлорид Fe (III):
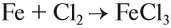
А при взаимодействии с соляной кислотой, атом хлора которой может проявлять только восстановительные свойства, образуется хлорид железа (II).
Задание 11.1. Составить уравнение реакции взаимодействия железа с серой, водой, соляной кислотой, разбавленной азотной кислотой.
Соли железа (II) и (III) имеют разную окраску: растворы соединений железа (II) бесцветные, а растворы железа (III) — окрашены в жёлтый цвет.
При взаимодействии с щелочами из растворов солей железа можно получить его гидроксиды. Они так сильно отличаются друг от друга по цвету, что эту реакцию можно считать качественной на соединения железа с разной степенью окисления. Так, из солей Fe (II) выделяется белый (в инертной атмосфере) осадок, который на воздухе мгновенно зеленеет:
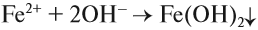
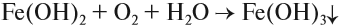
Наиболее чувствительной качественной реакцией на Fe 3+ является реакция с роданидом калия:
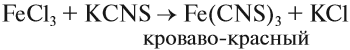
Оксид и гидроксид железа (II) проявляют основные свойства, т. е. реагируют с кислотами, но не реагируют со щелочами. В отличие от них, оксид и гидроксид железа (III) проявляют слабые амфотерные свойства. Это означает, что при обычных условиях эти вещества реагируют с кислотами и не реагируют со щелочами, но при сплавлении они со щелочами реагируют:
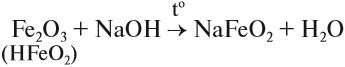
Кроме того, они растворяются в горячих, концентрированных растворах щелочей.
Таким образом, на примере свойств соединений железа ещё раз убеждаемся в справедливости закономерности: при возрастании степени окисления атома металла усиливаются и кислотные, и окислительные свойства соединений.
Задание 11.2. Составьте уравнение реакции гидролиза хлорида железа (III).

Получение железа (чугуна и стали)
Производство чугуна основано на восстановительных свойствах углерода. Чугун образуется в домнах, куда загружают смесь кокса и железной руды. В результате горения кокса образуется необходимое для реакции тепло и сильный восстановитель — угарный газ:
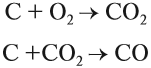
Впрочем, и кокс является прекрасным восстановителем:
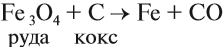
Угарный газ является основным восстановителем доменного процесса, поскольку ввиду газообразного состояния имеет высокую реакционную способность, способен проникать в любую точку домны. Кроме того, он не образует цементита. Эти реакции восстановления происходят при температуре 450…700 °C:
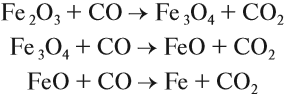
Полученный углекислый газ, реагируя с избытком кокса, вновь превращается в угарный газ:
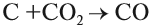
и процесс продолжается. Он происходит в верхней части домны. Выделяющееся в твёрдом виде железо опускается в нижнюю часть домны, контактирует с коксом, начинает плавиться, так как температура в этой части печи превышает 1300 °C. Кокс, образуя сплав с железом (чугун), понижает температуру плавления железа на 400°; одновременно с этим часть железа образует цементит:
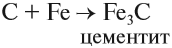
Для предохранения расплавленного железа от окисления в исходную смесь добавляют флюсы. Это известняк, который является поставщиком углекислого газа и, всплывая на поверхность, образует защитную плёнку.
Полученный чугун содержит до 4,5 % углерода, он используется для получения стали. Цель переработки — удаление примесей углерода, фосфора, серы. Готовая сталь должна содержать 0,3…2 % углерода. Кроме того, в сталь вводят различные добавки, которые изменяют её свойства. Так, нержавеющая сталь содержит около 12 % хрома.
Сталь является основным сплавом машиностроения, но легко ржавеет, так как подвергается коррозии (см. урок 8.4).

Выводы
Железо — главный металл нашей цивилизации. Станки, различные машины и механизмы, строительные конструкции, мосты, трубы — всё состоит из железа, точнее, стали или чугуна. Это достаточно активный металл, поэтому легко образует различные соединения, в которых чаще всего проявляет валентность III. Такие соединения имеют обычно красно-коричневую окраску (ржавчина).
В химическом отношении железо, кобальт и никель относятся к металлам средней активности. В электрохимическом ряду напряжений металлов они располагаются левее водорода, между цинком и оловом. Чистые металлы при комнатной температуре довольно устойчивы, их активность сильно увеличивается при нагревании, особенно если они находятся в мелкодисперсном состоянии. Наличие примесей значительно снижает устойчивость металлов.
-
Взаимодействие с неметаллами
При нагревании на воздухе выше 200 °С железо взаимодействует с кислородом, образуя оксиды нестехиометрического состава FexO, мелкодисперсное железо сгорает с образованием смешанного оксида железа (II, III):
Кобальт и никель реагируют с кислородом при более высоких температурах, образуя в основном оксиды двухвалентных элементов, имеющие переменный состав в зависимости от условий получения:
С галогенами металлы реагируют, образуя галогениды :
Металлы довольно устойчивы к действию фтора, никель не разрушается фтором даже при температуре красного каления.
При взаимодействии с азотом при невысокой температуре железо, кобальт и никель образуют нитриды различного состава, например:
Взаимодействие с серой экзотермично и начинается при слабом нагревании, в результате образуются нестехиометрические соединения, которые имеют состав, близкий к ЭS:
С водородом металлы триады железа не образуют стехиометрических соединений, но они поглощают водород в значительных количествах.
С углеродом, бором, кремнием, фосфором также при нагревании образуют соединения нестехиометрического состава, например:
Взаимодействие с водой
В воде в присутствии кислорода железо медленно окисляется кислородом воздуха (корродирует):
При температуре 700–900 °С раскаленное железо реагирует с водяным паром:
Кобальт и никель с водой не взаимодействуют.
Взаимодействие с кислотами
Железо реагирует с разбавленными растворами соляной и серной кислот, образуя соли железа (II):
с разбавленной азотной кислотой образует нитрат железа (III) и продукт восстановления азотной кислоты, состав которого зависит от концентрации кислоты, например:
При обычных условиях концентрированные (до 70 мас. %) серная и азотная кислоты пассивируют железо. При нагревании возможно взаимодействие с образованием солей железа (III):
По отношению к кислотам кобальт и никель устойчивее железа, медленно реагируют с неокисляющими кислотами с образованием солей кобальта (II) и никеля (II) и водорода. С разбавленной азотной кислотой образуют нитраты кобальта (II) и никеля (II) и продукт восстановления азотной кислоты, состав которого зависит от концентрации кислоты:
При обычных условиях концентрированные серная и азотная кислоты пассивируют кобальт и никель, хотя в меньшей степени, чем железо. При нагревании возможно взаимодействие с образованием солей железа двухвалентных металлов:
Взаимодействие со щелочами
Разбавленные растворы щелочей на металлы триады железа не действуют. Возможно только взаимодействие железа с щелочными расплавами сильных окислителей:
Для кобальта и никеля взаимодействие с расплавами щелочей не характерно.
Восстановительные свойства
Железо, кобальт и никель вытесняют металлы, которые расположены правее в электрохимическом ряду напряжений их растворов солей:
Образование карбонилов
Для металлов триады железа характерно образование карбонилов, в которых железо, кобальт и никель имеют степень окисления, равную 0. Карбонилы железа и никеля получаются при обычном давлении и температуре 20–60 °С:
Карбонилы никеля образуются при давлении 2·10 7 – 3·10 7 Па и температуре 150–200 °С:
Задание №1
Осадок, полученный при взаимодействии растворов хлорида железа (III) и нитрата серебра, отфильтровали. Фильтрат обработали раствором едкого кали. Выпавший осадок бурого цвета отделили и прокалили. Полученное вещество при нагревании реагирует с алюминием с выделением тепла и света. Составьте уравнения четырех описанных реакций.
при взаимодействии как солей соляной кислоты, так и самой кислоты с нитратом серебра образуется АgCl – нерастворимое в воде и кислотах творожистое вещество белого цвета (уравнение 1); эта реакция является качественной на хлорид-ион.
Фильтрат-раствор, прошедший через фильтр, который задерживает нерастворимые вещества. Взаимодействие растворимых солей с растворами щелочей-способ получения нерастворимых оснований (уравнение 2)
Fe(OH)3 – нерастворимое вещество бурого цвета, амфотерный гидроксид, разлагается при нагревании на оксид металла и воду (уравнение 3).
Восстановление металлов из их оксидов с помощью алюминияпромышленный способ получения многих металлов (алюмотермия); реакция экзотермическая, сопровождается выделением тепла, света и плавлением реакционной массы (уравнение 4)
Продукты разложения хлорида аммония последовательно пропустили через нагретую трубку, содержащую оксид меди(II), а затем через склянку с оксидом фосфора(V). Составьте уравнения четырёх описанных реакций.
Соли аммония и кислот, для которых нехарактерны окислительные свойства (NH4Cl, (NH4)2CO3), при нагревании разлагаются на аммиак NH3 и кислоту (уравнение 1)
Оксид меди (II) – основный оксид, кислоты реагируют с основными оксидами с образованием солей (уравнение2)
Аммиак, в котором азот находится в низшей степени окисления N –3 , проявляет восстановительные свойства и восстанавливает среднеактивные и малоактивные металлы из их оксидов (уравнение 3)
При взаимодействии P2O5 с водой, в зависимости от соотношения реагентов и температуры, могут образовываться фосфорные кислоты (H4P2O7, HPO3, H3PO4) (уравнение 4); азот с P2O5 не реагирует
Газ, выделившийся при взаимодействии хлороводородной кислоты с перманганатом калия, реагирует с железом. Продукт реакции растворили в воде и добавили к нему сульфид натрия. Более легкое из образовавшихся нерастворимых веществ отделили и ввели в реакцию с горячей концентрированной азотной кислотой.
Составьте уравнения четырёх описанных реакций.
Взаимодействие соляной кислоты с перманганатом калия является способом получения хлора (уравнение 1)
Железо взаимодействует с сильными окислителями с образованием соединений железа в степени окисления +3 (уравнение 2)
Железо в степени окисления +3 проявляет свойства окислителя, поэтому может взаимодействовать с восстановителем (сульфид натрия восстановитель, так как содержит серу в степени окисления S –2 ), образуя соединения двухвалентного железа (уравнение 3)
Горячая азотная кислота окисляет серу до высшей степени окисления +6 (до H2SO4), азот при этом восстанавливается до N +4 (до NO2) (уравнение 4)
При сжигании на воздухе простого вещества жёлтого цвета образуется газ с резким запахом. Этот газ выделяется также при обжиге некоторого минерала, содержащего железо, на воздухе. При действии разбавленной серной кислоты на вещество, состоящее из этих же элементов, что и минерал, но в другом соотношении, выделяется газ с запахом тухлых яиц. При взаимодействии выделившихся газов друг с другом образуется исходное простое вещество. Составьте уравнения четырёх описанных реакций.
Простое вещество желтого цвета, горящее на воздухе с выделением газа с резким запахом, – сера (уравнение 1)
Вещества, содержащие железо и серу: минерал пирит FeS2 и сульфид железа (II) (уравнения 2 и 3)
При взаимодействии оксида серы (IV) и сероводорода первый проявляет свойства окислителя, второй-восстановителя) и образуется простое вещество-сера (уравнение4)
После кратковременного нагревания неизвестного порошкообразного вещества оранжевого цвета начинается самопроизвольная реакция, которая сопровождается изменением цвета на зелёный, выделением газа и искр. Твердый остаток смешали с едким калии нагрели, полученное вещество внесли в разбавленный раствор соляной кислоты, при этом образовался осадок зелёного цвета, который растворяется в избытке кислоты. Составьте уравнения четырёх описанных реакций.
Решение:
Вещество оранжевого цвета, которое разлагается с изменением цвета на зелёный, – бихромат аммония (NH4)2Cr2O7 (уравнение 1)
Cr2O3 – вещество зелёного цвета, – амфотерный оксид и будет реагировать с безводной щелочью с образованием соли (уравнение 2)
В воде, в присутствии небольшого количества кислоты, KCrO2 будет гидролизоваться с образованием нерастворимого амфотерного гидроксида хрома(III) (уравнеие 3)
Амфотерный гидроксид хрома (III) растворяется в избытке кислоты с образованием Cr +3 , имеющий зелёный цвет (уравнение 4).
Как железо взаимодействует с кислородом
Железо — средний по химической активности металл. Входит в состав многих минералов: магнетита, гематита , лимонита, сидерита, пирита.
Химические и физические свойства железа
При нормальных условиях и в чистом виде железо — твердое вещество серебристо-серого цвета с ярким металлическим блеском. Железо — хороший электро- и теплопроводник. Это можно ощутить, дотронувшись в холодном помещении к железному предмету. Так как металл быстро проводит тепло, за короткий отрезок времени железо забирает большую часть тепла из человеческой кожи, поэтому во время прикосновения к нему ощущается холод.
Температура плавления железа — 1538 °С, температура кипения — 2862 °С. Характерные свойства железа — хорошая пластичность и легкоплавкость.
Железо реагирует с простыми веществами: кислородом, галогенами (бромом, йодом, фтором, хлором), фосфором, серой. При сжигании железа образуются оксиды металла. В зависимости от условий проведения реакции и пропорций между двумя участниками, оксиды железа могут быть разнообразными. Уравнения реакций:
Подобные реакции идут при высоких температурах. Здесь вы узнаете, какие опыты на изучение свойств железа можно провести дома.
Реакция железа с кислородом
Для реакции железа с кислородом необходимо предварительное нагревание. Железо сгорает ослепительным пламенем, разбрасывая искры — раскаленные частицы железной окалины Fe₃O₄. Такая же реакция железа и кислорода происходит и на воздухе, когда сталь при механической обработке сильно нагревается от трения.
При сгорании железа в кислороде (или на воздухе) образуется железная окалина. Уравнение реакции:
3Fe + 2O₂ = FeO • Fe₂O₃.
Железная окалина — соединение, в котором железо имеет разные значения валентности.
Получение оксидов железа
Оксиды железа — это продукты взаимодействия железа с кислородом. Наиболее известные из них — FeO, Fe₂O₃ и Fe₃O₄.
Оксид железа (III) Fe₂O₃ — оранжево-красный порошок, образующийся при окислении железа на воздухе.
Вещество образуется при разложении соли трехвалентного железа на воздухе при высокой температуре. В фарфоровый тигель насыпается немного сульфата железа (III), а затем прокаливается на огне газовой горелки. При термическом разложении сульфат железа распадется на оксид серы и оксид железа.
Оксид железа (II, III) Fe₃O₄ образуется при сжигании порошкообразного железа в кислороде или на воздухе. Для получения оксида в фарфоровый тигель насыпается немного смешанного с нитратом натрия или калия тонкого железного порошка. Смесь поджигается газовой горелкой. При нагревании нитраты калия и натрия разлагаются с выделением кислорода. Железо в кислороде горит, образуя оксид Fe₃O₄. После окончания горения полученный оксид остается на дне фарфоровой чашки в виде железной окалины.
Внимание! Не пытайтесь повторить эти опыты самостоятельно!
Оксид железа (II) FeO — это черный порошок, который образуется при разложении оксалата железа в инертной атмосфере.
1. Составьте формулы оксидов, гидроксидов и хлоридов железа, в которых он может проявлять степень окисления +2 и+3.
Напишите уравнения реакций взаимодействия железа с растворами: а) серной кислоты;
б) сульфата меди ( II ); в) бромоводородной кислоты ; г) нитрата свинца ( II ).
3. Допишите уравнения практически осуществимых реакций:
а) С uCl 2 + Fe в) Fe + H 2 O д) MgSO 4 + Fe
б ) Fe + H 2 SO 4 ( конц ) г ) Fe(NO 3 ) 2 + KOH ж ) Fe(OH) 2 + HCl
4. Заполните пропуски, расставьте коэффициенты в уравнениях:
а) FeCl 3 + _______ → ______ + NaCl г) Fe + ______ → FeCl 3
б ) ______ + BaCl 2 → FeCl 2 + BaSO 4 д ) _____ + ______ → FePO 4 ↓ + Na 2 SO 4
в ) Fe 2 O 3 + C → _____ + CO е ) Fe 2 O 3 + HNO 3 → _______ + _______
5. Напишите уравнения реакций взаимодействия железа с хлором, соляной кислотой, с кислородом, с серой. Обозначьте переход электронов. Сравните, в каких случаях железо окисляется более глубоко.
6. С какими из перечисленных веществ реагирует железо: бром, водород, концентрированная серная кислота, сульфат магния, гидроксид калия, хлорид ртути ( II )? Привести уравнения соответствующих реакций.
7. С какими из перечисленных веществ реагирует железо: хлор, сера, вода, серная кислота, гидроксид натрия, хлорид калия, сульфат меди ( II )? Привести уравнения соответствующих реакций.
8. Как доказать, что в одном из двух растворов есть ионы Fe 2+ , а в другом – ионы Fe 3+ ? Напишите уравнения протекающих реакций.
9. Какой характер имеют оксиды железа ( II ) и ( III ) и соответствующие им гидроксиды? Приведите уравнения реакций, подтверждающие эти свойства.
10. Получить железо из оксида железа ( III ) восстановлением углем, угарным газом, водородом, алюминотермией, магнийтермией. Показать число переходящих электронов.
11. Осуществить превращения, назвать вещества:
12. Осуществить превращения, назвать вещества:
13. В четырех колбах без этикеток находятся растворы: сульфата железа ( III ), сульфата железа ( II ), сульфата натрия и вода. Как практически определить эти вещества, опишите порядок предполагаемых действий, приведите уравнения соответствующих реакций.
14. Вычислить массу железной окалины, которая образуется при сгорании порции порошка железа массой 28 г.
15. Вычислить массы исходных веществ, которые потребуются для получения 10 г хлорида железа ( II ).
16. Порцию железа массой 12 г растворили в соляной кислоте. Найти объем газа, образовавшегося при этом.
17. Напишите уравнения реакций взаимодействия железа с хлором, серой, бромом, кислородом.
18. Вычислить массу оксида железа ( III ), который потребуется для получения железа массой 1 кг.
19. Осуществить превращения, назвать вещества:
Нитрат железа ( III ) → гидроксид железа ( III ) → оксид железа ( III ) → железо → хлорид железа ( II )
20. Осуществить превращения, назвать вещества:
Железо → сульфат железа ( II ) → гидроксид железа ( II ) → оксид железа ( II ) → хлорид железа ( II ) →железо
21. Как, исходя из сульфата железа ( II ) получить хлорид железа ( II )? Приведите уравнения соответствующих реакций.
22. Какой объем хлора (н.у.) необходим для реакции с 7 г железа?
23. Химическая реакция протекает согласно уравнению: FeCl 2 + NaOH → Fe ( OH )2↓+ NaCl . Расставьте коэффициенты и решите задачу по следующим данным (ответы впишите в колонки):
Читайте также:

