Брахитерапия рака предстательной железы с иридием 192
Брахитерапия рака предстательной железы – это современная методика лечения, основанная на применении излучений радиации на пораженные участки организма. При данном способе терапии рака соседние к опухоли здоровые участки практически не задействованы. Брахитерапия используется во всем мире как наиболее эффективный метод борьбы с онкологическими недугами, в том числе затрагивающими предстательную железу, результаты которой сопровождаются минимальным количеством побочных действий.
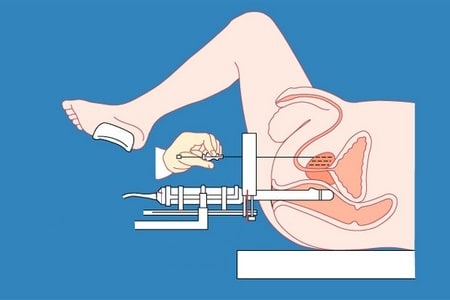
- Общие сведения о методике
- Когда рекомендуют процедуру
- Подготовительный этап
- Как проводится процедура?
- Положительные свойства методики
- Побочные эффекты
- Послеоперационные рекомендации
Общие сведения о методике
Брахитерапия подходит для лечения онкозаболеваний, но делать процедуру необходимо, когда нет вторичных патологических очагов – метастазов. Особенно широко метод себя зарекомендовал для борьбы со злокачественными образованиями в половых органах – предстательной железе, матке, а также желудочно-кишечном тракте – пищеводе, прямой кишке, это подтверждают многочисленные положительные отзывы пациентов.
- Внутритканевая (контактная) брахитерапия – применяется для лечения рака простаты.
- Внутриполостная – используют для терапии рака полых органов.
- Поверхностная – помещение радиоактивного импланта (аппликации) на кожные покровы.
- Внутрипросветная – источник радиации помещается в какой-либо канал организма.
- Внутрисосудистая.
- Применяется специальный автомат с радиационным источником – автоматизированная брахитерапия.
- Ручная методика – радиационный элемент внедряется и устраняется в ручном режиме.
Брахитерапия рака предстательной железы основывается на применении максимально допустимой дозировки излучения на опухолевую область. Есть два вида – низкодозная и высокодозная HDR-брахитерапия – это лучевая терапия, проводимая внутри ткани предстательной железы с использованием мощного источника энергии.
Когда рекомендуют процедуру
Брахитерапия может проводиться в поликлинике или в стационаре без госпитализации. Процедуру рекомендуют мужчинам, у которых опухоль находится в предстательной железе и ее размеры не более 2 мм. При больших размерах больному предварительно назначают гормональную терапию с целью уменьшения опухоли.
Существуют противопоказания, при которых брахитерапия не применяется для лечения рака:
Задайте вопрос врачу-урологу!

- Размер простаты больше 50 см3.
- Если показатель остаточной мочи выше нормы или скорость оттока мочи ниже 10 мл/с.
- Если рак предстательной железы рецидивировал, и у больного были обнаружены метастазы.
Любой повышенный показатель является серьезным показанием для того, чтобы вмешательство было отменено.
Подготовительный этап
Прежде всего, состояние предстательной железы определяют пальпаторным путем. После этого больного отправляют на проведение ТРУЗИ и магнитно-резонансную томографию органов. Также определяют результаты – в норме ли находится количество остаточной урины.
Брахитерапия может проводиться в поликлинике или в стационаре без госпитализации.
Обязательным является анализ на простатический специфический антиген – ПСА. На сегодняшний день ПСА – это самый точный опухолевый маркер, выявляющий наличие рака простаты. Для ПСА берется у мужчин кровь из вены. Онкомаркер ПСА используется в дальнейшем, чтобы отслеживать результаты операции.
Как проводится процедура?
В мировой медицине брахитерапия от рака проводится с применением одного из перечисленных химических элементов: йода, иридия, цезия, палладия. Но в российской практике результаты клинических испытаний доказали эффективность только двух элементов – йода (применяется низкая мощность дозирования) и иридия (повышенная мощность дозировки). Их и используют в отечественных клиниках и медицинских центрах для борьбы с раком простаты в том числе.
Высокодозная HDR-брахитерапия имеет направленное излучение, то есть только на определенный участок, на опухолевую область простаты. Результаты HDR такие, что в отличие от лучевой терапии она не повреждает здоровые участки ткани, например мочевого пузыря или прямой кишки.
Йодный изотоп помещен в специальную капсулу из титана, которая является микроисточником. Кроме основного элемента, есть еще маркер, контролирующий положение изотопа в период терапии. С помощью тончайших игл, внутри которых они расположены, микроисточники радиации вводятся в область злокачественного образования.
Перед проведением, используя программное обеспечение, происходит расчет максимально допустимой дозировки радиоизлучения. Доза облучения для каждого пациента индивидуальна. Распадаясь, изотоп облучает патологически измененные клетки опухоли, почти не влияя на здоровые клетки. В результате это выгодно отличает данный метод от лучевой терапии. В течение 12 месяцев, после того как провели операцию, от пациентов исходит повышенное излучение.
После мероприятия капсула остается в организме – в пределах предстательной железы, но существует также возможность ее выхода естественным путем вместе с уриной. Пациентов предупреждают, что в этом случае делать нельзя, а именно: брать в руки вышедший микроисточник. Его следует захватить при помощи пинцета, положить в емкость и доставить в больницу. Там источник впоследствии утилизируют по всем правилам.
В течение 12 месяцев, после того как провели операцию, от пациентов исходит повышенное излучение.
Брахитерапия иридием длится от 7 до 20 минут и осуществляется автоматическим методом. В процессе операции дозировка химического элемента подается через шланги в специальные иглы, которые помещены в ткани простаты. Операция на предстательной железе проводится под наблюдением трансректального ультразвукового исследования (ТРУЗИ).
Отзывы специалистов и результаты данных сходятся – йодный изотоп является эффективным элементом для проведения брахитерапии. Контроль за развитием рака и наблюдение после того, как проводится манипуляция, осуществляется при помощи трансректального УЗИ, компьютерной томограммы (КТ).
Если состояние больного раком является стабильным, то он пребывает в стационаре двое суток – 1 день до проведения брахитерапии предстательной железы и один после нее. До выписки проводится обязательная проверка радиационных показателей. После вмешательства мужчине ставят катетер в среднем на 24 часа, который облегчит мочеиспускание.
Положительные свойства методики
Учитывая отзывы, статистику и результаты исследований, брахитерапия является эффективным методом борьбы с раком предстательной железы. К ее положительным результатам можно отнести следующее:
- Процент рецидивов рака составляет всего 20%, это очень низкий показатель.
- Операция отличается высокой эффективностью.
- В случае рецидива есть возможность повторить процедуру, применяя иридий.
- Брахитерапия простаты подразумевает всего 2-дневное пребывание в стационаре. После прочих мероприятий лечение и наблюдение более длительное.
- Если сравнивать с другими методиками, осуществляемыми при онкологическом заболевании предстательной железы, в данном случае риски осложнений минимальны.
- Реабилитационный период после процедуры не длительный.
Побочные эффекты
Естественно, брахитерапия все же операция, и серьезная, и перед тем, как ее делать, специалисты предупреждают о возможных побочных действиях. Среди основных расстройств чаще наблюдается следующие:
- Затруднение мочеиспускания – наблюдается в течение первых суток, ничего делать не нужно, процесс самостоятельно нормализуется.
- У 1-2 больных из 100 учащается мочеиспускание, процесс может сопровождаться жжением, дискомфортом.
- Операция негативно влияет на эрекцию – у половины наблюдается эректильная дисфункция. В этом случае после процедуры проводится лечение по ее восстановлению.

Возможны побочные эффекты.
Послеоперационные рекомендации
Естественно, что операция, какая бы она ни была по сложности, оставляет определенный отпечаток на всю оставшуюся жизнь. В результате такого лечения рака предстательной железы врачи дают некоторые рекомендации. В первые 7-8 недель после операции простаты нельзя делать следующее:
- Брать детей, животных на руки.
- Контактировать с беременными женщинами.
- Посещать физиокабинет без совета онколога.
Уже через месяц-полтора после процедуры по удалению опухоли простаты мужчина возвращается к привычной жизни. Останется обязательным регулярный анализ ПСА. В течение первых 12 месяцев его рекомендовано делать каждые 3 месяца. После количество уменьшается, ПСА необходимо делать 2 раза в год.
Стоит отметить, что в случае рецидива рака железы уровень ПСА повышается постепенно, а вот после любого воздействия, в том числе радиационного, показатель ПСА резко и значительно увеличивается, через короткое время снова снижается. Поэтому после операции этот анализ не сдается, адекватные результаты онкомаркер ПСА даст только через 1-1,5 месяца.
Цена брахитерапии складывается из нескольких пунктов:
- Стоимости радиоактивных элементов.
- Планирования операции.
- Сюда же входит и цена самой процедуры, и послеоперационное пребывание в клинике.
Кроме того, цена может меняться в меньшую сторону, так как на территории РФ действуют квоты. Стоимость меняется и в зависимости от того, делать ее по полису ОМС или через хозрасчетный отдел. Средняя цена брахиотерапии рака простаты составляет 250000 рублей.
Если у вас остались вопросы, задайте их в комментариях (это абсолютно анонимно и бесплатно). По возможности, я или другие посетители сайта помогут вам.

Что такое брахитерапия рака предстательной железы
Брахитерапия рака простаты подразумевает уничтожение опухолевых клеток путем воздействия радиации. Для этого в железу внедряют заполненные специальным веществом иглы или зерна (капсулы) с радионуклидами. В качестве последних могут быть I-125 (микроисточник йода), Pd-103 (палладий), 198-Au (золото).

Капсула с изотопом
Цель брахитерапии – обеспечение предстательной железы такой дозой облучения, которая будет достаточна для уничтожения всех раковых клеток. Для этого важно правильно рассчитать дозировку, распределить зерна, чтобы диапазон воздействия охватывал контуры простаты, но облучение прилежащих тканей было бы минимальным.
Плюсы брахитерапии при РПЖ (раке предстательной железы):
- Минимальные кровопотери.
- Недолгий период реабилитации.
- Высокий шанс сохранения потенции.
- Возможно проведение у пожилых пациентов, состояние которых не совсем удовлетворительно.
- В большинстве случаев достаточно однократного проведения процедуры.
- Точечное воздействие на ткани.
- Незначительный период длительности побочных эффектов.
Основное условие успеха брахитерапии – тщательный отбор пациентов по показаниям.
Виды брахитерапии
По степени лучевой нагрузки и технике проведения выделяют низкодозную (постоянную, или LDR) и высокодозную (временную, или HDR) брахитерапию. Первая показана при раке простаты 1 и 2 степени. В качестве радиоактивного вещества используются йод или палладий. Эти вещества распадаются через несколько месяцев. Через год они станут биологически неактивными, но капсулы остаются в организме, не причиняя дискомфорта.
Высокодозная, или высокомощностная брахитерапия рака предстательной железы предполагает введение радиоактивного вещества (иридия-192) в заранее погруженные в ткани простаты полые иглы. Через 5-15 минут они извлекаются. Вещество подается в иглы через тонкие трубки, присоединенные к источнику – микроселетрону. Обычно процедура проводится трижды с интервалом в 2 дня. Временная брахитерапия показана пациентам с прогрессирующей карциномой, разрастающейся за пределы капсулы органа. При раке простаты 3 степени высокодозное излучение применяется в совокупности с внешним облучением.
По статистике 40% больных раком простаты получают чрезмерное лечение, поскольку их форма заболевания является клинически незначимой. В связи с этим остро стоит вопрос о развитии щадящих методов. Одним из таких является фокальная брахитерапия – зональное распределение источников излучения, при котором максимально высокая нагрузка направляется на только опухолевый очаг .

Примеры распределения лучевой нагрузки на простату методом фокальной брахитерапии: а – таргетная (ультрафокальная) схема; б – гемиаблативная (облучается одна доля простаты); в – фокусированная на видимый очаг; г – фокусированная на периферическую зону
Показания к проведению
Классическая низкодозная брахитерапия показана при локализованной опухоли (Т1-Т2), которая еще не проросла в простатическую капсулу. При принятии решения ориентируются на значение по шкале Глисона (градация найденных во время гистологии клеток опухоли по степени опасности). Оно должно быть меньше 7. Принимают во внимание и значение ПСА. Желательно, чтобы оно было в диапазоне от 10 до 20 нг/мл.
Основные критерии для назначения брахитерапии:
- Положительный прогноз на выживаемость пациента (более 5 лет), удовлетворительное самочувствие.
- Объем простаты по данным УЗИ не более 60 см 3 . Если железа слишком большая, то возможно ее уменьшение на 50% при помощи гормональной терапии – трехмесячного курса аналогов гонадотропин-рилизинг гормона.
- Отсутствие выраженных проблем с мочеиспусканием.
- В анамнезе пациента не должно быть трансуретральной резекции простаты. Брахитерапия допускается только в том случае, если последствия после ее проведения (рубцовые изменения) минимальны.
Если два последних условия игнорируются, то после брахитерапии очень высока вероятность развития недержания мочи.
Если по результатам гистологии раковые клетки обнаружены в различных областях простаты, то рекомендовано проведение брахитерапии в совокупности с гормональным лечением.

Показания к высокодозной брахитерапии
Лечит ли брахитерапия рак – эффективность метода
Согласно статистике, у пациентов со стадией опухоли простаты Т1 пятилетняя выживаемость составляет 100%, на Т2 – 75%, на Т3 – 60%. В среднем выживают 98% пациентов .
Успешного результата от постоянной брахитерапии изотопами I-125 либо Pd-103 (применяется в преимущественном большинстве клиник РФ) можно ожидать при соблюдении следующих условий:
- Локально ограниченная форма опухоли (стадия Т2а, статус N0M0);
- Значение по шкале Глисона меньше 6;
- Уровень ПСА не выше 10 нг/мл;
- Скорость потока мочи по итогам урофлоуметрии не меньше 15 мл/сек., объем остаточной мочи менее 50 мл;
- Объем простаты менее 50 мл.
От возраста пациента результат брахитерапии зависит не сильно. Гораздо большее значение имеет образ жизни: физическая и социальная активность. Говорить о победе над раком можно только через полтора года, в течение которых уровень ПСА будет стабильно низким, а по данным МРТ малого таза не обнаружится роста опухоли.

Подготовка к брахитерапии
Брахитерапии предшествует стандартный набор исследований:
- УЗИ, КТ малого таза.
- Коагулограмма.
- Анализ мочи и крови.
Полный список анализов и сроки их действия:

За сутки до брахитерапии следует соблюдать диету: минимум жиров, легкая пища, от ужина накануне лучше отказаться. Непосредственно в день процедуры рекомендуется сделать клизму для очищения прямой кишки. Пищу принимать нельзя.
Как проводится
Брахитерапия проводится в два этапа. На первом делают ТРУЗИ простаты. В мочевой пузырь предварительно вводится заполненный газом катетер, чтобы различить уретру. Затем на основании полученных УЗ-срезов формируют трехмерную модель, на которой определяют количество и места введения радиоактивных зерен. На втором этапе проводят собственно брахитерапию. Источник радиации герметичен, поэтому в дополнительных мерах предосторожности нет необходимости.

3D модель введения игл при высокодозной брахитерапии
Для проведения брахитерапии пациент укладывается в литотомическое положение (на урологическом кресле с разведенными ногами). Анестезия может быть как общей, так и местной. В прямую кишку помещают ТРУЗИ-датчик, изображение регулируют таким образом, чтобы оно максимально совпало с предварительно построенной моделью. Затем вводят иглы с зернами, которые могут быть размещены в них заранее, либо доставляются в ткани при помощи Мик-аппликатора. Последняя методика популярна за рубежом, а в России зерна выпускаются либо отдельно, либо нанизанными на рассасывающиеся нити (это исключает возможность их перемещения в тканях). Нити нарезают и заправляют в иглы-троакары. В качестве направляющего элемента для последних используется матрица, отверстия в которой совпадают с УЗИ-схемой.
Методикой последнего поколения является введение капсул при помощи игл Nucleotron. Зерна крепятся к кончику, а при доставке в нужную область отщелкиваются.
Под контролем КТ можно вводить капсулы в семенные пузырьки, область вокруг простаты. Такой метод контроля дает возможность проводить брахитерапию пациентам с железой более 50 см 3 в объеме, а также при наличии в ней конкрементов (камней).
Важным этапом является планирование дозы (составление дозиметрического плана). Эту задачу решает компьютерная программа (например, PSID 4.1.2) под контролем медицинского физика. Доза на всю железу составляет от 140 до 160 Гр. Мощность имплантата измеряется в греях (это мощность одной поглощенной дозы излучения).

Программный расчет дозировки 
Положение пациента во время брахитерапии 
Набор игл и матрица для облучения простаты 
Низкодозная брахитерапия при помощи матрицы
Сначала имплантируют капсулы в переднюю часть простаты, чтобы не затемнять область введения остальных. Всего имплантируется от 41 до 100 капсул. Процедура длится около 2 часов.
По завершении брахитерапии проводят цистоскопию (осмотр мочевого пузыря изнутри), чтобы не оставить случайно провалившихся или торчащих в просвет уретры зерен. КТ позволяет максимально четко идентифицировать каждое зерно и контуры железы, но сделать это можно и при помощи рентгенографии.

Рентгенография после брахитерапии 
Проведение высокодозной брахитерапии
Уровень ПСА после брахитерапии рака предстательной железы
После брахитерапии ПСА может сохраняться в крови еще длительное время. Первый раз анализ сдают через 3 месяца. Полностью маркер почти никогда не исчезает, поскольку какая-то часть деградировавшего эпителия все же сохраняется. Есть повод подозревать рецидив, если его уровень превысит 0,1-0,4 нг/мл. В течение первых трех лет может наблюдаться скачок ПСА до 0,2-0,3 нг/мл еще до достижения минимального порога.
Для контроля результатов также применяют биопсию (через год или позднее), УЗИ, КТ. Визуальные методы исследования в первый год проводят раз в 3 месяца, затем раз в полгода.
Последствия
Для брахитерапии в отличие от простатэктомии нехарактерно недержание мочи. Подобное может возникнуть только после ранее проведенной ТУР, поскольку лучевая энергия ослабляет наружный уретральный сфинктер. У пациентов после брахитерапии нередко развиваются другие осложнения со стороны мочеполовой системы: учащенное мочеиспускание, рези, чувство неполного опорожнения мочевого пузыря, но они проходят примерно за 3 месяца, в крайнем случае − через полгода. Для их лечения эффективнее всего альфа-адреноблокаторы.
Для брахитерапии характерна задержка мочи. Подобное случается у 5% пациентов. В таких случаях оптимальным методом лечения является периодическая катетеризация, при которой мочеиспускание нормализуется в течение нескольких недель.
У 10% пациентов в течение 5 лет после брахитерапии могут образоваться стриктуры (спайки) уретры. При необходимости они устраняются иссечением во время уретроскопии.

Стриктура уретры — это патологическое состояние, которое характеризуется сужением мочеиспускательного канала, и ведёт, в конечном итоге, к нарушению нормального оттока мочи при мочеиспускании
Что касается потенции, что в большинстве случаев она сохраняется. После брахитерапии качество эрекции и либидо сохраняется на 50-85%. Тут особую роль играет психологический фактор. Многие пациенты сами боятся вступать в половые отношения даже по истечении периода реабилитации. Им кажется, что уровень ПСА снижается слишком медленно, высока вероятность рецидива. От постоянного стресса падает потенция.
- Изъязвление или воспаление прямой кишки (1%).
- Некроз уретры (3%).
- Недержание мочи (6%).
- Цистит, уретрит (7%).
- Кровь в моче (1%).
Осложнения после брахитерапии минимальны по сравнению с радикальной простаэктомией или обычной лучевой терапией.
Реабилитация после брахитерапии простаты
После операции пациент около суток проводит в больнице. Катетер удаляют через 2-3 часа, после этого можно передвигаться, есть и пить. После высокодозной (временной) брахитерапии пациент может отправиться домой в тот же день, если нет противопоказаний.
На следующий день после введения зерен, а также через 4-6 недель обязательно осуществляют дозиметрический контроль для оценки лучевой нагрузки на органы. На расстоянии метра мощность излучения не должна превышать 10 мкЗв/час. Данные заносятся в выписку, которую пациент при необходимости может предъявить, например, в аэропорту. Этот же документ необходим при срабатывании металлоискателя (на зерна в простате).
В первые 2 недели нельзя подвергаться физическим нагрузкам, иначе капсулы начнут мигрировать в тканях простаты. Также не следует сидеть на одном месте дольше полутора часов, держать на коленях детей, ездить на велосипеде, ходить в баню. Кишечник и мочевой пузырь должны опорожняться своевременно, чтобы не давить на простату. Жирной, острой и жареной пищи, а также алкоголя нужно избегать. По истечении данного срока 80% пациентов без проблем возвращаются к своей нормальной жизни. К занятиям в спортзале можно приступать через 3 месяца.
В связи с тем, что после постоянной брахитерапии пациент на некоторое время становится носителем источника радиационного излучения, следует соблюдать особые меры безопасности. В первые 5 дней рекомендуется мочиться через марлю (чтобы капсула не попала в канализацию), а в течение 6 месяцев пользоваться презервативами во время полового акта. В первые 2 месяца после имплантации не следует долго находиться рядом с беременными женщинами.
Через полгода можно отменить данные меры предосторожности, поскольку носитель изотопа становится биологически нейтральным.
Стоимость брахитерапии простаты
Проведение брахитерапии за собственный счет стоит от 500000 руб. Например, цена в городском онкодиспансере СПб составит от 657400 руб. Что касается зарубежных клиник, то по сравнению с отечественными онкоцентрами стоимость брахитерапии в них возрастает в десятки раз при тех же результатах.
Отзывы пациентов
Заключение
Брахитерапия рака простаты является таким же радикальным методом лечения, как и хирургическое удаление, но негативных последствий в разы меньше. Многие пациенты из-за неосведомленности с опаской относятся к такого рода облучению, но бояться нечего: негативное воздействие на другие органы минимально, в случае рецидива можно провести или химиотерапию или повторную брахитерапию. Результат во многом зависит от квалификации врача. Отечественные онкологи в государственных специализированных центрах сейчас владеют техникой брахитерапии не хуже зарубежных.
В 2000e годы лучевая терапия зарекомендовала себя как надежный и эффективный метод лечения рака предстательной железы.
Помимо того, что онкологическим больным очень тяжело дается осознание собственной болезни, перед ними зачастую стоит непростая задача выбора метода лечения. Специалисты нашей клиники с большой ответственностью подходят к выбору диагностики и лечения рака предстательной железы. Чрезвычайно важно при назначении диагностического исследования и выборе метода лечения взвесить все возможные варианты, и, основываясь на изученных примерах из медицинской практики и проверенной информации, предложить пациенту оптимальный план. При обсуждении различных методов лечения, их преимуществ и недостатков, врачи Дократес всегда прислушиваются к мнению самого пациента и его родных.
Существует 2 типа брахитерапии: LDR (Lowe dose rate) – низкодозная брахитерапия и HDR (High dose rate) – внутритканевое высокодозное облучение. При технике LDR в предстательную железу под контролем УЗИ вводятся частицы, заряженные радиойодом I-125.Такое лечение проводится один раз. В Финляндии LDR-брахитерапия применяется все реже и реже. На смену ей приходит высокодозная брахитерапия, при которой используется источник высокой мощности Ir-192 (Иридий).
В основном, при раке предстательной железы HDR-брахитерапия проводится в комплексе с наружной лучевой терапией, усиливая ее действие, однако HDR-брахитерапия применяется также и как единственный способ лечения рака предстательной железы. В отличие от LDR-брахитерапии, высокодозная брахитерапия успешно применяется при лечении рака, распространенного за пределы капсулы предстательной железы. Ранее в Дократес применялась техника LDR, сейчас врачи клиники ею не пользуются, а проводят HDR-брахитерапию, которая имеет ряд очевидных преимуществ. HDR-брахитерапия подходит ко всем типам рака предстательной железы (LDR-брахитерапия рекомендуется только в случаях с хорошим прогнозом ПСА В Финляндии HDR -брахитерапия при раке предстательной железы впервые стала проводиться в онкологической клинике Дократес в 2009 г. На сегодняшний день наша клиника является лидером в Финляндии по лечению рака предстательной железы данным методом.
Как проводится HDR-брахитерапия
HDR-брахитерапия проводится совместно урологом и медицинским физиком, владеющим специальными знаниями дозпланирования и проведения терапии. В лечении также принимают участие: анестезиолог, онколог, медсестра, ассистирующая анестезиологу, медсестра рентгенологии и другой младший медперсонал.
HDR-брахитерапия рассчитывается интерактивной планирующей 3D программой. Программа создает точную объемную копию предстательной железы пациента, и планирует дозовое распределение источников радиации и время облучения (раньше было доступно только при планировании наружной лучевой терапии).
Сама процедура заключается в следующем: в зависимости от объема и строения предстательной железы рассчитывается количество игл-троакаров (10-20 игл, толщиной 1,5 или 1,9 мм.) и их расположение в предстательной железе. Иглы вводятся в простату через промежность.
Лечение проводится под общим наркозом или эпидуральной анестезией. Для расчета дозы врач визуализирует границы предстательной железы и определяет местоположение мочеиспускательного канала. После этого физик составляет предварительный расчет дозы и определяет количество и местоположение игл. Облучение направляется на всю железу, но брахитерапия рассчитывается таким образом, чтобы максимальная доза подавалась к участкам, в которых раковые клетки подтверждены при биопсии. Затем на основании внешних координат иглы устанавливаются на обозначенные места. Из-за установки игл простата немного смещается. Это учитывается, и вносятся соответствующие изменения, вызванные смещением границ простаты и мочеиспускательного канала. В завершение данного этапа на трехмерной картинке врач обозначает другие чувствительные к облучению здоровые ткани, например прямую кишку и мочевой пузырь. Затем физик проводит окончательный расчет доз, с учетом фактического положения игл. После расчета доз и определения участков облучения производится зарядка радиоактивного источника в иглы. По этим иглам источник излучения Иридий ( Ir – 192 ) последовательно доставляется к заданным участкам и задерживается там в соответствии с заранее определенной дозой с интервалом 2,5 мм. Весь процесс контролируется дистанционно. Чем дольше источник излучения находится в определенном месте, тем выше доза местного облучения. Облучение длится 10–20 минут. Затем иглы удаляют, вынимают катетер из мочевого пузыря, пациента будят и переводят в палату для наблюдения, где он проводит следующую ночь.
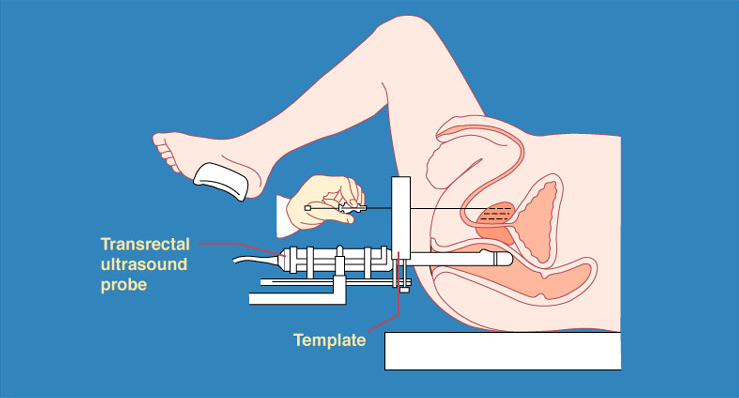
Рис. HDR-брахитерапия
Многообещающие результаты HDR-брахитерапии в Финляндии и в мире
Согласно отчетам, опубликованным в международных медицинских изданиях, HDR-брахитерапия эффективна при лечении рака в группах пациентов с низким, средним и высоким риском. По данным отчета известного немецкого центра HDR-брахитерапии – клиники Offenbach, из 718 пациентов, получивших монорежимно HDR-брахитерапию, у 95% не обнаружилось рецидива заболевания спустя 5 лет наблюдения ( в среднем 5 лет). По данным голландской публикации 2011 г., у 97 % группы из 264 пациентов с низким и средним риском, заболевание не было выявлено в течение 7 лет наблюдения. Согласно отчетам известной нью-йоркской онкологической клиники Memorial Sloan Kettering, у 81 % из 229 пациентов с высоким риском заболевания, получивших очень высокую дозу облучения (199 Гр), не был выявлен рак в течение 7 лет облучения. Доказано, что в группах онкологических пациентов с высоким риском сочетание наружной лучевой терапии с HDR-брахитерапией более эффективно, чем обычная лучевая терапия. Побочное воздействие от комбинированного лечения не выше, чем от обычной лучевой терапии.
Подробнее

В мае этого года врачи онкологической клиники Дократес приняли участие в престижной конференции Американского общества клинической онкологии (ASCO), чтобы услышать.
Читайте также:

