Биологическое поведение опухоли это
Выявление новообразования далеко не всегда угрожает жизни: разные виды опухолей могут быть доброкачественными и злокачественными, но даже в последнем случае при своевременном начале лечения имеются вполне реальные шансы на выживание. Рак можно победить, но главное условие успешной терапии – ранняя диагностика и активная лечебная тактика.

Опухолевая ткань может возникнуть в любом месте тела
Опухоль – что это
Новообразование – это разрастание клеточных структур в любых органах или тканях. Основная причина возникновения опухоли – действие канцерогенных факторов на генетический аппарат клеток (дефект в генах запускает процессы неконтролируемого опухолевого роста). Важными условиями злокачественности являются:
- скорость роста (быстрое увеличение размеров новообразования);
- дифференцировка тканей (гистологическая схожесть с исходными клетками органа);
- множественность поражения;
- распространение опухолевых клеток (метастазирование).
Чем раньше обнаружен рак, тем больше шансов для выздоровления. Разные новообразования по-разному диагностируются: легко доступные для исследования локализации (кожа, шейка матки, прямая кишка, молочная железа) можно выявить в 0-1 стадии, что позволяет надеяться на полное излечение. Сложные для диагностики разновидности рака (головной мозг, кишечник, панкреатическая железа, почки) часто приводят к запущенным формам заболевания с неблагоприятным прогнозом. Большое значение имеет настороженность пациента: если человек с типичными признаками опухолевого роста или симптомами общей интоксикации не обратится к врачу, то никто не поставит диагноз и не начнет лечение.
Виды опухолей – важные критерии
- первично-локализованные (одиночный узел);
- первично-системные (диффузные формы);
- первично-множественные (много узлов в разных местах);
- мультифокальные (несколько опухолей в одном органе);
- билатеральные (новообразования в парных органах);
- вторичные (любые варианты метастазов).
В зависимости от прогностической значимости для жизни выделяют следующие виды:
- Доброкачественные;
- Злокачественные.

Только гистологическое исследование может подтвердить или опровергнуть опасный диагноз
К важнейшим критериям опухолевого роста для обоих вариантов относятся:
- скорость увеличения размеров (медленный рост в первом случае, быстрый – во втором);
- поверхность опухоли (гладкая и ровная у доброкачественных, бугристая и неровная у злокачественных);
- размер (маленькая раковая опухоль убьет быстрее, чем большое доброкачественное новообразование);
- кровоснабжение (излишне выраженное формирование сосудистой сети указывает на рак);
- метастазирование (рак на последних стадиях практически всегда отправляет опухолевые клетки в отдаленные органы и ткани, доброкачественная опухоль никогда не метастазирует).
Опухолевый рост может начаться в любом месте организма – ткани или клетки при повреждении канцерогенами или при врожденном дефекте генного аппарата запускают процесс бесконтрольного увеличения размера и количества. Многообразные виды опухолей указывают на универсальность формирования новообразования: биологическое поведение рака зависит от активности клеточных структур и наличия защитных факторов в организме. Избавиться от рака можно, но только при вовремя поставленном диагнозе, четком определении разновидности новообразования и правильном использовании современных методов лечения онкологического заболевания.
Опухоли- атипичные разрастания тканей организма, по характеру роста и функциональному значению резко отличающиеся от нормального развития и других патологических процессов. В основе роста лежит безграничное размножение клеток.
Опухоли могут возникать из любой ткани организма, в любом организме.
Изучением опухолей занимается специальная наука- онкология( от греч. Oncos-опухоль)
По биологическому поведению могут быть доброкачественными, злокачественными и с местным деструирующим ростом.
В зависимости от гистогенеза:
эпителиальные— папилломы, аденомы, кистомы, дерматомы, карциномы; соединительнотканные — фибромы, миксомы, липомы, хондромы, остеомы, меланосаркомы; сосудистые — гемангиомы, лимфангиомы; мышечные— миомы, рабдомиомы; из нервной ткани — глиомы и невромы; смешанные — остеосаркома, фибромиксохондрома, фиброхондроостеома.
1) Физико-химическая теория.Автор теории немецкий ученыйРудольф Вирхов— 1855 год. опухоли вызываются длительным повреждающим действием физических и химических факторов. Примеры – рак в рубце после ожога, многочисленные профессиональные раки, паразитарные инфек-ции, гормональные раки, раки при курении, действии радиоактивных веществ, стронция, кобальта и других факторов
2) Вирусная и вирусно-генетическая теория.Автор – советский ученыйЛев Зильбер– вторая половина 20 века. По этой теории главным фактором, который вызывает превращение нормальной клетки в раковую клетку яв-ляется онкогенный вирус, который встраивается в геном клетки. А все остальные физические и химические факторы действуют только как активаторы вируса. 3) Дизонтогенетическая теория.Автор — немецкий ученыйКонгейм, 19 век. По данной теории считается, что источником опухоли являются пороки развития тканей с наличием эмбриональных клеток. Именно эмбриональные клетки затем превращаются в раковые клетки. Эта теория имеет ограниченное значение. Так как только небольшая группа опухолей имеет чисто эмбриональное происхождение. Примером такой опухоли может быть дермоидная киста яичника. Опухоль представляет собой полость. Стенкой полости является кожа(дерма). Внутренняя поверхность полости покрыта эпидермисом и содержит придатки кожи – сальные, потовые железы и волосяные фолликулы. Снаружи располагается подкожно-жировая клетчатка. В полости дермоидной кисты накапливаются жировые массы, пучки волос, а в стенке могут нахо-диться зачатки зубов.
4) Полиэтиологическая теория.По этой теории представляется, что опухоль могут вызывать все факторы — химические, физические, вирусы, бактерии, то есть очень много факторов. Опухоль – это процесс полиэтиологический. Но теория не отвечает на механизмы трансформации нормальной клетки в раковую
32 Морфологическая характеристика доброкачественных опухолей.
Доброкачественные опухоли – опухоли которые при развитии пагубно не влияют на организм животного. Они построены из хорошо дифференцируемых клеточных элементов. По их строению можно определить из какой ткани они развились. В их структуре можно видеть признаки тканевого атипизма, в то время как клеточный атипизм практически не выступает. Растут опухоли медленно, характеризуются центральным ростом, при росте сдавливают окружающие ткани, но не нарушают ткань в которой растут. Окружающая ткань при их росту атрофируется. Такие опухоли после хирургического удаления не растут повторно. Сильно влияет на организм размер опухоли.
Форма – шаровидная ; консистенция – мягкая или эластичная ; граница – отчетливая ; наличие псевдокапмулы - характерно ; тип, рост – экспансивный ; проростание в соединит. ткани - нет ; некрозы – нет ; метастазы – нет ; множество однотипных образований - нередкость ; рецидивы - бывают.
Существуют классификация и градация опухолей головного мозга, которые достаточно быстро подвергаются изменениям в связи с появлением метода молекулярного профилирования. Несмотря на это, система градации опухолей головного мозга, основанная на гистологических признаках, остается основным средством прогнозирования биологического поведения опухолей. В то время, как предлагается множество различных схем классификации таких новообразований, система классификации и градации опухолей ЦНС, предложенная ВОЗ, является наиболее широко принятой и используется в данной книге.
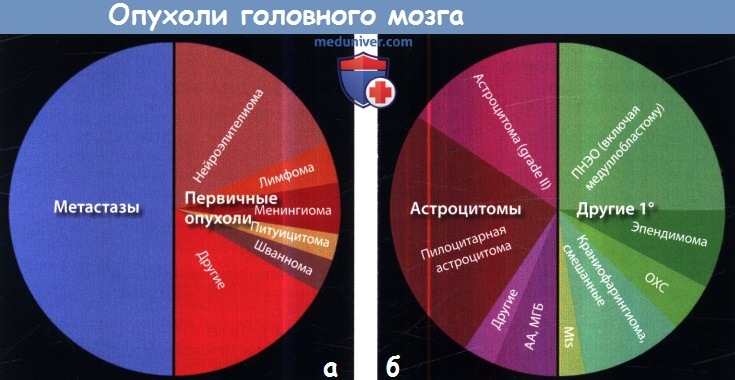
(а) Как видно из диаграммы, встречаемость опухолей головного мозга преобладает у взрослых.
Практически 1/2 опухолей составляют метастатические поражения при раке других локализаций; к другой 1/2 относятся первичные новообразования.
(б) Опухоли головного мозга у детей. Метастазы, анапластическая астроцитома (АА) и мульти-формная глиобластома (МГБ) встречаются редко.
Пилоцитарная астроцитома и примитивные нейроэктодермальные опухоли (ПНЭО) у детей встречаются более часто, чем у взрослых.
ОХС — опухоли хориоидного сплетения.
Классификация/градация новообразований ЦНС:
а) Общие сведения. Новообразования ЦНС подразделяются на первичные и метастатические. Первичные новообразования подразделяются на 6 основных групп. Самой крупной на сегодняшний день является группа нейроэпителиальных опухолей, на втором месте-группа опухолей мозговых оболочек. Опухоли черепных и спинномозговых нервов, лимфомы и гемопоэтические новообразования, а также опухоли зародышевых клеток встречаются менее часто, но являются важными группами.
В последнюю группу первичных новообразований опухоли селлярной области включены исходя из их локализации, а не гистологического типа.
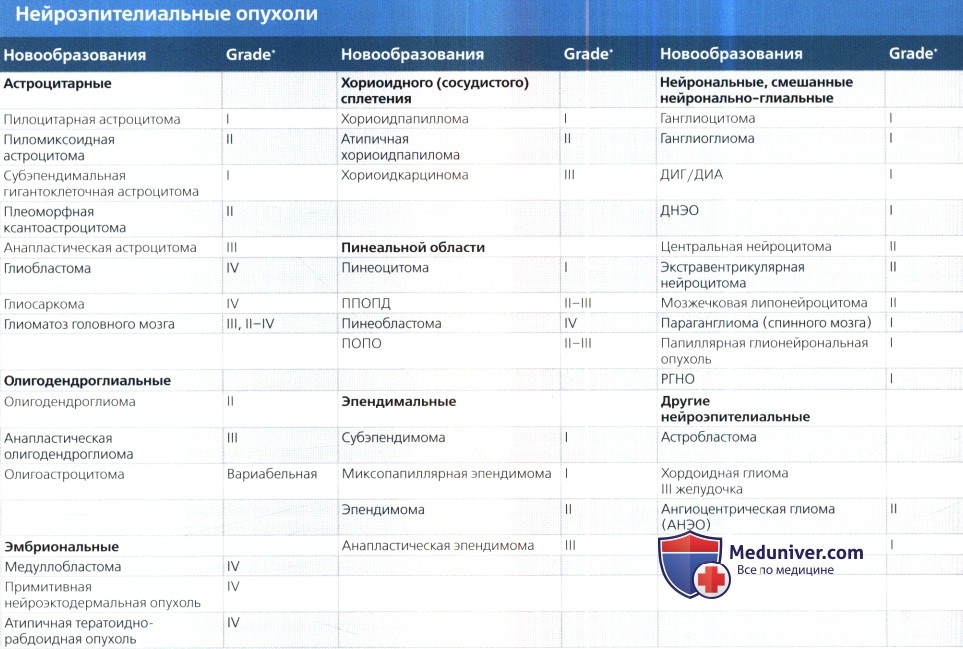
б) Нейроэпителиальные опухоли. Эта группа включает в себя огромное количество опухолей, поэтому она разделена на несколько отдельных подгрупп. Ранее считалось, что такие опухоли возникают из дедифференцированных зрелых нейронов или глиальных клеток (например, астроцитов, олигодендроцитов, эпендимных клеток и т.д.). Но теперь выяснено, что большинство опухолей головного мозга возникают из нервных стволовых клеток.
1. Астроцитомы. Существует множество гистологических типов и подтипов астроцитом, которые выделяют исходя из их биологического поведения: от доброкачественных относительно отграниченных опухолей, таких как пилоцитарная астроцитома (ПА) и субэпендимальная гигантоклеточная астроцитома (СГКА) до высокозлокачественной, характеризующейся диффузным инфильтративным ростом, глиобластомы (МГБ).
Две из локализованных астроцитом (ПА и СГКА) относятся к новообразованиям I степени злокачественности по классификации ВОЗ (grade I). Они не имеют тенденции к злокачественной прогрессии, хотя вариант ПА, называемый пиломиксоидной астроцитомой, может вести себя более агрессивно и классифицируется как опухоль II степени злокачественности (grade II).
Возраст пациента оказывает существенное влияние на тип и локализацию астроцитомы. Например, астроцитомы, характеризующиеся диффузным инфильтративным ростом, наиболее часто локализуются в больших полушариях головного мозга у взрослых, а в мосту мозга - у детей. ПА являются опухолями детей и молодых взрослых. Они часто локализуются в мозжечке и вокруг третьего желудочка, но, при этом, редко встречаются в больших полушариях.
2. Олигодендроглиальные опухоли. Варьируют от диффузно инфильтративных, но относительно хорошо дифференцированных новообразований grade II (олигодендроглиома) до анапластических олигодендроглиом (grade III).
3. Глиомы низкой степени злокачественности (ГНСС). ГНСС были подразделены на три молекулярных подтипа, такая классификация предстает собой надежную неперекрывающуюся, клинически значимую систему, которая превосходит традиционные гистологические методы прогнозирования биологического поведения опухолей. Группа ГНСС основана на определении FISH -статуса (флуоресцентная гибридизация), основанного на анализе 3-х важных генетических маркеров: IDH1, 1р19q (коделеция как 1р, так и 19q) и ATRX (α-талассемия/ген Х-связанного синдрома умственной отсталости).
Для олигодендроглиом характерна коделеция 1р19q, типично ЮН1(+). Ген ATRX не мутирован.
4. Глиомы у детей по сравнению с глиомами у взрослых. У детей глиомы часто генетически отличаются от таковых у взрослых, даже несмотря на то, что они выглядят идентично при микроскопии. Свойственные детям глиомы моста мозга, агрессивные новообразования, которые почти всегда ведут к смертельному исходу, характерны мутации гистона (ИЗ) и гена ACVR1. По сравнению с олигодендроглиомами взрослого возраста, при таких опухолях у детей коделеция 1p19q редка.
5. Эпендимальные опухоли. Эпендимальные новообразования на основании классических гистологических критериев подразделяются на субэпендимомы grade I или миксопапиллярные эпендимомы, эпендимомы grade II (подразделяющиеся в свою очередь на клеточный, папиллярный, светлоклеточный, и таницитарный типы) и grade III (анапластические) эпендимомы.
Профилирование метилирования ДНК позволило недавно выделить девять молекулярных подгрупп эпендимом. Такая молекулярная классификация превосходит современную патогистологическую систему градаций при стратификации риска у пациентов при планировании лечения.
6. Опухоли сосудистого сплетения. Опухоли сосудистого сплетения (ОСС) являются папиллярными внутрижелудочковыми новообразованиями. Почти 80% таких опухолей встречаются у детей. Классически ОСС подразделяются на хориоидпапилломы (ХП) (grade I), атипичные хориоидпапилломы (аХП) (grade III) и хориоидкарциномы (ХК), относящиеся к grade III. Последние геномные исследования показали, что аХП является незрелым вариантом ХП со схожим цитогенетическим профилем и отличающимся лишь более высокой пролиферативной активностью. ХК является генетически обособленной группой опухолей.
ХП встречаются в 5-10 раз чаще, чем ХК. Все виды опухолей сосудистого сплетения могут диффузно распространяться через СМЖ, поэтому перед хирургическим вмешательством необходима визуализация всех структур ЦНС.
7. Другие нейроэпителиальные опухоли. Эти редкие новообразования включают астробластому, хориоидную глиому третьего желудочка и ангиоцентрическую глиому.
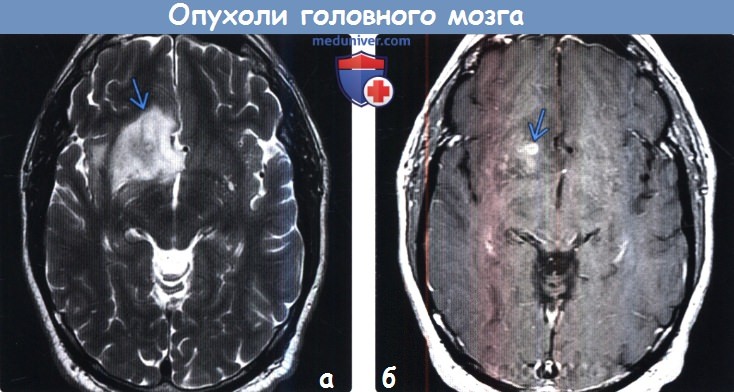
(а) МРТ, Т2-ВИ, аксиальный срез: у мужчины 58 лет, перенесшего два эпизода судорожных приступов, определяется неоднородно гиперинтенсивное объемное образование, инфильтрирующее базальные ганглии, вещество лобной доли, наружную капсулу и заднее бедро внутренней капсулы правого полушария.
(б) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у того же пациента определяется несколько очагов контрастирования в центре объемного образования.
Основываясь на данной локализации (лобная доля) и отсутствии контрастирования обширных зон опухолевого поражения, наиболее вероятно, данная опухоль является вторичной МГБ. При биопсии было выявлено:
IDH 1 (+), EGFR(-), MGMT(+), р53 70%(+), PTEN25%(+) и MIB1 90%.
8. Нейрональные и смешанные нейронально-глиальные опухоли. В данную гетерогенную группу включены нейроэпителиальные опухоли, содержащие ганглиоцитарно-подобные клетки, дифференцированные нейроциты или плохо дифференцированные нейробласты. Также включены ганглиоцитарные новообразования (ганглиоцитома, ганглиоглиома), десмопластическая инфантильная ганглиоглиома или астроцитома (ДИГ/ДИА) вызывающая развитие фиброзной ткани астроцитома (ДИГ/ДИА), нейроцитома (центральный, а также недавно описанный экстравентрикулярный варианты), дисэмбриобластическая нейроэпителиальная опухоль (ДНЭО), папиллярная глионейрональная опухоль, розеткообразующая глионейрональная опухоль (IV желудочка), и мозжечковая липонейробластома.
9. Опухоли пинеальной области. Новообразования пинеальной области составляют 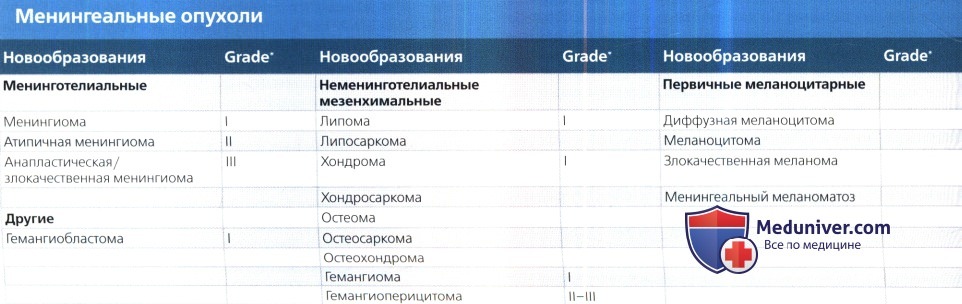
в) Менингеальные опухоли:
1. Обзор. Менингеальные опухоли являются второй по величине группой первичных опухолей ЦНС. Они разделены на менингиомы и мезенхимальные неменинготелиальные опухоли (т.е. опухоли, которые не являются менингиомами). Гемангиоперицитомы, гемангиобластомы и меланоцитарные поражения также рассматриваются в группе менингеальных опухолей.
2. Менингиомы. Менингиомы возникают из менинготелиальных (арахноидальных верхушечных) клеток. Большинство менингиом имеют связь с твердой мозговой оболочкой, но могут имеют и другую локализацию (например, сосудистые сплетения боковых желудочков). В то время как менингиомы подразделяются на большое количество гистологических подтипов (например, менинготелиальный, фиброзный, псаммоматозный, и т.д.), текущая система ВОЗ классифицирует их достаточно просто. Большинство менингиом являются доброкачественными и относятся к опухолям grade I. Атипичная менингиома, а также хориоидальный и светлоклеточный варианты, относятся к опухолям grade II. Анапластическая (злокачественная) менингиома соответствует grade III.
3. Мезенхимальные, неменинготелиальные опухоли. Как доброкачественные, так и злокачественные мезенхимальные опухоли могут возникать и в ЦНС. Наиболее соответствуют опухолям мягких тканей или костей. Обычно встречаются как доброкачественный, так и злокачественный (саркоматозный) типы. К примерам таких опухолей относятся липомы и липосаркомы, хондромы и хондросаркомы, остеомы и остеосаркомы. Гемангиоперицитома (ГПЦ) представляет собой высокоцеллюлярную сосудистую мезенхимальную опухоль, которая практически всегда имеет связь с твердой мозговой оболочкой.
ГПЦ относится к новообразованиям grade II или grade III. Гемангиобластома (ГГБ) является новообразованием grade I, состоящим из стромальных клеток и бесчисленного количества мелких кровеносных сосудов. Она встречается как спорадически, так и в составе синдрома фон Гиппеля-Линдау (ФГЛ). Первичные меланоцитарные новообразования ЦНС встречаются редко. Они возникают из лептоменингиальных меланоцитов и могут иметь как диффузный, так и отграниченный характер роста, могут быть как доброкачественными, так и злокачественными.
г) Опухоли черепных (и спинномозговых) нервов:
1. Шваннома. Шванномы являются доброкачественными, инкапсулированными опухолями оболочек нервов, которые состоят из хорошо дифференцированных шванновских клеток. Они могут быть как одиночными, так и множественными. Множественные шванномы связаны с нейрофиброматозом 2-го типа и шванноматозом, синдромом, характеризующимся множественными шванномами в отсутствие других признаков НФ2. Внутричерепные шванномы практически всегда связаны с черепными нервами (считается, что наиболее часто поражается ЧН VIII), но иногда возникают как паренхимальные поражения. Шванном не подвергаются злокачественной дегенерации и относятся к новообразованиям grade I.
2. Нейрофиброма. Нейрофибромы (НФ) являются диффузно инфильтративными, экстраневральными опухолями, состоящими из шванновских клеток и фибробластов. Встречаются одиночные нейрофибромы кожи головы. Множественные НФ или плексиформные НФ встречаются в составе нейрофиброматоза 1 -го типа. Нейрофибромы гистологически соответствуют опухолям grade I. Плексиформные нейрофибромы могут дегенерировать в злокачественные опухоли оболочек периферических нервов (ЗООПН). ЗООПН градируются от II до IV степенями злокачественности по классификации ВОЗ, что аналогично подходу градации саркомы.
д) Лимфомы и гемопоэтические опухоли. Первичная лимфома ЦНС. Первичные лимфомы ЦНС (ПЛЦНС) очень часто развиваются в результате ВААРТ терапии у пациентов с ВИЧ/СПИД, а также у других страдающих иммунодефицитом больных. ПЛЦНС может быть как фокальной интрапаренхимальной, так и интраваскулярной опухолью. Кроме того, ПЛЦНС может быть как одиночной, так и множественной. Наиболее частой локализацией являются большие полушария головного мозга. Более 95% ПЛЦНС являются диффузными В-крупноклеточными лимфомами.
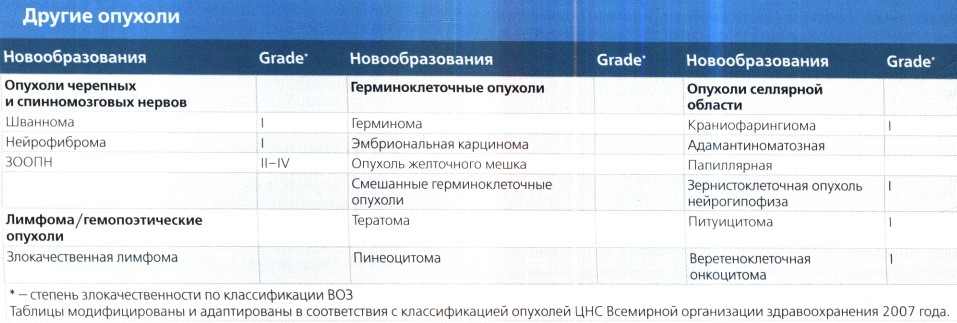
е) Опухоли зародышевых клеток. Внутричерепные опухоли зародышевых клеток (ОЗК) морфологически гомологичны герминальным новообразованиям, которые возникают в гонадах, а также имеют внегонадную локализацию. 80-90% таких опухолей встречаются у подростков. Большинство локализуются по средней линии (область эпифиза, вокруг третьего желудочка).
ж) Опухоли селлярной области:
1. Краниофарингиома. Краниофарингиома - доброкачественная (grade I), часто имеющая кистозный компонент, опухоль, являющаяся наиболее частым ненейроэпительальным внутричерепным новообразованием у детей. С этим связана ярко выраженное бимодальное распределение по возрасту: кистозный адамантиноматозный тип чаще всего наблюдаются у детей, а второй, меньший пик встречаемости опухоли наблюдается у людей среднего возраста. Реже встречается папиллярный тип опухолей, которые обычно имеют солидный характер и обнаруживаются практически исключительно у взрослых.
2. Другие опухоли селлярной области. Гранулоцитарная опухоль нейрогипофиза является редкой опухолью взрослого возраста, которая, как правило, произрастает из воронки гипофиза. Питуицитомы являются глиальными новообразованиями взрослого возраста, которые обычно также произрастают из воронки гипофиза. Веретеноклеточная онкоцитома аденогипофиза является неэндокринным новообразованием аденогипофиза. Все эти редкие опухоли имеют I степень злокачественности по классификации ВОЗ (grade I).
Редактор: Искандер Милевски. Дата публикации: 27.3.2019
Опухоль - это избыточное, продолжающееся после прекращения действия вызывающих его причин, некоординированное с организмом, патологическое возрастание ткани, состоящая из клеток, ставших атипичными в отношении дифференцировки и характера роста и передающих эти свойства своим потомкам (Л.М. Шабад).
Опухоли бывают доброкачественными и злокачественными.
Доброкачественная опухоль растет экспансивно, раздвигая, сдавливая, но не разрушая здоровые ткани.
Для злокачественногороста характерен инфильтративный, деструктивный рост, завершающийся разрушением здоровых тканей.
*Опухолям и опухолевым клеткам независимо от вызвавшей их причин, локализации и гистогенеза присущи особенности (атипизм), отличающие их от нормальных клеток и тканей.
Все разновидности атипизма можно разделить на 2 вида:
- характерные для добро- и злокачественных опухолей;
-характерные только для злокачественных опухолей.
К первому типу относятся:
1. Атипизм размножения и дифференцировки.
2. Морфологический атипизм.
3. Биохимический атипизм.
4. Физико-химический атипизм.
5. Антигенный атипизм.
6. Функциональный атипизм.
Только злокачественному росту присущи:
1. Инфильтративный (инвазивный, деструктивный) рост.
Атипизм размножения – заключается в том, что опухолевые клетки обладают относительной автономностью и слабо поддаются регулирующим влияниям со стороны организма. Это обусловлено прежде всего нарушением контактного торможения деления осуществляемого соседними клетками.Нарушается и процесс дифференцировки клеток, что проявляется частичным или полным торможением их созревания.
Морфологический атипизм– включает в себя:
1) – нарушение структуры ткани (тканевый атипизм) и
2) – клеток (клеточный атипизм).
* Тканевый атипизм выражается нарушением в ткани опухоли стромально- паренхиматозных соотношений, изменением расположения сосудов, нервных волокон, цитоархитектоники.
* Клеточный атипизмпроявляется клеточным полиморфизмом (изменение ядер по форме и размерам);
увеличением ядерно-цитоплазматического состояния; увеличением размеров и числа ядрышек; увеличением количества рибосом; уменьшением количества митохондрий; появлением различных по величине и форме митохондрий; увеличением числа митозов; изменением числа, формы и размеров хромосом (хромосомные аберрации); увеличением поверхности клеток за счет пластинчатых выростов.
Биохимический атипизм- характеризуется изменением основных биохимических процессов в опухолях и, прежде всего, вследствии утраты такими клетками ряда ферментов, необходимых для выполнения специфических функций.
1. Опухолевая клетка получает энергию (АТФ) преимущественно за счет анаэробного гликолиза (брожения), причем и в присутствии кислорода в ней продолжается интенсивное образование молочной кислоты (так называемый, отрицательный эффект Пастера), тогда как обычно в аэробных условиях клетка получает энергию прежде всего за счет процессов тканевого дыхания (аэробного окисления), а гликолиз заторможен (так называемый, положительный эффект Пастера). Это свойство опухолевых клеток обепечивает им высокую устойчивость и выживаемость в условиях гипоксии.
2. В опухолевой ткани существенно изменен обмен белков и углеводов.
- Основными проявлениями физико-химического атипизма являются:
1. Наличие в опухолевой ткани содержания молочной кислоты и концентрации водородных ионов (ацидоз), прежде всего, в зоне интенсивного деления клеток.
2. Увеличение поверхностного отрицательного заряда опухолевой клетки.
3. В опухолевых клетках увеличивается количество воды и ионов калия, уменьшается количество кальция и магния.
Гидратация клетки повышает электропроводимость и снижает вязкость клеточных коллоидов. Снижение кальция приводит к уменьшению сцепления между клетками, что облегчает отрыв и миграцию клеток, метастазирование и инвазивный рост.
- Функциональный атипизмпроявляется:
1. Частичной или полной утратой опухолевой тканью способности выполнять свои специфические функции.
2. Может наблюдаться повышенное, по сравнению с нормой, выделение опухолевыми клетками веществ, подчас обладающих высокой биологической активностью (например, гормонов).
3. опухолевые клетки могут синтезировать и секретировать вещества, не свойственные клеткам тканей, из которых они произошли.
- Инфильтративный (инвазивный) рост связан со способностью опухолевых клеток прорастать ткани (это присуще только злокачественным опухолям). Такой рост обусловлен изменениями мембран опухолевых клеток, нарушением межклеточного взаимодействия и контактного ингибирования.
Метастазирование - это свойство опухолевых клеток отделяться от первичного узла, распространяться по организму и вызывать образование новых, вторичных опухолевых узлов. Распространение опухолевых клеток может идти по лимфогенным, гематогенным и имплантационным (непосредственный переход этих клеток с поверхности опухоли на контактирующие органы и ткани, например, с верхней губы на нижнюю) путями.
Рецидивирование – это возврат, повторное появление опухоли по гистологическому строению идентичной той, которая была удалена ранее каким-либо способом (хирургическим, химиотерапией, лучевой терапией).
Раковая кахексия – симптокомплекс, развивающийся при злокачественном росте и характеризуется истощением и общей слабостью организма.
В клинической работе чрезвычайно важно отличать истинные опухоли от неопухолевых процессов, сопровождающихся изменением объема, массы и структуры тканей и органов.
Учение о новообразованиях представляет собой важнейшую часть более широкой патофизиологической доктрины, описывающей причины и механизмы избыточною или недостаточного роста и размножения клеток — то есть гипербиотических и гипобиотических процессов соответственно.
Гипо- и гипербиотические процессы
Атрофия — уменьшение объема клеток и их числа вследствие превышения скорости гибели клеток над темпами их размножения, приводящее к уменьшению веса и объема органов (тканей) и развитию соответствующей гипофункции. При атрофии происходит усиление интенсивности апоптоза и аутофагоцитоза.
Атрофия — важный адаптационный механизм — лежит в основе рассасывания провизорных органов плода, регрессии гиперплазированных органов, связанных с беременностью, лактацией, натуральными биоритмами и возрастом (инволюционная физиологическая атрофия).
Если гипобиотический процесс, аналогичный атрофии, носит врожденный характер, то он именуется гипоплазией. Гипоплазия чаще касается отдельных органов (например, костной системы — при хондродисплазии), но может относиться и ко всему телу (гипофизарный нанизм). Крайне выраженная гипоплазия, когда имеется лишь органный зачаток, известна под названием аплазии, а если отсутствует и органный зачаток, то это состояние называют агенезией (пример - агенезия почки).
Гипербиотические процессы представляют собой избыточное образование клеток или увеличение их размеров. В организме они представлены гипертрофией, гиперплазией, регенерацией и опухолевым ростом.
Гипертрофия — компенсаторно-приспособительный процесс, индуцированный избытком ростостимулирующих и/или дефицитом ростингибирующих факторов, увеличения размеров клеток и числа функционирующих внутриклеточных структур с соответствующим увеличением размеров и функциональных возможностей органов.
Гиперплазия — адаптационное или патологическое увеличение числа нормальных клеток в органах и тканях и, соответственно, — их размеров. Гиперплазия обратима, дифференцировка клеток и тканевая структура органа при этом остаются нормальными, клетки по-прежнему чувствительны к регуляторным сигналам, или, говоря иначе, остаются под контролем организма.
Гиперплазия может наступать вместе с гипертрофией, под воздействием избытка ростостимулирующих и/или устранения ростингибирующих сигналов. Гиперплазия бывает физиологической и патологической.
Примером гормональной физиологической гиперплазии может служить пролиферация эпителиальных структур в молочной железе во время беременности. Патологическая гиперплазия также обычно является следствием избыточной гормональной стимуляции или воздействия факторов роста на клетки-мишени.
Одним из примеров дисгормональной патологической гиперплазии является железистая гиперплазия эндометрия при высоком уровне эстрогенов. Примером гиперплазии может служить также зоб, когда в условиях гипотиреоза наступает компенсаторная гиперплазия щитовидной железы.
Регенерация
Гипертрофия и гиперплазия составляют основу для такого гипербиотического процесса как регенерация. Регенерацией называется возрождение (восстановление) утраченных тканей, органов и отдельных частей организма Она может быть физиологической (в процессе самообновления тканей) и патологической (при убыли клеток из-за повреждения).
Процессы регенерации присущи всем живым существам, но чем сложнее животные, гем способность к полной (с правильной дифференцировкой и восстановлением исходной ткани) регенерации меньше. У человека регенерируют лишь части органов и тканей, но чаще имеет место неполная регенерация в виде рубцевания.
Рубцевание (или фиброплазия) — это возникновение регенерата, представленного в основном соединительной тканью (например, заживление ран вторичным натяжением). Наиболее хорошо регенерируют эпителиальная и соединительная ткани. Разновидностью неполной регенерации считается метаплазия.
Метаплазия — процесс, при котором одна вполне дифференцированная ткань замещается другой вполне дифференцированной в пределах одного гистиотипа: либо эпителиального, либо мезенхимального (нервным и мышечным тканям метаплазия не свойственна). Метаплазия обычно является реакцией на повреждающие воздействия и носит приспособительный характер. Иногда метаплазию рассматривают как неполную регенерацию с отклонением в дифференцировке клеток органа или ткани.
При метаплазии камбиальные клетки дифференцируются не в характерные, а в иные, не типичные для органа, но вполне зрелые клетки Чаще всего наблюдается замещение однослойного призматического или цилиндрического эпителия на многослойный плоский при хроническом раздражении или воспалении. Например, очаги плоскоклеточной метаплазии часто формируются в бронхах при хроническом бронхите или как реакция на курение.
Считается, что многослойный плоский эпителии более устойчивый и лучше приспособленный к выживанию при воздействии неблагоприятных факторов.
Иногда метаплазия имеет обратную направленность — от плоского эпителия к цилиндрическому. В частности, это наблюдается при так называемом пищеводе Барретта, когда на фоне длительно существующего рефлюкс-эзофагита отмечается метаплазия плоского эпителия нижней трети пищевода в эпителий кишечного типа.
Явление метаплазии само по себе не носит опухолевого характера, однако известно, что рак на фоне пищевода Барретта развивается в 30-40 раз чаще, чем у здоровых лиц
Более того, развивающаяся при наличии метаплазии опухоль обычно имеет строение аденокарциномы, что вообще для рака пищевода не характерно. Примером метаплазии мезенхимальных тканей может служить гетеротопическое костеобразование, когда клетки волокнистой соединительной ткани трансформируются в остеобласты и продуцируют кость там, где в норме ее никогда не бывает.
Принято считать, что метаплазия обратима, а клетки, подвергшиеся этому процессу, не проявляют признаков нарушения нормальных межклеточных взаимоотношений, то есть при метаплазии нет признаков тканевого атипизма.
В большинстве случаев, нет прямой связи между метаплазией и раком. Однако в метапластических участках могут в последующем появляться признаки дисплазии (см ниже). В этом случае определяется повышенный риск возникновения рака. Поэтому метаплазия обычно рассматривается не как предопухолевый, а как фоновый процесс.
Дисплазия — (в переводе с греч. — отклонение в формировании) — характеризуется частичной потерей кош роля за дифференцировкой клеток. Вследствие лого появляются признаки атипии клеток и ткани. Дисплазия частично обратима.
Для нее нехарактерен избыточный рост ткани, но частота возникновения опухолей соответствующей локализации повышена. В некоторых случаях диспластическая стадия в развитии рака очень четко очерчена, присоединяется к гиперплазии или метаплазии и имеет большое значение при скрининге и диспансеризации.
Таковы, например, дисгормональные пролифераты молочных желез, матки и простаты, аденоматозные полипы желудка и толстой кишки, дисплазии эпителия бронхов, папилломы мочевою пузыря. В связи с этими особенностями, дисппазию характеризуют как предопухолевый рост.
Общие сведения об опухолях
Опухоль (новообразование) — продукт неопластического роста — является разновидностью гипербиотического процесса. Единого, общепринятого определения опухопевою роста нет до настоящего времени, что объясняется сложностью и многообразием нонсюбразовании.
В разные исторические периоды опухоль определяли по-разному. М.А. Пальцев, Н.М. Аничков (2001) считают, что целесообразно придерживаться следующего определения: опухоль — это патологический процесс, представленный новообразованной тканью, в которой изменения генетического аппарата клеток приводят к нарушению регуляции их роста и дифференцировки.
При локальном прогрессирующем увеличении объема участка органа или ткани за счет роста числа клеток в нем опухоли называются первично-локализованными (в виде узла).
Однако при лейкозах опухолевые клетки расселены по организму и обнаруживаются в кроветворных органах, крови, а иногда — в других тканях, причем узловые локальные образования могут отсутствовать из-за того, что ткань костного мозга представляет собой суспензию.
Такие опухолевые процессы называются первично-системными, т.е. возникающими в разных участках одной (лимфоидной) системы Как и в нормальных органах, строма любого новообразования (кроме лейкозов), — это в основном опорная и снабжающая фиброваскулярная ткань, не являющаяся носительницей опухолевых свойств, а паренхима — это профильная ткань, сосредоточие ее фенотипа. Кроме того, различают опухоли первично-множественные, мультифокальные, билатеральные.
Мультифокальные (мультицентрические) — это множественные опухоли одинаковой гистологической структуры в одном и том же органе; билатеральные опухоли — опухоли в парных органах (например, в почках) одинаковой гистологической структуры.
По течению и прогнозу для здоровья и жизни ее носителя существует деление опухолей на злокачественные и доброкачественные. Последние имеют гораздо лучший прогноз
Следовательно, подобная классификация является практической, а не строго научной и определяется клиническим течением опухоли и ее морфологической характеристикой. При диагностике задача состоит в том, чтобы максимально объективно оценить морфологическое строение и особенности роста опухоли, с одной стороны, и все детали клиническою плана — с другой.
Доброкачественные опухоли морфологически соответствуют зрелым опухолям, четко отграничены от окружающих тканей, имеют обычно форму узла или полипа (на слизистой оболочке), характерен медленный экспансивный или раздвигающий (а не инфильтрирующий) рост, не дают метастазов и не рецидивируют.
Нередко они вообще могут прекращать свой рост, претерпевая инволюционные изменения При своем росте опухоли раздвигают окружающие ткани, иногда сдавливают их, но, обычно, не повреждают: в некоторых случаях инкапсулируются.
Доброкачественные опухоли, как правило, не оказывают выраженного неблагоприятного воздействия на организм. Однако понятие доброкачественности является относительным.
Например, доброкачественные опухоли тонкой кишки (лейомиомы) больших размеров, сдавливая петли, могут вызывать некроз кишечника; неинвазивно растущая и неметастазирующая опухоль внутри черепа но чисто механическим последствиям может быть фатальной для больного.
Доброкачественные опухоли также могут угрожать жизни больного, если они вызывают эндокринные нарушения (например, гормонально активные аденомы надпочечников).
Злокачественные опухоли соответствуют незрелым опухолям, имеют характерные морфологические признаки, растут быстро, инвазивно (то есть с прорастанием и замещением окружающих тканей), способны к диссеминации и метастазируют.
В финале своего развития неоплазма может разрушать жизненно важные органы и целые системы организма. Но понятие злокачественности также относительное. Некоторые злокачественные опухоли несмотря на способность к метастазированию. имеют относительно доброкачественное течение, обладая низким метастатическим потенциалом и менее выраженными инвазивными свойствами.
Так, папиллярный рак щитовидной железы даже при наличии отдаленных метастазов успешно лечится и обладают лучшим прогнозом по сравнению с другими типами рака этого органа.
Считается, что единственный абсолютный признак злокачественности — метастазирование. Но практически важно уметь оценить степень риска, вызываемого опухолью, до появления метастазов. Поэтому принимают во внимание и другие признаки злокачественности, более или менее тесно связанные с метастатическими потенциями: скорость роста опухоли и ее размер, степень атипизма и т.д.
Считается, например, что карциноид аппендикса должен быть больше 2 см в диаметре, чтобы подпадать под критерий злокачественности, так как известно, что опухоли этого типа при меньших размерах метастазируют редко. Однако, не метастазируют и многие крупные карциноиды. У многиx злокачественных опухолей нет капсулы, но нет ее и у карциноидов, дерматофибром и других доброкачественных опухолей.
Таким образом, точка зрения, жестко разграничивающая доброкачественные и злокачественные новообразования, не получила достаточного обоснования, так как онкогены активированы в обеих типах опухолей. Речь может идти только о разном количестве и степени их активации и о различной степени сохранности активности антионкогенов. Именно в связи с этим имеется много промежуточных вариантов опухолей.
Вместе с тем, есть ряд критериев, которые позволяют с определенной степенью достоверности разделять их на две основные группы. Так, для доброкачественных опухолей характерен только тканевой атипизм (изменения пространственных и количественных взаимоотношений между компонентами ткани: стромой, сосудами и паренхимой).
У злокачественных опухолей присутствует атипизм и тканевой, и клеточный. У злокачественных новообразовании больше выражен биохимический (метаболический) и иммунопотический атипизм, что закономерно сопровождается развитием в организме носитепя паранеоплазий. Некоторые дополнительные, относительные разграничительные признаки двух типов опухолей, представлены в таблице 6.1.
Таблица 6.1. Относительные критерии доброкачественности и злокачественности опухолей [Зайчик А.Ш., Чурилов Л.П., 2002]. 
Вопрос о возможности озлокачествлении доброкачественных опухолей решается неоднозначно. Механизмы нарушения регуляции роста и течения доброкачественных и злокачественных опухолей отличаются друг от друга качественно, что связано с различиями их гено- и фенотипа.
Однако чаще доброкачественные опухоли непосредственно в злокачественные не переходят. Как правило, злокачественная опухоль формируется в доброкачественной заново, на основе появления нового, активированного онкогенами клона. Но есть и исключения — так, нейрофиброма может трансформироваться в злокачественную опухоль, аденоматозный полип толстой кишки и кератопапилпома, при достаточной длительности существования — в рак.
Очевидно, для такой трансформации необходимы дополнительный мутации. Принципиально, возможна спонтанная регрессия опухолей, гораздо чаще при их доброкачественном характере и очень редко — при злокачественном. Лишь как исключение указывают на возможность спонтанного приобретения признаков дифференцировки клетками некоторых злокачественных опухолей и чуть пи не единственным, традиционно приводимым примером служит нейробластома.
Кроме доброкачественных и злокачественных опухолей выделяются новообразования с местнодеструирующим ростом и потенциально злокачественные (или опухоли неопределенной степени злокачественности). Это неясная в плане адекватности лечения и прогнозирования группа опухолей по клинико-морфологическим признакам является неоднородной и до настоящего времени недостаточно изученной.
Местнодеструирующие опухоли часто называют третьим (промежуточным) видом новообразовании. Гистологически они проявляются выраженной пролиферацией клеточных элементов.
Для местнодеструирующих опухопей, как и для злокачественных, характерен инфильтрирующий рост, и даже после их радикального удаления часто возникают рецидивы.
Однако они никогда не озлокачествляются и не обладают способностью к метастазированию. Типичными представителями местнодеструирующих опухолей принято считать базалиому (базальноклеточный рак) кожи, цесмоид, миксому, плеоморфную аденому слюнной железы (смешанную опухоль).
Опухоли неопределенной степени злокачественности или потенциально злокачественные при морфологических признаках доброкачественности иногда могут метастазировать.
Если подходить строго, то правильнее их расценивать как доброкачественные новообразования, имеющие своеобразные черты роста и клинического течения. Среди них можно назвать карциноиды тонкой кишки, гигантоклеточная опухоль кости (остеобластокластома) и др.
В таблице 6.2. представлен перечень наиболее часто встречающихся опухолей неопределенной степени злокачественности и с неустановленным прогнозом.
Таблица 6.2. Перечень опухолей неопределенной степени злокачественности
[Колосов А.Е. и соавт., 1990]. 
Биологическое поведение опухолей, т.е. скорость роста, способность к инфильтрирующему росту, метастазированию, определяется не только морфологическими признаками атипии, но и происхождением гистогенезом опухоли.
При доброкачественных опухолях установление их гистогенеза не представляет трудностей. Однако определить происхождение низкодифференцированных злокачественных опухолей по гистоструктуре удается далеко не всегда. В настоящее время признано, что наиболее точно гистогенез опухоли устанавливается при иммуногистохимических исследованиях.
Накопленный опыт морфологического анализа опухолей в сочетании с клиническими данными говорит в пользу того, что именно с позиций конкретного органа или ткани и с точки зрения нозологических форм, которые типичны для этой локализации, нужно исходить для правильной ориентировки в особенностях течения опухолевою процесса и прогноза ею у конкретного больного.
Угляница К.Н., Луд Н.Г., Угляница Н.К.
Читайте также:

