Бензол может реагировать с хлором с раствором перманганата калия
- Строение, номенклатура, изомерия
- Способы получения
- Химические свойства
Первая группа реакций реакции замещения. Мы говорили, что арены не имеют кратных связей в структуре молекулы, а содержат сопряженную систему из шести электронов, которая очень стабильна и придает дополнительную прочность бензольному кольцу. Поэтому в химических реакциях происходит в первую очередь замещение атомов водорода, а не разрушение бензольного кольца.
С реакциями замещения мы уже сталкивались при разговоре об алканах, но для них эти реакции шли по радикальному механизму, а для аренов характерен ионный механизм реакций замещения.
Первое химическое свойство галогенирование. Замещение атома водорода на атом галогена хлора или брома.
Реакция идет при нагревании и обязательно с участием катализатора. В случае с хлором это может быть хлорид алюминия или хлорид железа три. Катализатор поляризует молекулу галогена, в результате чего происходит гетеролитический разрыв связи и получаются ионы.
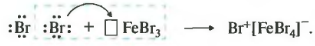
Положительно заряженный ион хлора и вступает в реакцию с бензолом.
Если реакция происходит с бромом, то катализатором выступает бромид железа три или бромид алюминия.

Важно отметить, что реакция происходит с молекулярным бромом, а не с бромной водой. С бромной водой бензол не реагирует.
У галогенирования гомологов бензола есть свои особенности. В молекуле толуола метильная группа облегчает замещение в кольце, реакционная способность повышается, и реакция идет в более мягких условиях, то есть уже при комнатной температуре.
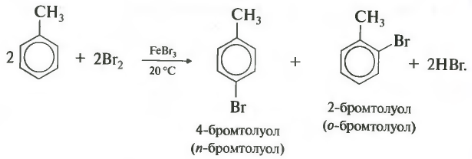
Важно отметить, что замещение всегда происходит в орто- и пара-положениях, поэтому получается смесь изомеров.
Второе свойство нитрование бензола, введение нитрогруппы в бензольное кольцо.
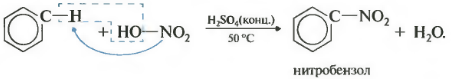
Образуется тяжелая желтоватая жидкость с запахом горького миндаля нитробензол, поэтому реакция может быть качественной на бензол. Для нитрования используется нитрующая смесь концентрированной азотной и серной кислот. Реакция проводится при нагревании.
Напомню, что для нитрования алканов в реакции Коновалова использовалась разбавленная азотная кислота без добавления серной.
При нитровании толуола, также как и при галогенировании, образуется смесь орто- и пара- изомеров.
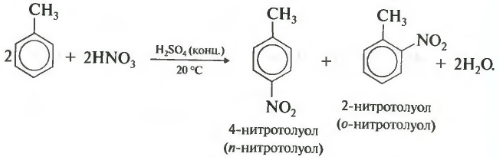
Третье свойство алкилирование бензола галогеналканами.
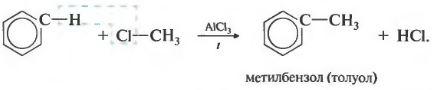
Эта реакция позволяет ввести углеводородный радикал в бензольное кольцо и может считаться способом получения гомологов бензола. В качестве катализатора используется хлорид алюминия, способствующий распаду молекулы галогеналкана на ионы. Также необходимо нагревание.
Четвертое свойство алкилирование бензола алкенами.
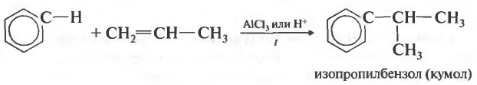
Таким способом можно получить, например, кумол или же этилбензол. Катализатор хлорид алюминия.
Вторая группа реакций реакции присоединения. Мы говорили, что эти реакции не характерны, но они возможны при достаточно жестких условиях с разрушением пи-электронного облака и образованием шести сигма-связей.
Пятое свойство в общем списке гидрирование, присоединение водорода.
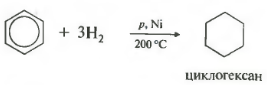
Температура, давление, катализатор никель или платина. Таким же образом способен реагировать толуол.
Шестое свойство хлорирование. Обратите внимание, что речь идет именно о взаимодействии с хлором, поскольку бром в эту реакцию не вступает.
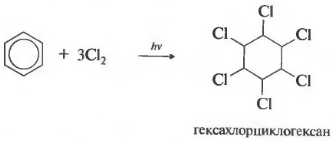
Реакция протекает при жестком ультрафиолетовом облучении. Образуется гексахлорциклогексан, другое название гексахлоран, твердое вещество.
Важно помнить, что для бензола не возможны реакции присоединения галогеноводородов (гидрогалогенирование) и присоединение воды (гидратация).
Третья группа реакций касается только гомологов бензола это замещение в боковой цепи.
Седьмое свойство в общем списке галогенирование по альфа-атому углерода в боковой цепи.
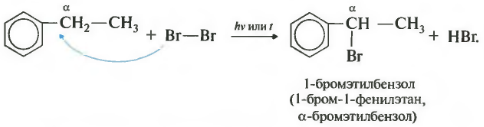
Реакция происходит при нагревании или облучении и всегда только по альфа-углероду. При продолжении галогенирования, второй атом галогена снова встанет в альфа-положение.
Четвертая группа реакций окисление.
Бензольное кольцо слишком прочное, поэтому бензол не окисляется перманганатом калия не обесцвечивает его раствор. Это очень важно помнить.
Зато гомологи бензола окисляются подкисленным раствором перманганата калия при нагревании. И это восьмое химическое свойство.
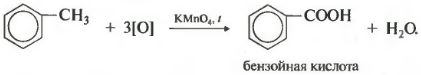
Получается бензойная кислота. Наблюдается обесцвечивание раствора. При этом, какой бы длинной не была углеродная цепь заместителя, всегда происходит ее разрыв после первого атома углерода и альфа-атом окисляется до карбоксильной группы с образованием бензойной кислоты. Оставшаяся часть молекулы окисляется до соответствующий кислоты или, если это только один атом углерода, до углекислого газа.
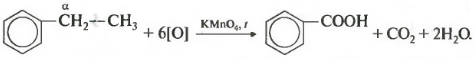
Если гомолог бензола имеет больше одного углеводородного заместителя у ароматического кольца, то окисление происходит по тем же правилам окисляется углерод, находящийся в альфа-положении.
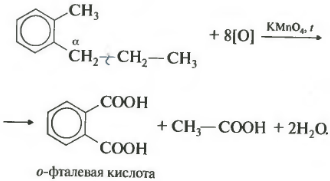
В данном примере получается двухосновная ароматическая кислота, которая называется фталевая кислота.
Особым образом отмечу окисление кумола, изопропилбензола, кислородом воздуха в присутствии серной кислоты.
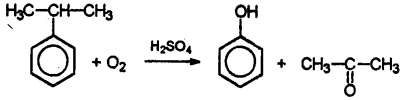
Это так называемый кумольный способ получения фенола. Как правило, сталкиваться с этой реакцией приходится в вопросах, касающихся получения фенола. Это промышленный способ.
Девятое свойство горение, полное окисление кислородом. Бензол и его гомологи сгорают до углекислого газа и воды.
Запишем уравнение горения бензола в общем виде.

По закону сохранения массы атомов слева должно быть столько же, сколько атомов справа. Потому что ведь в химических реакциях атомы никуда не деваются, а просто изменяется порядок связей между ними. Так вот молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле арена, поскольку в состав молекулы входит один атом углерода. То есть n молекул CO2. Молекул воды будет в два раза меньше, чем атомов водорода, то есть (2n-6)/2, а значит n-3.
Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа, потому что в каждой молекуле два атома кислорода, плюс n-3 из воды, итого 3n-3. Слева атомов кислорода столько же 3n-3, а значит молекул в два раза меньше, потому как в состав молекулы входят два атома. То есть (3n-3)/2 молекул кислорода.
Таким образом, мы составили уравнение сгорания гомологов бензола в общем виде.
Арены - ароматические углеводороды, содержащие одно или несколько бензольных колец. Бензольное кольцо составляют 6 атомов углерода, между которыми чередуются двойные и одинарные связи.
Важно заметить, что двойные связи в молекуле бензола не фиксированы, а постоянно перемещаются по кругу.
Арены также называют ароматическими углеводородами. Первый член гомологического ряда - бензол - C6H6. Общая формула их гомологического ряда - CnH2n-6.
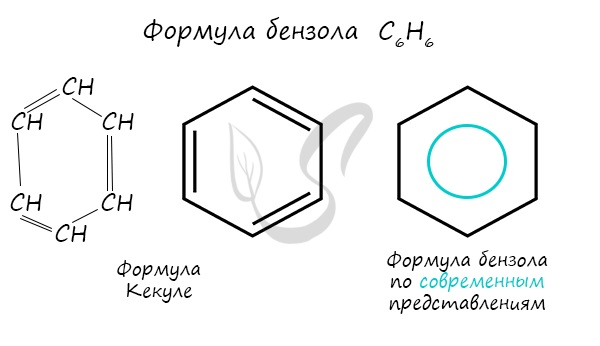
Долгое время структурная формула бензола оставалась тайной. Предложенная Кекуле формула с двумя тройными связями не могла объяснить то, что бензол не вступает в реакции присоединения. Как уже было сказано выше, по современным представлениям, двойные связи в молекуле постоянно перемещают, поэтому правильнее рисовать их в виде кольца.
За счет чередования двойных связей в молекуле бензола формируется сопряжение. Все атомы углерода находятся в состоянии sp 2 гибридизации. Валентный угол - 120°.
Названия аренов формируются путем добавления названий заместителей к главной цепи - бензольному кольцу: бензол, метилбензол (толуол), этилбензол, пропилбензол и т.д. Заместители, как обычно, перечисляются в алфавитном порядке. Если в бензольном кольце несколько заместителей, то выбирают кратчайший путь между ними.
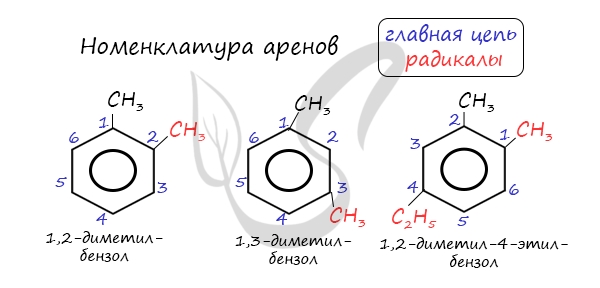
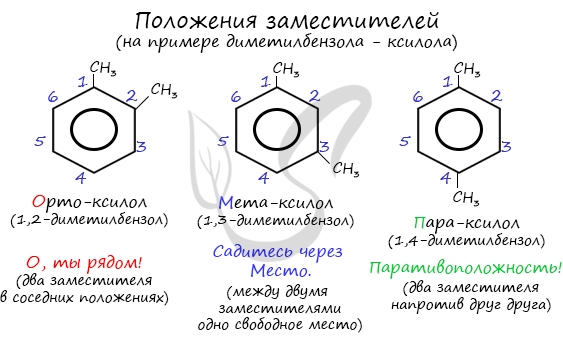
Для аренов характерна структурная изомерия, связанная с положением заместителей. Например, два заместителя в бензольном кольце могут располагаться в разных положениях.
Название положения заместителей в бензольном кольце формируется на основе их расположения относительно друг друга. Оно обозначается приставками орто-, мета- и пара. Ниже вы найдете мнемонические подсказки для их успешного запоминания ;)
Арены получают несколькими способами:
-
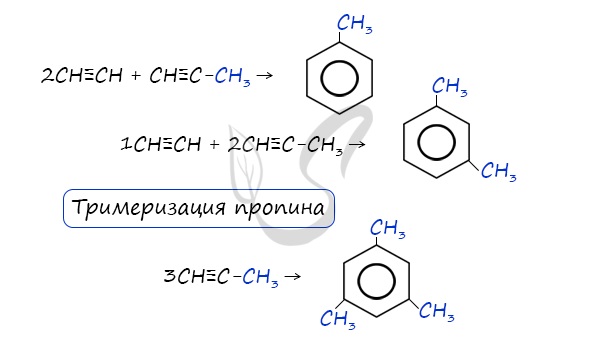
Реакция Зелинского (тримеризация ацетилена)
Данная реакция протекает при пропускании ацетилена над активированным углем при t = 400°C. В результате образуется ароматический углеводород - бензол.

В случае, если к ацетилену добавить пропин, то становится возможным получение толуола. Увеличивая долю пропина, в конечном итоге можно добиться образования 1,3,5-триметилбензола.
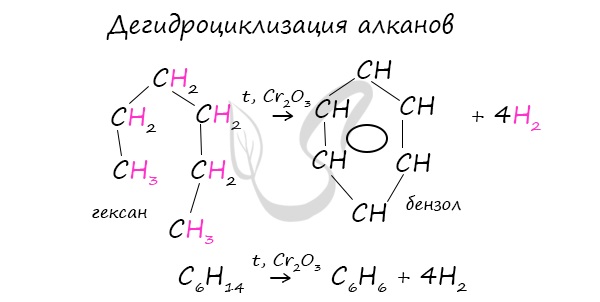
В ходе таких реакций, протекающих при повышенной температуре и в присутствии катализатора - Cr2O3, линейная структура алкана замыкается в цикл, отщепляется водород.
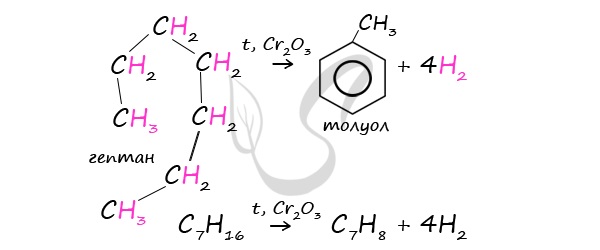
При дегидроциклизации гептана получается толуол.
В результате дегидрирования уже "готовых" циклов - циклоалканов, отщепляются 3 моль водорода, и образуется соответствующий арен, с теми же заместителями, которые были у циклоалкана.

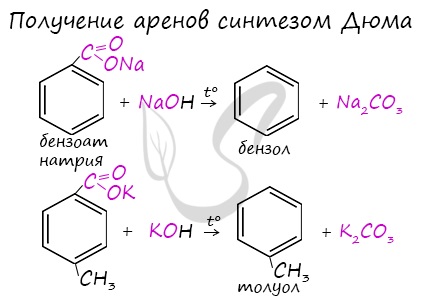
Синтез Дюма заключается в сплавлении солей карбоновых кислот с щелочами. В результате такой реакции возможно образование различных органических веществ, в том числе аренов.
Арены - ароматические углеводороды, которые содержат бензольное кольцо с сопряженными двойными связями. Эта особенность делает реакции присоединения тяжело протекающими (и тем не менее возможными!)
Запомните, что, в отличие от других непредельных соединений, бензол и его гомологи не обесцвечивают бромную воду и раствор перманганата калия.
При повышенной температуре и наличии катализатора, водород способен разорвать двойные связи в бензольном кольце и превратить арен в циклоалкан.

Реакция бензола с хлором на свету приводит к образованию гексахлорциклогексана, если же использовать только катализатор, то образуется хлорбензол.
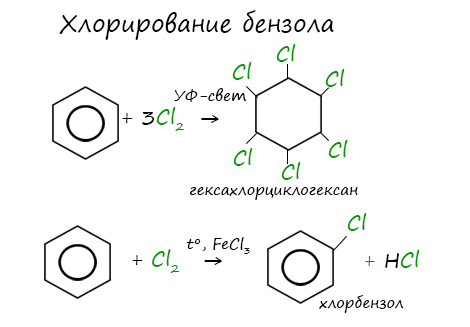
Реакции с толуолом протекают иначе: при УФ-свете хлор направляется в радикал метил и замещает атом водорода в нем, при действии катализатора хлор замещает один атом водорода в бензольном кольце (в орто- или пара-положении).
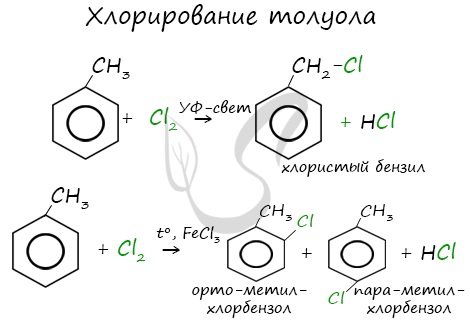
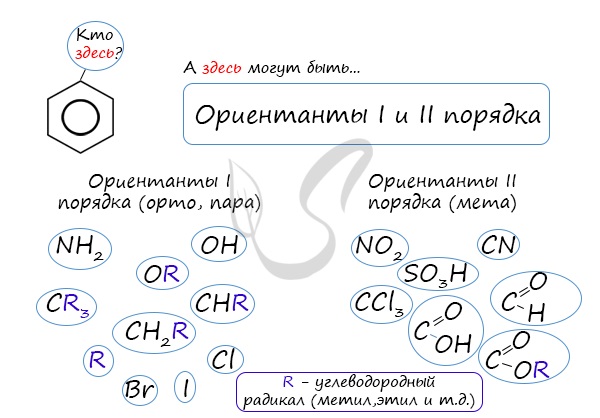
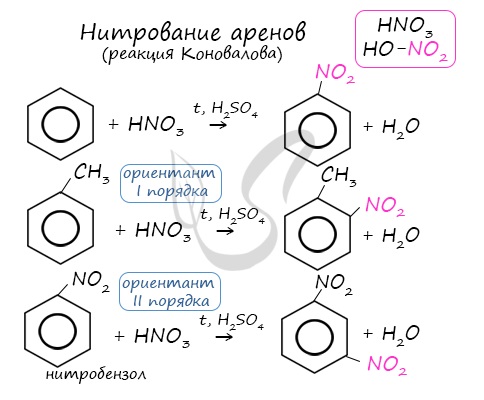
Почему хлор направляется именно в орто- и пара-положения относительно метильной группы? Здесь самое время коснуться темы ориентантов I (орто-, пара-ориентантов) и II порядков (мета-ориентанты).
К ориентантам первого порядка относятся группы: NH2, OH, OR, CR3, CHR2, CH 2R, галогены. К ориентантам второго: NO2, CN, SO3H, CCl3, CHO, COOH, COOR.
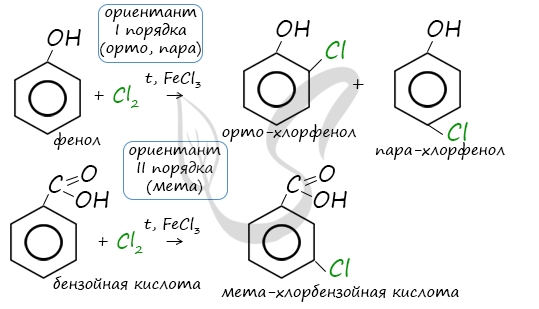
Например, ориентант I порядка, гидроксогруппа OH, обеспечивает протекание хлорирования в орто- и пара-положениях. А карбоксильная группа COOH, ориентант II порядка, обуславливает хлорирование в мета-положениях.
Арены вступают в реакции нитрования, протекающие при повышенной температуре и в присутствии серной кислоты, обладающей водоотнимающими свойствами.
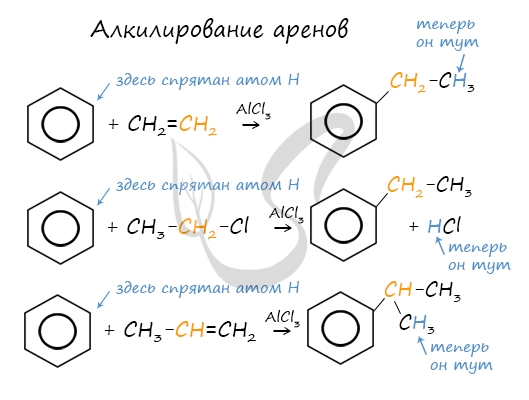
Алкилирование аренов осуществляется путем введения алкильного радикала в молекулу бензола. Алкильным радикалом чаще всего выступает алкен или галогеналкан.
В случае если для алкилирования используется алкен, то с молекулой бензола соединяется наименее гидрированный атом углерода алкена, прилежащий к двойной связи. Один атом водорода переходит из бензольного кольца к радикалу.
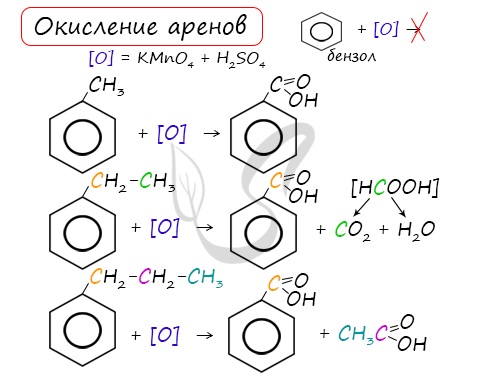
Арены, как и все органические вещества, сгорают с образованием углекислого газа и воды.
При неполном окислении гомологи бензола способны окисляться до бензойной кислоты (при подкислении раствора серной кислотой). Сам бензол не вступает в реакцию окисления с KMnO4, не обесцвечивает его раствор.
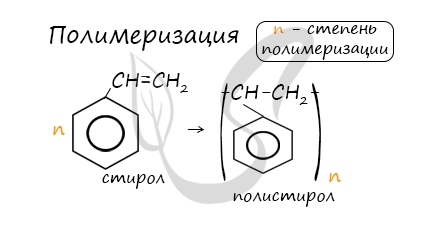
В реакцию полимеризации способен вступать стирол (винилбензол), в радикале которого содержится двойная связь.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
В лекции о бензоле мы рассмотрели строение молекулы и определили, что бензольное кольцо — уникальная система. И у этой системы свои характеристики, отличающиеся от свойств других углеводородов.

Первая такая характеристика — прочность бензольного кольца . Прочность не просто геометрической фигуры шестиугольника, а именно системы связей и делокализованного электронного облака.
Что это означает? Это означает, что разрушить эту систему (раскрыть кольцо) возможно при специальных условиях — давление, температура, катализатор…
Для бензола и его гомологов характерны реакции замещения.
Остальные реакции идут с трудом.
Лучше, конечно, разделить химические свойства бензола и химические свойства алкилбензолов. По сути, алкилбензолы — вещества с двумя функциональными группами — бензольным кольцом и насыщенным алкильным радикалом, для которого более характерны свойства алканов.
Химические свойства бензола
Реакции замещения в бензольном кольце проходят в присутствии катализаторов: солей Al(3+) или Fe(3+):
Реакция галогенирования бензола (взаимодействие с бромом — качественная реакция на бензол):
C6H6 + Br2 = C6H5Br + HBr

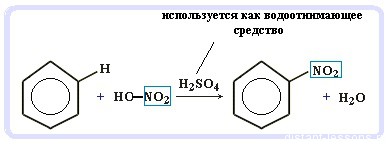
Нитрование бензола (обратите внимание, в органической химии неорганические кислоты реагируют немного по-другому — с отщеплением группы -OH):
C6H6 + HO-NO2 → C6H5NO2 + H2O
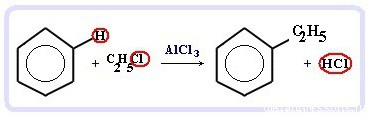
Химические свойства бензола — Алкилирование — получение гомологов бензола, алкилбензолов (катализаторы реакции — галогениды алюминия: AlCl3, AlBr3 и т.д.):
С6H6 + С2H5Cl → C6H5C2H5 + HCl
Реакции замещения алкилбензолов:
во-первых, гомологи бензола более ракционноспособны — легче вступают в реакции,
во-вторых, эти реакции идут немного по-другому:
Галогенирование алкилбензолов:
С6H5-CH3 + Br2 (на свету) = С6H5-CH2Br + HBr
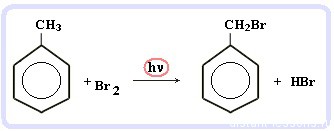
Т.е. бром идет в боковую цепь, а не в кольцо.
Чтобы бром пошел в кольцо, надо использовать катализатор — соли Al(3+)
Нитрование алкилбензолов:
С6H5-CH3 + 3HNO3 → C6H2CH3(NO2)3
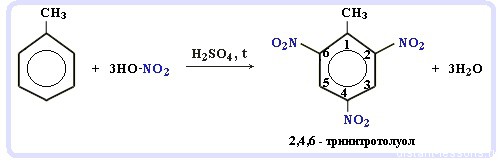
тринитротолуол, он же тротил
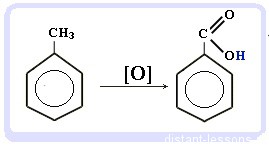
Окисление: реакция, характерная для алкилбензолов и не характерная для самого бензола
С6H5CH3 + [O] → C6H5COOH — бензойная кислота
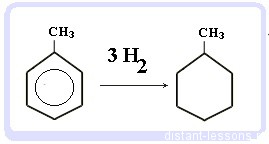
Гидрирование бензола и алкилбензолов:
Тут уже различий нет. при гидрировании всех аренов (температура, давление, катализатор — бензольное кольцо разорвать не так уж и просто) получаются циклоалканы, а точнее, циклогексан и циклогексан с радикалами:
С6H6 + 3 H2 → C6H12 циклогексан
С6H5CH3 + 3 H2 → C6H11-CH3 — метилциклогексан
Реакция горения: все органические вещества горят с образованием углекислого газа CO2 и воды H2O:
16. Бензол взаимодействует с
| 1) | бромной водой | 3) | бромоводородом |
| 2) | водородом | 4) | соляной кислотой |
17. Бензол не взаимодействует с
| 1) | водородом | 3) | бромом |
| 2) | кислородом | 4) | раствором перманганата калия |
18. Бензол не взаимодействует с
| 1) | СН3Сl | 2) | HNO3 | 3) | CH4 | 4) | C2H4 |
19. Продуктом взаимодействия бензола с хлором на свету является
| 1) | хлорбензол | 3) | гексахлорбензол |
| 2) | 1,3,5-трихлорбензол | 4) | гексахлорциклогексан |
20. Продуктом взаимодействия бензола с хлором в присутствии хлорида железа(III) является
| 1) | хлорбензол | 3) | гексахлорбензол |
| 2) | 1,3-дихлорбензол | 4) | гексахлорциклогексан |
21. Ароматическая связь сохраняется в молекуле в результате реакции бензола с
| 1) | концентрированной азотной кислотой |
| 2) | хлором при освещении |
| 3) | водородом в присутствии катализатора (Pt) |
| 4) | кислородом (горение) |
22. Хлорбензол является продуктом реакции, схема которой
23.Обесцвечивание раствора KMnO4 происходит под действием
| 1) | гексана | 3) | бензола |
| 2) | циклогексана | 4) | метилбензола |
24.Обесцвечивание бромной воды происходит под действием
| 1) | гексана | 3) | бензола |
| 2) | винилбензола | 4) | диметилбензола |
25. Сумма коэффициентов в уравнении реакции горения бензола равна
| 1) | 17 | 2) | 25 | 3) | 30 | 4) | 35 |
26. Коэффициент перед формулой кислорода в уравнении реакции горения толуола равен
| 1) | 7 | 2) | 8 | 3) | 9 | 4) | 11 |
27. Этилбензол взаимодействует с
| 1) | бромной водой | 3) | перманганатом калия |
| 2) | хлоридом алюминия | 4) | гидроксидом калия |
28. И бензол, и толуол взаимодействуют с
| 1) | cульфатом меди(II) | 3) | перманганатом калия |
| 2) | бромом | 4) | оксидом магния |
29. И бензол, и толуол взаимодействуют с
| 1) | бромной водой | 3) | гидроксидом меди(II) |
| 2) | азотной кислотой | 4) | бромоводородной кислотой |
30. Толуол в отличие от бензола взаимодействует с
| 1) | KMnO4 | 2) | HI | 3) | NaOH | 4) | O2 |
31. И бензол, и циклогексан взаимодействуют с
| 1) | натрием | 3) | хлором |
| 2) | перманганатом калия | 4) | азотом |
32. И бензол, и бутан взаимодействуют с
| 1) | кислородом |
| 2) | гидроксидом меди(II) |
| 3) | аммиачным раствором хлорида меди(I) |
| 4) | хлороводородом |
33. И бензол, и этин взаимодействуют с
| 1) | натрием |
| 2) | хлороводородом |
| 3) | аммиачным раствором оксида серебра |
| 4) | водородом |
34. И толуол, и этен взаимодействуют с
| 1) | водой | 3) | хлоридом натрия |
| 2) | оксидом углерода(IV) | 4) | перманганатом калия |
35. В отличие от бензола гомологи бензола реагируют с
| 1) | кислородом | 3) | азотной кислотой |
| 2) | хлором | 4) | перманганатом калия |
36. Бензол взаимодействует с каждым из двух веществ
| 1) | Br2 и HCl | 3) | Сl2 и HNO3 конц. |
| 2) | KMnO4 и Н2 | 4) | C2H4, и СН4 |
37. Толуол взаимодействует с каждым из двух веществ
| 1) | Сl2 и HCl | 3) | NaOH и HNO3 конц. |
| 2) | KMnO4 и Н2 | 4) | H2SO4 и СuSO4 |
38. С каждым из трех веществ:
бромом, перманганатом калия, водородом –
| 1) | толуол | 2) | бензол | 3) | гексан | 4) | циклогексан |
39. Реакции присоединения характерны для каждого их двух углеводородов
| 1) | этана и циклобутана | 3) | циклопропана и бутина |
| 2) | циклогексана и бензола | 4) | гексана и толуола |
40. При взаимодействии толуола с водным раствором перманганата калия в кислой среде образуется
| 1) | уксусная кислота | 3) | углекислый газ |
| 2) | фенол | 4) | бензойная кислота |
41. Толуол в отличие от бензола реагирует с
| 1) | Н2 | 2) | КMnO4 | 3) | HBr | 4) | Na |
42. В качестве взрывчатого вещества используют:
| 1) | нитробензол | 3) | ксилол |
| 2) | толуол | 4) | тринитротолуол |
43. Гексахлорциклогексан используется в качестве
| 1) | ядохимиката | 3) | красителя |
| 2) | лекарственного препарата | 4) | растворителя |
44. Какие из приведенных утверждений о бензоле и его свойствах верны?
А. Молекула бензола имеет плоское строение.
Б. Для бензола наиболее характерны реакции присоединения.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
45. Какие из приведенных утверждений о бензоле и его свойствах верны?
А. Атомы углерода в молекуле бензола находятся в состоянии sp-гибридизации.
Б. Бензол и его пары ядовиты.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
46. Какие из приведенных утверждений о бензоле и его свойствах верны?
А. Бензол – бесцветная жидкость без запаха.
Б. Продуктом взаимодействия бензола с бромом в присутствии FeBr3 является бромбензол.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
47. Какие из приведенных утверждений о бензоле и его свойствах верны?
А. Бензол хорошо растворим в воде.
Б. Продуктом взаимодействия бензола с хлором при освещении является хлорбензол.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
48. Какие из приведенных утверждений о бензоле и его свойствах верны?
А. Промышленным способом получения бензола является сплавление натриевой соли бензойной кислоты со щелочами.
Б. Бензол легко окисляется водным раствором перманганата калия.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
49. Какие из приведенных утверждений о бензоле и его свойствах верны?
А. Бензол неустойчив к действию окислителей.
Б. Пробирку с бензолом можно нагревать на открытом пламени.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
50. Какие из приведенных утверждений о бензоле и его свойствах верны?
А. Для бензола характерна реакция полимеризации.
Б. Бензол можно получить при дегидрировании циклогексана.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
51. Какие из приведенных утверждений о толуоле и его свойствах верны?
А. Толуол в промышленности можно получить в результате дегидроциклизации гептана.
Б. Толуол обесцвечивает бромную воду.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
52. Какие из приведенных утверждений о толуоле и его свойствах свойствах верны?
А. В молекуле толуола имеется тетраэдрический фрагмент атомов.
Б. Толуол проявляет более высокую реакционную способность по сравнению с бензолом.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
53. Какие из приведенных утверждений об этилбензоле и его свойствах верны?
А. В молекуле этилбензола все атомы углерода находятся в состоянии sp 2 -гибридизации.
Б. При окислении этилбензола перманганатом калия в кислотной среде образуется бензойная кислота.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба утверждения |
| 4) | оба утверждения неверны |
54. В схеме превращений
1-бромпропан → X→ бензол
веществом Х является
| 1) | ацетилен | 2) | пропен | 3) | гексан | 4) | циклогексан |
55. В схеме превращений
веществом Х является
| 1) | C2H4 | 2) | C6H12 | 3) | CH4 | 4) | C2H2 |
56. В схеме превращений
веществами Х1 и Х2 соответственно являются
| 1) | CH4 и C6H6 | 3) | C2H2 и CH≡C-CH=CH2 |
| 2) | C2H4 и C6H5CH3 | 4) | C2H2 и C6H6 |
57. В схеме превращений
веществами Х1 и Х2 соответственно являются
| 1) | циклогексан и хлорциклогексан | 3) | бензол и хлорбензол |
| 2) | толуол и 2-хлортолуол | 4) | бензол и гексахлоран |
58. В схеме превращений
веществами Х1 и Х2 соответственно являются
| 1) | C6H5CH3 и C6H5CH2Cl | 3) | C6H6 и C6H5Cl |
| 2) | C6H5CH3 и C6H4ClCH3 | 4) | C6H6 и C6H6Cl6 |
59. В схеме превращений
веществами Х1 и Х2 соответственно являются
| 1) | метан и 2-хлортолуол | 3) | хлорметан и 2-хлортолуол |
| 2) | метан и 3-хлортолуол | 4) | хлорметан и 3-хлортолуол |
60. В схеме превращений
веществами Х1 и Х2 соответственно являются
| 1) | C2H5Cl и C6H5COOH | 3) | C2H4 и C6H5OH |
| 2) | C2H5Cl и C6H5OH | 4) | C2H6 и C6H5COOH |
Повышенный уровень сложности
61. Все атомы углерода находятся в состоянии sp 2 -гибридизации в молекулах
| 1) | толуола | 4) | бутадиена-1,2 |
| 2) | этилена | 5) | бензола |
| 3) | бутадиена-1,3 | 6) | этилбензола |
62. Гомологами бензола являются
| 1) | стирол | 4) | этилбензол |
| 2) | толуол | 5) | ксилол |
| 3) | крезол | 6) | фенол |
Дата добавления: 2019-01-14 ; просмотров: 1057 ;
Читайте также:

