Анемия при раке предстательной железы

Анемия представляет собой патологическое состояние, для которого характерно снижение эритроцитов и/или концентрации гемоглобина в единице объема крови. Анемия не является самостоятельным заболеванием, это симптом, который характерен для самых разнообразных заболеваний, в том числе и для злокачественных опухолей.
Согласно статистике, данное состояние выявляется у каждого третьего онкологического пациента, а при прохождении химиотерапии — более чем в 90% случаев. Опасность анемии в онкологии заключается в том, что вместе с уменьшением уровня гемоглобина и эритроцитов, уменьшается и кислородная емкость крови. Этот фактор неблагоприятно сказывается на течении ракового процесса, снижает эффективность лечения и ухудшает дальнейший прогноз.
- Основные причины развития анемии у онкологических пациентов
- Как выявить анемию
- Как классифицируется анемия
- Методы лечения анемии
- Лечение анемии народными способами
Основные причины развития анемии у онкологических пациентов
Снижение уровня эритроцитов и гемоглобина может развиваться вследствие снижения их образования, ускоренного разрушения или в результате потери. Каждой из этих причин способствуют собственные факторы, которые рассмотрим подробнее:
- Недостаточная выработка форменных элементов крови и гемоглобина может развиваться при поражении костного мозга, недостатке железа в организме или некоторых витаминов (фолиевая кислота, витамин В12). Данные состояния могут быть напрямую связаны с напрямую с онкологическим заболеванием. Например, потеря железа может развиваться в результате постоянной рвоты, отсутствия аппетита и нарушения его всасывания в кишечнике, который поражен опухолевым процессом. Некоторые виды препаратов, которые назначают при злокачественных опухолях, подавляют рост не только раковых клеток, но и клеток крови, которые активно делятся. Также анемия может развиваться при непосредственном поражении костного мозга опухолевым процессом.
- Ускоренное разрушение эритроцитов отмечается при воздействии различных лекарственных препаратов и при аномальной активности иммунной системы. Разрушение эритроцитов непосредственно в сосудах называется внутрисосудистым гемолизом. Этот процесс протекает в норме после завершения жизненного цикла эритроцитов, который составляет 120 дней. Однако при воздействии различных факторов (прием антибиотиков, цитостатиков, присоединение вторичной инфекции и др.), этот срок значительно уменьшается, что и приводит к развитию анемии.
- Кровопотеря у онкологических пациентов может быть как острой, так и хронической. Первый вариант встречается при проведении хирургического лечения рака, а также при развитии внутренних кровотечений, которые являются частым осложнением основного заболевания. Развитие анемии при хронической кровопотере отмечается в тех случаях, когда имеется скрытый источник незначительного кровотечения. Например, при колоректальном раке кровь может выделяться с калом незаметно для пациента.
Установление точной причины анемии играет решающее значение при выборе метода лечения. Кроме того, врач учитывает степень тяжести, тип анемии, общее состояние пациента и другие параметры. Получить эту информацию можно на диагностическом этапе.
Как выявить анемию
Обследование традиционно начинается с опроса пациента и сбора анамнеза. Врач должен помнить, что не всегда анемия развивается вследствие основного заболевания. Возможны наследственные или любые другие причины, которые не связаны с опухолевым процессом. Также необходимо установить вид предшествующего противоопухолевого лечения, продолжительность и количество курсов, наименование препаратов, которые применялись. На следующем этапе врач проводит общий осмотр. Анемия может проявляться бледностью кожных покровов, слабостью, потерей аппетита, головокружением и другими симптомами. Очень часто эти проявления отмечаются при различных видах рака, который протекает без анемии, поэтому поставить диагноз исходя только из жалоб пациента невозможно.
Объективную информацию можно получить только при помощи лабораторных исследований. Анемия диагностируется по следующим анализам:
- Количество ретикулоцитов.
- Уровень железа сыворотки крови.
- Уровень белка трансферрина и ферритина.
- Уровень витамина В12 и фолиевой кислоты.
Отдельное внимание уделяется общему анализу крови. В нем определяется уровень гемоглобина, количество эритроцитов и гематокрит (отношение форменных элементов к жидкой составляющей крови). Также определяют средний объем эритроцита, среднее содержание гемоглобина в эритроците и среднее содержание гемоглобина во всей эритроцитарной массе.
При необходимости в программу комплексного обследования при анемии могут включаться и другие лабораторные анализы или специальные методы.
Как классифицируется анемия
В зависимости от значения цветового показателя, степени тяжести и механизма развития, анемия разделяется на несколько категорий. Цветовой показатель крови отражает степень насыщения эритроцитов гемоглобином. Его значение в норме колеблется от 0,85 до 1,05 единиц. Снижение показателя отмечается при гипохромной анемии, а повышение — при гиперхромной. Если цветовой показатель в норме, но уровень гемоглобина все равно низкий, то говорят о нормохромной анемии.
По степени тяжести, анемия разделяется на три группы, в зависимости от концентрации гемоглобина:
- При легкой степени анемии уровень гемоглобина не опускается ниже отметки в 90 г/л.
- При средней степени анемии показатель колеблется в пределах 90-70 г/л.
- Тяжелая анемия характеризуется падением гемоглобина ниже 70 г/л.
Классификация анемии по механизму развития наиболее обширна. Среди распространенных форм отмечаются:
- Железодефицитная анемия. Развивается в результате нарушения всасывания, усиленной потери или недостаточного поступления железа в организм.
- Гемолитическая анемия. Характеризуется разрушением эритроцитов в сосудистом русле или за его пределами. Наиболее частые причины — недостаточность специфических ферментов, аутоиммунные заболевания, воздействие лекарственных препаратов.
- Постгеморрагическая анемия. Данное состояние характерно для острой или хронической кровопотери
- Апластическая анемия. Характеризуется снижением уровня клеток-предшественников эритроцитов в костном мозге. Обычно отмечается снижение и других форменных элементов — тромбоцитов и лейкоцитов.
- В12-дефицитная анемия. При недостатке витамина В12 нарушается процесс образования эритроцитов, снижается их продолжительность жизни. Дефицит витамина может быть связан как с нарушением его всасывания в кишечнике, так и с недостаточным поступлением в организм.
В большинстве случаев определить точный вид анемии можно после нескольких лабораторных тестов, но иногда приходится применять более сложные методы диагностики, например, генетическое исследование. Понимание механизма развития анемии и получение максимально полной информации об изменениях в показателях крови являются важным компонентом эффективной терапии данного симптома.
Методы лечения анемии
Устранить анемию у онкологических пациентов можно тремя способами: переливание эритроцитарной массы, введение эритропоэтина, назначение препаратов, содержащих железо. В отдельных случаях может применяться комбинация этих методов.
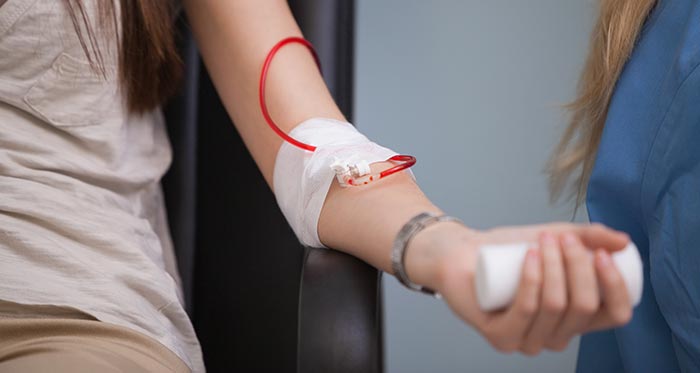
Переливание эритроцитарной массы является самым действенным методом, при помощи которого можно быстро восполнить дефицит эритроцитов, восстановить уровень гемоглобина и гематокрита. Однако без устранения причины анемии, этот способ даст лишь временный эффект. Поэтому переливание эритроцитарной массы не является альтернативой другим методикам и применяется только при наличии показаний. Одним из них является снижение уровня гемоглобина ниже 90 г/л. Переливание проводят при развитии у пациента характерных признаков анемии, среди которых отмечаются:
- Головокружение.
- Потеря сознания.
- Тахикардия.
- Быстрая утомляемость.
- Боль в груди.
- Одышка.
Данный метод лечения анемии также может применяться у пациентов, которые прошли курс химиотерапии или лучевой терапии и у которых отмечается быстрое снижение уровня гемоглобина или эритроцитов.
Стимуляторы эритропоэза при анемии увеличивают концентрацию гемоглобина и эритроцитов за счет усиления их образования в костном мозге. При сочетании с гемотрансфузиями, данный метод показывает очень хорошие результаты, но при этом имеет и ряд недостатков, которые касаются осложнений. В частности, применение стимуляторов эритропоэза для лечения анемии повышает риск развития тромботических осложнений, который и так является высоким у онкологических пациентов. По данным, полученным в ходе нескольких научных исследований, этот риск увеличивается в 1.4-1.7 раз.
В последнее время обсуждается вопрос о влиянии стимуляторов эритропоэза на выживаемость онкологических пациентов. В частности, специалисты установили, что применение препаратов данной группы при лечении анемии у пациентов с распространенным опухолевым процессом головы и шеи, шейки матки, молочной железы и других диагнозах снижает продолжительность жизни на 10-17%. В связи с этим специалисты предлагают придерживаться следующих правил:
- Если уровень гемоглобина составляет менее 100 г/л и пациент при этом проходит лечение химиопрепаратами, то стимуляторы эритропоэза могут назначаться с целью коррекции анемии и профилактики дальнейшего снижения показателей.
- Если уровень гемоглобина падает до 100 г/л и ниже, но химиотерапия при этом не проводится, то применять стимуляторы эритропоэза не рекомендуется ввиду повышенного риска развития осложнений и снижения продолжительности жизни.
- Во всех остальных случаях применять стимуляторы эритропоэза для лечения анемии у онкологических пациентов следует с осторожностью.
Также на протяжении всего времени лечения важно контролировать динамику лабораторных показателей и при увеличении уровня гемоглобина постепенно снижать дозировку стимуляторов эритропоэза.
Препараты железа применяются с целью лечения железодефицитных анемий, которые выявляются у 30-60% онкологический больных. При этом снижение уровня железа может быть связано как с самим опухолевым процессом или проводимым лечением, так и с другими факторами. Например, при назначении стимуляторов эритропоэза, существующего запаса железа в организме становится недостаточно для того, чтобы покрыть потребность, которая возникает в результате активного синтеза гемоглобина в костном мозге.

Для лечения анемии могут применяться как внутривенные, так и пероральные препараты. Второй вариант более удобен для пациента, так как таблетки проще принимать, но при этом данная форма действует медленнее и чаще приводит к осложнениям со стороны ЖКТ. Внутривенное введение позволяет добиться быстрого эффекта, что актуально при проведении химиотерапии.
Таким образом, для лечения анемии современная онкология может предложить различные методы, которые воздействуют на механизмы развития данного симптома. Точный план терапии подбирается индивидуально для каждого пациента, с учетом лабораторных показателей крови, особенностей лечения основного заболевания и других параметров.
Лечение анемии народными способами
Некоторые пациенты по разным причинам отказываются от приема описанных выше препаратов и обращаются к народной медицине. Безусловно, некоторые растения или продукты могут оказывать стимулирующее действие на систему кроветворения. Однако, учитывая основной диагноз и тяжесть анемии, этого действия крайне недостаточно для восстановления уровня гемоглобина и кислородной функции крови. В результате снижается эффективность противоопухолевого лечения, ухудшается прогноз и существенно повышается риск неблагоприятного исхода. Устранить выраженную анемию в домашних условиях при помощи народных методов невозможно. Этим должны заниматься врачи соответствующего профиля, в распоряжении которых имеются современные лекарственные препараты.

-
3 минут на чтение

Анемия – патологическое состояние, при котором в крови снижается концентрация гемоглобина и/или эритроцитов. Анемия редко встречается как самостоятельно заболевание, чаще является признаком различных патологий. Нередко такое состояние выявляется у онкологических больных, особенно во время прохождения лечения, негативно влияющего на функционирование кровеносной системы.
- Может ли анемия быть симптомом рака
- Связь анемии и рака
- Как избавиться от анемии онкологическим больным
- Трансфузия эритроцитарной массы
- Препараты, влияющие на эритропоэз
- Препараты железа
Может ли анемия быть симптомом рака
После стремительного снижения веса анемия считается главным признаком раковых заболеваний. Опытный онколог по уровню гемоглобина и внешним признакам анемии может заподозрить наличии злокачественных новообразований и направить пациента на обследование.
Снижение уровня гемоглобина выявляется у 40-50% пациентов к моменту постановки диагноза. У остальной части онкологических больных анемия развивается после облучения или прохождения химиотерапии.
Быстрее всего анемия развивается при раке органов пищеварения, лейкемии и лимфоме. Если обнаруживается значительное и беспричинное снижение уровня гемоглобина, врачи назначают комплексное обследование пациента, в которое включают ФГДС, колоноскопию и скрининговые анализы крови и исследование кала на скрытую кровь.
Если рак протекает скрыто и больной еще не знает о своем диагнозе, он ощущает только легкую усталость, сонливость и периодические головокружения. Большинство пациентов не обращают внимания на такое состояние, списывая его на переутомление. С прогрессированием опухоли появляется настолько сильная слабость, что даже нагрузка приводит к учащенному сердцебиению и отдышке.
Связь анемии и рака
Злокачественная опухоль и анемия тесно связаны между собой. На ранних стадиях анемия возникает из-за развития раковой анорексии, характеризующейся снижением или полным отсутствием аппетита, тошнотой и рвотой. В организм не поступает достаточно элементов, участвующих в процессах кроветворения, развивается анемия. На ее фоне все органы и ткани начитают испытывать гипоксию, что еще сильнее влияет на прогрессирование злокачественного процесса.

- Общее
![]()
Наталья Геннадьевна Буцык- 6 декабря 2019 г.
При раке развивается хроническая анемия на фоне влияния злокачественного процесса на иммунную систему. В результате в крови увеличивается концентрация интерлейкинов и фактора некроза опухоли. В комплексе эти процессы нарушают обмен железа, уменьшают продолжительность жизни эритроцитов и негативно влияют на функции кроветворения.
Нормально, если анемия при раке развивается после операции по удалению злокачественной опухоли. Послеоперационные кровопотери обычно умеренны и уровень гемоглобина приходит в норму через 2-3 недели, если не возникло осложнений. При тяжелых формах опухоли и обширных кровотечениях в ранний послеоперационный период назначают препараты железа, чтобы предотвратить состояние.
Хроническая анемия развивается после лучевой терапии у 70-80% онкобольных. Вероятность нарушения синтеза эритроцитов напрямую зависит от площади облучения. Лучевая терапия негативно влияет на функции костного мозга, в результате синтезируются эритроциты неправильной формы, которые имеют более низкую продолжительность жизни, чем здоровые красные клетки.
Так же установлена прямая связь между концентрацией гемоглобина и эффективностью противоопухолевого лечения. Пациенты с нормальным уровнем гемоглобина лучше переносят химиотерапию и у них реже возникают рецидивы. Если после приема противоопухолевых препаратов резко падает гемоглобин, вероятность развития рецидива и стремительного прогрессирования заболевания увеличивается в два раза.
Как избавиться от анемии онкологическим больным
Схема лечения анемических состояний у пациентов с опухолями подбирается в индивидуальном порядке. При назначении препаратов лечащий врач учитывает показатели крови больного, тяжесть анемии, стадию рака и вероятность развития осложнений, которые могут возникнуть на фоне лечения.
Переливание эритроцитарной массы — самый быстрый метод повышения уровня гемоглобина. Но без устранения причин патологического состояния трансфузия дает лишь временный эффект, поэтому назначается строго по показаниям.
Основными мужскими гормонами-андрогенами являются тестостерон и дигидротестостерон. Они вырабатываются в тестикулах под воздействием гипофиза и напрямую влияют на синтез, качество и количество семенной жидкости. Однако, помимо этого, тестостерон и дигидротестостерон (ДГТ) провоцируют рост злокачественных опухолей.
Любая гормонотерапия при раке простаты может снижать либо вовсе прекращать выработку андрогенов или предотвращать их воздействие на раковые клетки в предстательной железе.
Существует несколько методик гормонального лечения. Оптимальную и наиболее эффективную должен подбирать лечащий врач с учетом стадии заболевания, особенностей его течения, возраста и общего состояния здоровья пациента.

Лечение рака предстательной железы гормонами может проводиться как самостоятельный вид терапии, в комплексе с радио- либо химиотерапией, а также после хирургического удаления части простаты либо всего органа.
Гормональная терапия при раке простаты
Лечить онкологические патологии предстательной железы медикаментозно можно препаратами различного спектра действия. В современной медицине в этой области выделяют четыре основных направления:
- гормональная терапия при раке предстательной железы с применением препаратов-агонистов лютеинизирующего гормона. Их назначение – блокировать сигналы, поступающие из гипофиза, и таким образом прекратить выработку тестостерона в яичках. Этот метод также называют химической либо медикаментозной кастрацией;
- лечение андрогенами. Препараты этой группы предотвращают прикрепление тестостерона к озлокачествленным клеткам. Вследствие этого рост раковых клеток замедляется либо прекращается;
- гормонотерапия при раке предстательной железы с использованием антагонистов гонадотропин-высвобождающего гормона. Они способствуют прекращению выработки этого гормона в гипофизе. Как следствие, синтез тестостерона в мужском организме прекращается;
- метод с применением ингибиторов синтеза андрогенов. Единственный препарат, используемый в рамках данного метода, – абиратерон. Он подавляет активность фермента, отвечающего за выработку андрогенов. При этом концентрация тестостерона снижается не только в предстательной железе, но и в крови, надпочечниках, яичках;
- гормональное лечение рака предстательной железы эстрогенами. Женские половые гормоны, также способны влиять на интенсивность синтеза андрогенов. Такой метод имеет тяжелые побочные эффекты, например, развитие тромбоза. Поэтому врач назначает его только в том случае, если иные стратегии не сработали.
Отдельно стоит выделить орхэктомию – хирургическую кастрацию. Во время операции пациенту полностью удаляют яички, что в скором времени приводит к значительному снижению уровня тестостерона. Несмотря на то, что метод предполагает хирургическое вмешательство, по результату его можно отнести к гормонотерапии при раке простаты. Более того, он считается одним из наиболее эффективных, быстрых, недорогих и безопасных видов гормонального лечения данного заболевания.
Цели и ожидания
Правильно назначенное гормональное лечение при раке простаты позволяет добиться нескольких целей:
- снизить болевые ощущения, облегчить процесс мочеиспускания и таким образом улучшить качество жизни пациента;
- уменьшить размер предстательной железы. Это позволяет минимизировать площадь здоровых тканей, попадающих под воздействие радиоактивных лучей при последующей радиотерапии;
- замедлить скорость развития онкологического процесса в предстательной железе.
При назначении гормональных препаратов врач обязательно взвешивает прогнозируемую результативность лечения и сравнивает ее с вероятными рисками. Если последний фактор существенно преобладает, от гормональной терапии при раке предстательной железы лучше отказаться и сосредоточиться на других, менее опасных для больного методах, стратегиях и тактиках.
Даже грамотно подобранная терапия может спровоцировать ухудшение самочувствия пациента. О побочных эффектах такого лечения стоит знать заранее и воспринимать их без паники.

Чаще всего мужчины, принимающие гормоны при раке предстательной железы, жалуются на:
- общую и мышечную слабость, потливость, приливы жара;
- уменьшение сексуального влечения и ослабление либо прекращение эрекции;
- запоры или, наоборот, диарею;
- рост молочных желез и неприятные ощущения в них;
- заметную прибавку в весе;
- снижение концентрации внимания, бессонницу, депрессивные состояния.
Как минимизировать негативные последствия гормонотерапии при раке простаты?
Чтобы не допустить возникновения диабета и сердечно-сосудистых заболеваний, риск появления которых повышает гормональная терапия при раке простаты, пациентам рекомендуют не злоупотреблять алкоголем и табакокурением, правильно питаться – в рационе должны преобладать белок, клетчатка, полезные жиры и сложные углеводы, стараться удерживать оптимальный вес и не пренебрегать физическими нагрузками – даже если в силу самочувствия они будут низкоинтенсивными и ограниченными по времени.
Еще одно частое последствие гормональной терапии при раке предстательной железы – остеопороз. Чтобы избежать изменений в костных структурах, необходимо в процессе лечения регулярно принимать витамин D и препараты кальция. А снизить риск развития анемии поможет введение в рацион продуктов, содержащих большое количество железа, а также профилактический прием назначенных врачом препаратов железа.
Предстательная железа — небольшой орган, расположенный под мочевым пузырем, который окружает мочеиспускательный канал. Функцию простаты сложно переоценить, ведь именно сок предстательной железы поддерживает жизнедеятельность сперматозоидов вне яичек. В этой статье мы рассмотрим такое онкологическое заболевание как рак предстательной железы, симптомы, лечение и причины возникновения этого недуга.
Статистика заболевания
Рак предстательной железы — опухоль, локализованная в предстательной железе, имеющая злокачественный характер и представляющая серьезную угрозу не только для половой функции, но и для жизни мужчины. Другое название рака — карцинома.
В Европе это одно из самых серьезных заболеваний мужской части населения, которое встречается у 214 человек из 1000 исследуемых. Следует отметить, что частота встречаемости рака предстательной железы в разных регионах различается. Например, в Швеции, обсуждаемое заболевание составляет 37 процентов всех случае раковых опухолей.
Рак простаты — заболевания, имеющее тесную связь с генетикой и возрастом человека. Чаще среди больных встречаются мужчины, возраст которых превышает 40 лет.
Некоторые закономерности, причины возникновения рака предстательной железы
В настоящее время причины рака предстательной железы — вопрос открытый. Ученые установили однозначную связь возникновения рака простаты с двумя факторами:
С годами в организме мужчины происходят гормональные изменения. Следом возникают изменения в предстательной железе, способные привести к раку. Выявлено, что рак простаты напрямую зависит от уровня тестостерона в крови. Поэтому заболеванию подвержены мужчины среднего и преклонного возраста. У молодых лиц рак встречается крайне редко и только в случае наследственной предрасположенности или под влиянием серьезных мутагенных факторов.
- Наследственность
Риск заболевания удваивается, если у мужчины среди близких родственников присутствуют больные раком простаты. Если же болели родственники первой и более степеней родства, риск снижается, но имеет место быть. Наследственный рак простаты отличается от остальных этиологических типов заболевания лишь более ранней датой возникновения (с разницей в 6-7 лет).
Остальные факторы, по которым человека можно отнести к группе риска, на данный момент установлены, но не доказаны, но они существуют:
Образ жизни существенно влияет на возможность развития ракового процесса в предстательной железе. Наличие вредных привычек заметно увеличивает (в недоказанных пропорциях) риск возникновения опухоли: склонность к употреблению алкоголя, курению, наркотическим веществам. Вышеперечисленные вещества обладают мощным мутагенным эффектом и способны активировать процесс злокачественного перерождения уже имеющейся опухоли простаты.
Спровоцировать онкологию способны красное мясо и жиры животного происхождения. Четкой связи между питанием и появлением рака не отмечено. Но врачи рекомендуют избегать принимать в пищу указанные продукты, если есть предпосылки к онкологии.
Классификация
Существует 2 классификации рака предстательной железы. Первая относится к стандартной номенклатуре всех раковых опухолей, а вторая, более приемлемая в случае рака простаты, основана на агрессивности опухоли. Агрессивность определяется индексом Глисона после исследования биоптата раковой опухоли. Балл (индекс) выставляется от 1 до 10, что означает, соответственно, менее и более агрессивную опухоль.
Симптомы рака простаты
Проявлений у рака простаты слишком много, чтобы точно установить диагноз лишь по анамнезу больного и пальпации.
- Боль и жжение при мочеиспускании и после него
![]()
- Прерывистое мочеиспускание
- Частые позывы к мочеиспусканию
- Боли в области паха
- Боли при ректальной пальпации простаты
- Гематурия
- Импотенция и др.
В целом, симптомы рака предстательной железы можно объединить в три большие группы:
- Функциональные нарушения оттока мочи;
- Признаками, связанные с метастазами опухоли, выходящими за пределы простаты;
- Симптомы при обширном метастазировании раковых клеток далеко за пределы предстательной железы.
Первая группа признаков связана с тем, что раковая опухоль начинает механически сдавливать мочеиспускательный канал, проходящий через простату. В связи с этим мочеиспускание становится болезненным, проблемным и нерегулярным. Это приводит к застою мочи в мочевом пузыре, нервозности, отечности, стрессам.
Когда опухоль проникает за пределы предстательной железы, это причиняет мужчине дополнительные болевые ощущения. Кроме этого, может наблюдаться эректильная дисфункция, гематурия и гематоспермия.
При глубоких и обширных метастазах рак распространяется по тазовой области, поражая кости, спинной мозг, близлежащие органы. При этом основные симптомы рака предстательной железы будут следующими:
- Боли в области таза и поясницы костного происхождения
- Анемия (см. препараты железа при анемии)
- Отечность тела и конечностей
- Паралич
Стадии рака простаты
Стадийность заболевания классифицируется в соответствии с формами рака. Существует 2 основные номенклатуры:
TNM — В рамках данной классификации рассматривается степень разрастания раковой опухоли:
- T — опухоль находится в предстательной железе или чуть выходит за границы ее капсулы.
- N — раковые клетки прорастают в регионарные лимфатические узлы, расположенные ниже бифуркации подвздошной артерии.
- M — в данном пункте речь идет об отдаленных метастазах, при которых поражаются не регионарные лимфатические узлы, кости и другие органы.
Система Джуит-Уайтмор — Данная классификация разделяет патологический процесс на стадии А, B, C, D. Первые 2 стадии являются излечимыми, последние 2 — несут более печальные перспективы.
Самой ранней стадией является А , при которой пациент может не испытывать никаких неприятных ощущений, а раковые клетки могут единично или массово локализоваться в паренхиме предстательной железы.
Стадия B характеризует разрастание опухоли внутри простаты до пальпируемых размеров. На данный момент рак можно выявить за счет умеренного повышения концентрации белка ПСА.
Следующий этап С , обозначает выход раковых клеток за пределы капсулы предстательной железы. Опухоль доходит до семенных пузырьков, других органов, может перекрывать просвет уретры и мочевого пузыря. На данной стадии рак становится неизлечимым заболеванием.
Стадия D — финальный этап развития рака. Характеризуется увеличением числа метастазов и разрастанием опухоли в сторону регионарных лимфатических узлов и за их пределы. Также стадией D именуются и рецидивирующие метастазы после операционного лечения рака простаты.
Нужно помнить, что стадии рака предстательной железы, симптомы которых могут крайне различаться, выделены условно. Четких критериев, по которым можно отнести опухоль к тому или иному этапу, нет.
Диагностика
Применяются следующие методы:
- Пальцевая диагностика или пальцевое ректальное исследование. Врач на ощупь диагностирует наличие/отсутствие опухоли.
- ПСА (простатический специфический антиген). Чем выше концентрация ПСА в сыворотке крови, тем больше вероятность наличия рака простаты.
- Трансректальное ультразвуковое исследование. Чаще его обозначают, как ТРУЗИ (аббревиатура). Это исследование простаты с помощью ультразвука путем введения диагностического прибора в прямую кишку.
- Биопсия простаты.
- Патоморфологическое исследование пункционных биоптатов простаты и др.
В качестве мониторинга рака предстательной железы используются первые 3 методики. ПСА — отличный и простой способ регулярно следить за состоянием предстательной железы.
До появления ПСА в 30% случаев выявлялась распространенная форма рака простаты, сейчас при регулярном контроле этого анализа крови и осмотра уролога только в 6% случаев выявляют распространенный рак предстательной железы, что улучшает прогноз и позволяет вовремя провести радикальное лечение.
В норме содержание ПСА должно быть менее 4 нг/мл, выше 10 говорит о высоком риске возникновения рака. Однако существуют и исключения:
- Редко регистрируются случаи, когда при раке простата анализ ПСА остается в пределах нормы.
- При лечении простаты могут использоваться препараты, которые приводят к снижению показателя ПСА (ложно отрицательный результат) на фоне рака предстательной железы.
- Аденома простаты и простатит могут влиять на показатель ПСА, увеличивая его значение при отсутствии признаков и симптомов рака предстательной железы.
Лечение рака простаты
Очень важным и актуальным на сегодняшний день является вопрос о лечении рака предстательной железы. Решение о лечении принимается исходя из возраста пациента.
Если мужчине 65 и более лет и рак не выходит за пределы предстательной железы, то принимать меры нет смысла. На сегодняшний день смертность в этом возрасте достаточно высока и отнюдь не от рака простаты.
Если процесс вышел за пределы предстательной железы, то пациенту без лечения остается жить не более трех лет. Все известные на данный момент методы лечения можно представить следующим образом:
- Таргетная терапия и химиотерапия
- Гормональная терапия
- Брахитерапия, лучевые методики
- Хирургические вмешательства
Сейчас лечение рака предстательной железы является максимально безболезненным.
Действие лекарственных веществ направлено на торможение роста раковых клеток. Но действие это недостаточно специфично, поэтому затрагивает здоровые клетки и наносит вред организму.
Как альтернативу химиотерапии ученые разработали таргетное лечение опухоли. В данном случае раковые клетки подвергаются атаке высокоспецифичных моноклональных антител. Такая практика позволяет свести побочный эффект к минимуму и значительно облегчает лечение рака предстательной железы.
Использование определенного набора гормонов позволяет остановить или серьезно замедлить деление раковых клеток. Этот вид лечения чаще применяется в качестве сопровождения к хирургическому, или же лучевой терапии, но может использоваться и самостоятельно.
Воздействие рентгеновским и прочими радиоактивными излучениями всегда вызывало опасения пациентов и множество побочных явлений. Это связано с тем, что при обширных метастазах приходиться подвергать облучению не только опухоль, но и близлежащие ткани и органы. В случае опухоли, локализованной в простате, такая методика менее опасна, но не является целесообразной.
В современной медицине разработаны менее рискованные методы лечения:
Она подразумевает ввод через прямую кишку специальной иглы, через которую в простату будет введен изотоп йода. Локализация инъекции вычисляется абсолютно точно. Действие радиоактивного вещества распространяется лишь на раковые клетки, не причиняя системного вреда, как в случае облучения старыми методиками.
— это точечное воздействие узльтразвуком на опухолевые клетки. Доказано, что раковые клетки полностью разрушаются под действием высоких частот.
Современные способы лечения существенно уменьшают риск возникновения побочных эффектов, а их эффективность, наоборот, становится всё более высокой.
Хирургическое вмешательство — самый простой и эффективный способ уничтожения опухоли на первых стадиях (A и B по классификации Джуит-Уайтмор). Пока опухоль не начала прорастать за пределы простаты, ее, действительно, лучше удалить. Существует два типа операций:
- Простаэктомия
В случае простаэктомии предстательная железа удаляется целиком через разрез. Это наиболее травматичный вид хирургического лечения рака простаты.
- Трансуретральная резекция
Трансуретральная резекция подразумевает частичное удаление простаты через мочеиспускательный канал. Показаниями к такого рода процедуре являются невозможность полного удаления простаты или непереносимости операций. Выполняется эндоскопическим методом.
Наиболее частые вопросы пациентов
Нет, такой вид наблюдения означает то, что у опухоли медленный рост, и возможно, она даже не проявит себя. При динамическом наблюдении показано обследование 2 раза в год — пальцевое ректальное исследование и ПСА. Такой регулярный контроль без лечения позволяет вовремя выявить прогрессирование опухоли и перейти от наблюдения к интенсивной терапии.
Исследования в США установили, что у мужчин, не имеющих рака предстательной железы и у пациентов с медленно растущей опухолью (при динамическом наблюдении в течение 15 лет), смертность была одинаковой. Для определения — кому показано динамическое наблюдение учитывается возраст больного и сопутствующие заболевания.
Динамическое наблюдение проводится у пожилых людей с предполагаемой продолжительностью жизни не более 10 лет, при отсутствии признаков прогрессирования опухоли. Это считается более целесообразным, поскольку рост опухоли медленный, а лечение онкологии может ухудшать соматический статус пациента, обладая рядом побочных действий.
Однако выбор всегда остается за пациентом, не каждый может принять выжидательную тактику, поскольку это серьезное психологическое испытание, приводящее к депрессии, ухудшению качества жизни. Также существует риск, что опухоль будет прогрессировать быстрее, нежели ожидалось и тогда понадобится более агрессивнее лечение, к тому же эффективность терапии на поздних стадиях ниже.
Причины, по которым возможно отсутствие эффекта от лечения сегодня недостаточно изучены, но определенные факты могут способствовать развитию рецидива:
- перед подготовкой к лечению или операции стадия онкологического процесса была определена не верно из-за несовершенства методов обследования;
- при динамическом наблюдении рост опухоли был более стремительным, в результате новообразование вышло за капсулу простаты;
- до лечения уже произошло проникновение раковых клеток в близлежащие ткани, на сегодняшний день не существует методов, определяющих распространение единичных патологических клеток по организму;
- при нечувствительности клеток опухоли к стандартным дозам облучения, при ситуации, когда участки предстательной железы не могут попасть в зону облучения или когда произошло проникновение опухоли за пределы облучения.
Это зависит от того, насколько агрессивна была первичная опухоль, высокодифференцированные опухоли дают рецидив медленнее, низкодифференцированные быстрее, обычно рецидив происходит в первые 5 лет, но бывают случаи возникновения рецидива после лечения через 15 лет.
Сначала (в первые годы) рецидив может протекать бессимптомно, раньше считалось, что трудности с мочеиспусканием, боли в костях, увеличение лимфатических узлов свидетельствуют о рецидиве, но это уже указывает на множественные метастазы. Сегодня о начале рецидива можно узнать по росту ПСА. Если отсутствуют прочие проявления рака, а ПСА увеличивается, то говорят о биохимическом рецидиве и только спустя несколько лет у такого пациента начинают проявляться признаки роста опухоли. Поэтому важным условием после проведения курса терапии является контроль ПСА, биопсия, пальцевое ректальное исследование, МРТ, КТ, остеосцинтиграфия.
При раке предстательной железы метастазы могут быть местными (регионарные лимфоузлы) и отдаленные — это любые органы, чаще всего это бедренные и плечевые кости, позвоночник, легкие, печень, головной мозг.
Оснований для таких опасений нет, биопсия не влияет на рост опухоли, более того это важнейшая составляющая диагностики, легкая и безопасная процедура, достоверный метод отвергающий или подтверждающий наличие рака простаты.
Операция не может быть методом профилактики, поскольку это серьезное вмешательство с возможным комплексом осложнений, таких как импотенция и недержание мочи. Кроме того, рак простаты достаточно медленно прогрессирует и у многих пациентов он не становится причиной смерти или резкого ухудшения здоровья, поскольку причиной смерти за это время могут стать прочие заболевания.
На сегодняшний день не существует ни единого народного способа или метода нетрадиционной медицины способного вылечить это заболевание. Более того, использовать только какие-либо прочие способы лечения и откладывать эффективную терапию, предлагаемую специалистами, опасно. Затягивание с лечением может увеличивать риск прогрессирования опухоли и возникновения метастазов.
В странах, где традиционно высокий уровень потребления рафинированных продуктов и излишков животных жиров, таких как Европейские страны, Канада, США риск возникновения онкологии намного выше, чем в странах, население которых питается соей, рисом и морепродуктами. Также выявлена связь повышенного риска рака простаты у мужчин с ожирением, при этом увеличивается риск не только онкологии, но и гипертонии, атеросклероза сосудов головного мозга, сахарного диабета у мужчин.
Следует помнить, что своевременная диагностика рака предстательной железы — залог успешного выздоровления! Поэтому при любых неприятных ощущениях не затягиваете поход к специалисту-урологу.
Читайте также:



