Ампутация руки при саркоме
Саркома мягких тканей слабо чувствительна к химио- и лучевой терапии и дает рецидивы при операциях, когда не удается убрать все пораженные ткани. Чтобы лечение было успешно, нужно усиливать действие химиотерапии и избежать резкого всплеска метастазирования и роста саркомы после операции.

Метод общей электромагнитной гипертермии своим высокотемпературным воздействием (от 42,5 °С и выше):
- усиливает действие лучевой терапии и химиопрепаратов;
- стимулирует противоопухолевый иммунитет;
- повреждает жизнеспособность клеток саркомы до операции, что снижает риск метастазирования и рецидива после.
При лечении саркомы мягких тканей гипертермией становится возможным:
- выполнение органосохранных операций, а не ампутаций и травмирующих;
- предупреждение рецидивов болезни;
- уменьшение дозы облучения или отпадает необходимость проведения лучевой терапии.
В клинику “К-тест” больных с саркомами мягких тканей принимают на лечение из любых регионов России и СНГ, Европы. Ознакомиться с условиями размещения пациентов и их сопровождающих можно в соответствующем разделе.
Саркома мягких тканей: результаты лечения гипертермией
Предыстория: Большинство пациентов поступали к нам с устойчивостью к нескольким схемам химиотерапии. Они имели высокозлокачественные опухоли размером более 5 см с метастазами. У 42 % больных первичная опухоль была неудалимой. Другой части больных уже были проведены травмирующие операции, множественные курсы химио- и лучевой терапии. На фоне проводимого лечения наблюдалось только прогрессирование. После радикальных операций метастазирование и неоперабельные рецидивы выявлялись в среднем через 20 месяцев.
Таким образом, мы приступали к лечению крайне тяжелой и малоперспективной категории больных. Общая гипертермия проводилась как последняя попытка добиться ремиссии.
Но и при таких исходных данных гипертермия давала эффект: под действием температуры опухоль некротизировалась, уменьшалась, что позволяло отказаться от ампутации конечностей.
Клинический пример:
Больная О., 53 года. Диагноз: Саркома мягких тканей правой подколенной области.
В феврале 2017 года была обнаружена опухоль в подколенной области. Обратилась за помощью в ЦРБ по месту жительства через 6 месяцев. Выполнена операция – удаление опухоли. Гистология: миксофибросаркома. Через 2,5 мес. появился рецидив опухоли. В январе 18 выполнена химиоэмболизация артерий опухоли. В феврале иссечена рецидивная опухоль. Иммуногистохимия: эмбриональная рабдомиосаркома.
Поступила в клинику К-тест в феврале 2018 года. С незажившей раной, некрозами кости в подколенной области. Больной проведено 5 курсов гипертермии с химиотерапией в период с февраля по август 18 года. После заживления раны в послеоперационном рубце в январе 2019 года выявлен узел 13х10 мм. В феврале 2019 года произведено удаление рецидивной опухоли. Гистология: рабдомиосаркома 3 стадии лечебного патомарфоза. Послеоперационная рана зажила. При контрольных обследованиях признаков рецидива и отдаленных метастазов не выявлено через 3,6 и 9 месяцев.
3 стадия патаморфоза говорит о глубоком повреждении опухоли и о практическом отсутствии потенциала для рецидивирования и метастазирования.
НЕПОСРЕДСТВЕННЫЕ РЕЗУЛЬТАТЫ. 155 больных в выборке:
| Диагноз | Полная регрессия | Частичная регрессия | Стабили зация | Улучшение качества жизни |
| Саркомы мягких тканей T2bN0M1 | 3,6 % | 36,4 % | 47,3 % | 83,6 % |
Подсчет показателей выживаемости проводился по методу Каплана — Майера. Результаты достоверны (P ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ
Достигнутый в результате гипертермии пятилетний рубеж пережили 49,8 % больных саркомами мягких тканей с 4-й стадией.
Выживаемость с саркомами 4-й стадии, прошедших лечение гипертермией
| Диагноз | 1 год | 3 года | 5 лет |
| Саркомы мягких тканей, 4-я стадия | 94,2 % | 68,2 % | 49,8 % |
Подсчет показателей выживаемости проводился по методу Каплана — Майера. Результаты достоверны (P Наилучшие результаты получены при лечении следующих видов сарком мягких тканей:
- лимфосаркомы;
- липосаркомы;
- ангиолейомиосаркомы;
- синовиальные саркомы;
- злокачественные невриномы;
- мезенхимомы;
- злокачественные шванномы;
- миксомы;
- саркомы GIST;
- хондросаркомы.
По локализации наиболее успешно лечатся саркомы желудочно-кишечного тракта, саркомы матки и забрюшинного пространства.
Если после 2-3 курсов проводимой химиотерапии в рамках стандартного лечения по ОМС нет заметной положительной динамики, улучшения самочувствия, уменьшения размеров опухоли и метастазов, то следует задуматься о необходимости усиления химиотерапии нагревом. Дальнейшее продолжение стандартной химиотерапии при отсутствии динамики, даже со сменой химиопрепаратов, приведет только к устойчивости саркомы к лекарствам.
Мы остановились на схемах, наиболее изученных при саркомах мягких тканей. Применяя известные режимы полихимиотерапии (комбинирование нескольких препаратов), мы получили возможность сравнить их эффективность и токсичность в обычных условиях и в условиях гипертермии. Химиопрепараты вводились на высоте максимального нагрева в дозе 50–70 % от курсовой дозы и давали в разы больший эффект, чем без нагрева.
Перспективно также применение на фоне общей гипертермии новых противоопухолевых средств. Нескольким пациентам в ходе гипертермии вводился препарат Йонделис®, мы видим быстрый и мощный эффект, но окончательные выводы пока делать рано.
Что касается осложнений химиотерапии в сочетании с общей гипертермией, то они встречались реже, чем при классической химиотерапии, и были легкими по степени тяжести.
Инфильтративный рост является собенностью заболевания. Саркома относится к группе злокачественных опухолей, лечение которых затруднено из-за наличия:
• инфильтрирующего роста опухоли, которая разрушает расположенные рядом ткани;
• частых рецидивов после удаления саркомы;
• быстрого развития метастазов, распространяющихся в легкие или печень.
Саркома может развиваться без симптомов, причем общая клиническая картина очень схожа с болезнями не опухолевого характера или доброкачественными опухолями. Лечение саркомы требует несколько специфического подхода о котором мы расскажем в данной статье.
Новые технологии приходят в Россию.
Приглашаем пациентов принять участие в новых методах лечения онкологических заболеваний, а также в клинических испытаниях препаратов на основе Т-клеток (LAK-терапия). Терапия проводится в различных научно-исследовательских онкологических центрах, в зависимости от вида опухоли.
Отзыв о методе министра здравоохранения РФ Скворцовой В.И.
Комментарий о клеточных технологиях главного онколога России, академика Давыдова М.И.
Саркома подразделяется на виды
Синовиальная саркома - злокачественная опухоль, местом возникновения является синовиальная оболочка суставов, синовиальные сумки, сухожилия или фасциально-апоневротические структуры. Синовиальная саркома может возникнуть в различных областях тела, но наиболее часто она возникает в крупных суставах конечностей.
Липосаркома - злокачественное новообразование жировой ткани. Ее рост за очень короткий промежуток времени способен достигать огромных размеров. Визуально опухоль представляет собой мягкий узел овальной формы с четкими границами. На разрезе просматривается серый, белый или желтоватый цвет, что характерно для эмбрионального происхождения опухоли. Отличительной чертой данной саркомы является то, что она может быть множественной. Метастазирование проходит гематогенно и лимфогенно.
Рабдомиосаркома - ростет из мышечной ткани. Локализация данной опухоли это конечности, голова или шея. Бывают одиночного, многодольчатого и мультицентрического типа. На разрезе серо-розовый или бурый цвет, в большинстве случаев с очагами некрозов и кровоизлияний. Метастазирование проходит гематогенно, чаще в легкие.
Ангиосаркома - развитие данной опухоли происходит из элементов стенок кровеносных сосудов. Данный вид опухоли очень агрессивен по причине быстрого распространения метастазов. Локализация различная. На разрезе беловато-серый, желто-розовый цвет, часто с множественными кистами, с кровянистым содержанием, некрозами и кровоизлияниями. Микроскопически данная саркома подразделяется на 2 подвида: гемангиоперицитому и злокачественную гемангиоэндотелиому.
Саркома, признаки и симптомы
Начальным признаком саркомы считается узел или припухлость в какой-либо части тела. Такое образование имеет овал или круглую форму, часто безболезненную. Распространение и рост опухоли определяется исходя из вида саркомы. При быстром росте саркомы, ее поверхность может содержать сеть подкожных вен, имеет цианотичную окраску с изъявлениями. Пальпация опухоли показывает ее ограниченную подвижность.
Изредка саркома дает осложнение - происходит деформация конечностей, при этом функции рук и ног сохраняются. Саркома характеризуется агрессивным ростом, распространяется преимущественно по межфасциальным пространствам, вдоль пораженных мышц, саркома часто растет в виде тяжей опухолевой инфильтрации. Именно в связи с сохранением участков таких тяжей после нерадикального иссечения опухоли и отмечаются такие частые и типичные для сарком мягких тканей явления, как рецидивы и продолженный рост опухоли.
Саркома распространяется гематогенным метастазированием. Частота гематогенного метастазирования составляет от 25 до 100 %. Так, липосаркомы и фибросаркомы G1 метастазируют редко, а вот неклассифицируемые саркомы, злокачественные гистиоцитомы характеризуются ранним метастазированием. Поражение регионарных лимфатических узлов является менее характерной особенностью сарком мягких тканей и встречается обычно в 20 % случаев. Во всех подобных случаях прогноз становится крайне неблагоприятным.
Характерными ранними признаками сарком мягких тканей является появление подвижной опухоли, что в ряде случаев может сопровождаться появлением болей и нарушением функции сустава, расположенного вблизи опухоли. По мере ее роста и вовлечения периферических нервов, сосудов, капсулы суставов, костей клиническая картина дополняется новыми симптомами — интенсивными болями, тромбофлебитами, нарушением функции конечности, свидетельствующими о запущенности процесса. Об этом же свидетельствует и манифестация общих явлений опухолевого поражения: анемии, лихорадки, интоксикации, потери массы тела больного.
Диагностика заболевания саркома
При обследовании необходимо собрать анамнез, клинически оценить состояние больного, провести лабораторные и инструментальные методы исследования. В комплексе диагностических исследований гистологическому анализу придается главенствующее значение.
- магнитно-резонансная томография (МРТ) проводится при локализации опухоли вблизи костей осевого скелета;
- ангиография магистральных сосудов в зоне опухолевого роста (при больших опухолях конечностей, верхнего и нижнего тазового поясов);
- остеосцинтиграфия.
Проводимые исследования направлены на уточнение распространения опухоли, что позволяет избирательно подходить к выбору метода лечения. Диагностирование саркомы мягких тканей завершается определением стадии заболевания, а также оценкой резектабельности опухоли и риска хирургического вмешательства, что предусматривает проведение необходимого объема функциональных исследований.
Терапия
Выбор метода терапии пациентов с заболеванием саркома базируется на оценке стадии процесса, распространенности опухолевого образования. При этом используются методы лучевой терапии, хирургический, химиотерапевтический метод.
При лечении заболевания саркома необходимо соблюдать правила:
Радикальными признаются операции, сопровождающиеся удалением саркомы в пределах мышечно-фасциального футляра, либо когда применяется широкое иссечение опухоли и здоровых тканей с отступлением от краев опухоли во все стороны не менее 5 см. При снижении этой ширины до 2 см (простое иссечение) операция считается условно-радикальной, а менее 2 см — нерадикальной, так как нередко сопровождается нарушением целостности опухоли.
К радикальному лечению заболевания саркома относятся еще два варианта операций: радикальная резекция, а также ампутация и экзартикуляция конечности. Контроль радикальности оперативного вмешательства проводится в результате срочного интраоперационного гистологического исследованиятканей по краю резекции.
Интраартериальная химиотерапия

Лучевая терапия при заболевании саркома
Проведение предоперационного облучения предпринимается с целью снижения злокачественного потенциала опухоли. Суммарная очаговая доза составляет 40—50 Гр, операция выполняется через 3 недели. В результате создаются благоприятные условия для выполнения радикального вмешательства и возможность уменьшения объема резекции. Такой подход приводит к существенному снижению частоты рецидивов саркомы. Вместе с тем известно, что при неоадъювантной лучевой терапии отмечается более высокий процент послеоперационных осложнений, особенно связанных с некрозом кожного лоскута и слабым заживлением раны. При отсутствии морфологической верификации опухоли проведение неоадъювантной лучевой терапии противопоказано.
Послеоперационное облучение проводится при опухолях более 5 см, при сомнительности в радикальности операции и с целью уничтожения предполагаемых диссеминированных в ране клеток опухоли. Назначается через 3 недели после операции при наличии окрепшего послеоперационного рубца. СОД составляет обычно 50—70 Гр, облучение проводится в режиме классического фракционирования. К моменту проведения послеоперационной лучевой терапии уже обычно известно гистологическое заключение о морфологической форме удаленной опухоли и степени ее злокачественности, а также о наличии или отсутствии опухолевых клеток в краях резекции. При наличии остаточной опухоли, маркированной во время операции, эта зона дополнительно облучается до СОД не менее 70 Гр. Целесообразно использование радиомодификаторов (гипертермия, методы оксигенация), избирательно усиливающих противоопухолевое воздействие радиоактивного излучения.
Органосохраняющие операции при заболевании саркома
Различные варианты ампутаций и экзартикуляций в течение многих лет до появления комбинированной и комплексной терапии признавали основными и наиболее радикальными. Однако такие обширные хирургические вмешательства сопровождались существенным увеличением частоты отдаленного метастазирования, а в 10—15 % — местными рецидивами опухоли и не влияли на продолжительность жизни больных. Пересмотр хирургической тактики совпал с усовершенствованием диагностики, внедрением новых технологий, муль-тидисциплинарных подходов с рациональным использованием основополагающих методов лечения в онкологии. В результате частота калечащих операций снизилась до 10 %, а вмешательства, сопровождавшиеся сохранением конечности, быстро вошли в повседневную практику онкохирургов.
Даже больные с многократно рецидивирующими саркомами, которым обычно выполнялись ампутации конечности, теперь лечатся в соответствии с современными подходами. Выполняемое при этом оперативное вмешательство носит название радикальная частичная резекция, или радикальная сберегающая операция. Она заключается в полном удалении единым блоком в мышечно-фасциальном футляре вместе с опухолью фасций и окружающих мышц, что может сопровождаться резекцией сосудов, нервов, костей, суставов и их одномоментной реконструкцией.
Ампутация показана для удаления сарком больших размеров с признаками инфицирования, кровотечения, инфильтрации окружающих тканей, для которых органосохраняющий подход не гарантирует оптимального функционального результата. По принятым правилам она производится на вышележащем сегменте конечности. Поэтому при поражении опухолью проксимального отдела плеча, ключицы или лопатки онкологически оправданной является межлопаточно-грудная резекция, а при локализации в области таза - межподвздошно-брюшная резекция.
Для подбора эффективного метода лечения вы можете обратиться за
- методы инновационной терапии;
- возможности участия в экспериментальной терапии;
- как получить квоту на бесплатное лечение в онкоцентр;
- организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.
Саркомами называют опухоли, которые развиваются из клеток предшественниц соединительной ткани — мезодермы. Как и рак, они представляют собой злокачественные новообразования, но с той разницей, что источником раковой опухоли является эпителий, выстилающий внутренние органы и тело человека. Поэтому эти опухоли имеют привязку к конкретному органу, например, рак предстательной железы, рак молочной железы и др. Саркомы же развиваются из соединительной ткани и могут возникнуть в любом органе, где есть такие клетки, то есть фактически везде.
- Виды сарком мягких тканей
- Стадии развития
- Факторы риска
- Симптомы саркомы мягких тканей
- Диагностика саркомы мягких тканей
- Лечение саркомы мягких тканей
- Прогноз выживаемости при саркоме мягких тканей
Виды сарком мягких тканей
Саркома мягких тканей — это собирательный термин, который объединяет большое количество злокачественных опухолей, среди которых наиболее часто встречаются следующие:
- Лейомиосаркома — опухоль из гладкомышечных клеток.
- Рабдомиосаркома — опухоль из поперечно-полосатой мускулатуры.
- Липосаркома — злокачественная опухоль из жировой ткани.
- Ангиосаркома — злокачественное новообразование, произрастающее из ткани кровеносных сосудов.
- Фибросаркома — опухоль из фиброзной ткани.
Также саркомы мягких тканей принято разделять по степени злокачественности. Низкозлокачественные новообразования редко метастазируют, но склонны к упорному рецидивированию. Высокозлокачественные опухоли склонны давать метастазы гематогенным путем (с током крови), лимфатические узлы поражаются реже.
Стадии развития
Стадия саркомы мягких тканей определяется степенью злокачественности опухоли, ее размером и наличием метастазов.
- К 1 А стадии относят новообразования низкой степени злокачественности, размером менее 5 см, без метастазов в регионарных лимфатических узлы и отдаленных органах.
- 1 В стадия — опухоли низкой степени злокачественности, более 5 см без метастазов.
- 2А стадия — новообразования средней степени злокачественности, менее 5 см без метастазов.
- 2В стадия — новообразования средней степени злокачественности, более 5 см в наибольшем измерении, без метастазов.
- 3А стадия — саркомы высокой степени злокачественности, менее 5 см без поражения лимфатических узлов и внутренних органов.
- 3В стадия — саркомы высокой степени злокачественности, более 5 см без метастазов.
- 4 стадия — саркома любой степени злокачественности, любого размера при наличии поражения лимфатических узлов или метастазов во внутренних органах.

Факторы риска
В большинстве случаев, саркомы мягких тканей развиваются спонтанно, т. е. без видимых причин. Однако есть определенные обстоятельства, которые увеличивают вероятность развития данного заболевания:
- Воздействие химических канцерогенов, в частности гербицидов, хрорфенолов.
- Генетическая предрасположенность — нейрофиброматоз, синдром Ли-Фраумени, синдром Гарднера.
- Воздействие ионизирующего излучения, например, прохождение лучевой терапии.
- Иммунодефицитные состояния — иммуносупрессия после трансплантации органов, прохождение химиотерапии, СПИД.
- Некоторые виды сарком мягких тканей могут развиваться на фоне лимфостаза конечности.
Симптомы саркомы мягких тканей
На начальных этапах, саркома мягких тканей проявляется как безболезненная опухоль, которая медленно увеличивается в размерах. Может иметь капсулу, которая, впрочем, не мешает метастазированию. Также опухоль может иметь инфильтративный рост, в этом случае определить ее края проблематично.
При дальнейшем росте, симптоматика будет зависеть от локализации опухоли. Например, при саркомах матки будут кровотечения, при поверхностной локализации опухоль вызывает отечность и боли, при этом нарушается функция пораженного органа, например, руки или ноги.
Диагностика саркомы мягких тканей
В рамках диагностики саркомы мягких тканей проводится физикальное обследование, используются методы медицинской визуализации с последующим проведением биопсии и морфологического исследования полученного материала.
Обязательно проводится КТ или МРТ пораженной области. Во-первых, исследование помогает обнаружить опухоль, а во-вторых проконтролировать радикальность излечения.
Для постановки диагноза обязательно проводится морфологическое исследование фрагмента опухоли. Чтобы его получить, выполняют трепанбиопсию с помощью специальной толстой иглы под контролем УЗИ, или инцизионную биопсию, которая подразумевает хирургическое иссечение фрагмента новообразования. В ряде случаев, для уточнения типа саркомы необходимо более детальное исследование, тогда проводят иммуногистохимические и молекулярно-генетические анализы.
Для того чтобы установить степень распространения опухоли, проводят КТ грудной клетки, брюшной полости, а также ультразвуковое исследование лимфатических узлов.
Лечение саркомы мягких тканей
Выбор метода лечения саркомы определяется степенью ее злокачественности, местом расположения и наличием метастазов. Для лечения низкозлокачественных опухолей, лечение преимущественно хирургическое, в остальных случаях используются комбинированные методы, включающие облучение и химиотерапию.
При хирургическом лечении сарком используются следующие виды операций:
- Широкая местная резекция. Таким способом удаляются низкозлокачественные небольшие новообразования, располагающиеся в коже и подкожной клетчатке.
- Широкое иссечение. При таком вмешательстве саркома удаляется в пределах анатомической зоны, отступая от края новообразования не менее чем на 4-6 см.
- Радикальная органосохраняющая операция. При таком объеме вмешательства удаляется опухоль совместно с мышечными фасциями и неизмененными мышцами, которые отсекаются в месте их прикрепления. При вовлечении в процесс кровеносных сосудов, нервных стволов и костей, производят их резекцию с одномоментной пластикой кожным или кожно-мышечным лоскутом.
- Ампутации или экзартикуляции — удаление конечности или ее вычленение по линии суставной щели. Такие вмешательства проводятся при обширных местно-распространенных высокозлокачественных процессах с вовлечением магистральных кровеносных и нервных стволов на большом протяжении, а также костных структур и мышц.
Во время операции обязательно проводится интраоперационное срочное гистологическое исследование. При наличии злокачественных клеток в краях отсечения и при потенциальной возможности радикального удаления опухоли, выполняют реоперацию.
Лучевая терапия применяется в рамках комбинированного лечения в предоперационном и/или послеоперационном этапе. В первом случае преследуется цель — уменьшение размера саркомы и создание условий для проведения радикального вмешательства. Во втором — уничтожение оставшихся злокачественных клеток. Чтобы воздействие на опухоль было равномерным, используются многопольные методики облучения.
Предоперационная лучевая терапия
При предоперационной ЛТ, границы полей облучения (ПО) должны выходить за размеры ткани опухоли минимум на 3-4 см. Если опухоль имеет большие размеры, производят облучение в пределах 10 см от ее края до достижения суммарной очаговой дозы 45-50Гр. Затем ПО сокращают до размеров новообразования.
Если опухоль располагается на конечности, есть вероятность развития остеолучевого некроза, мышечных контрактур и отеков. Чтобы этого избежать, рекомендуется облучать не более 2/3 окружности конечности, если это возможно. Минимальная толщина необлучаемых тканей в зоне предплечья составляет 2 см, на бедре 4 см, и на голени — 3 см.
Послеоперационная лучевая терапия
Послеоперационная лучевая терапия показана в следующих случаях:
- Высокая степень злокачественности саркомы по данным гистологического исследования.
- Нерадикально проведенная операция — наличие злокачественных клеток в краях отсечения при невозможности проведения реоперации.
- Вскрытие капсулы саркомы во время хирургического вмешательства.
Послеоперационную ЛТ начинают выполнять не позднее, чем через 4 недели после окончания хирургического лечения.
Если предоперацинная ЛТ не выполнялась, поля облучения включают в себя следующие области:
- Ложе опухоли.
- Ткани, которые располагаются на расстоянии 2 см от удаленной опухоли.
- Послеоперационный рубец.
Облучение проводят в суммарной очаговой дозе 60 Гр. Если была проведена нерадикальная операция, дозу увеличивают до 70 Гр. В аналогичном режиме проводят лучевую терапию при невозможности оперативного лечения.
Химиотерапия широко используется для лечения высокозлокачественных сарком мягких тканей. Как и при лучевой терапии, ее могут назначать на дооперационном и/или послеоперационном этапе. Неоадъювантная (предоперационная) ХТ призвана воздействовать на очаг опухоли, уничтожать микрометастазы и создать условия для органосохраняющего хирургического лечения. С этой целью проводят 2-3 курса химиотерапии с перерывом в 3-4 недели.
Послеоперационная ХТ может проводиться для уничтожения микрометастазов или уже визуализируемых метастазов. С этой целью выполняют 3-4 курса лечения. При химиотерапевтическом лечении сарком применяют различные комбинации следующих препаратов:
- Доксорубицин.
- Этопозид.
- Винкристин.
- Ифосфамид.
- Дакарбазин.
- Цисплатин и др.
Схема химиотерапии будет определяться морфологическим вариантом опухоли и ее чувствительностью к ранее проводимому лечению.
Прогноз выживаемости при саркоме мягких тканей
Прогноз выживаемости зависит от многих факторов:
- Степень злокачественности саркомы. Наиболее благоприятное течение у низкозлокачественных сарком без метастазов во внутренних органах и лимфоузлах.
- Размеры опухоли.
- Возможность проведения радикального лечения.
- Возраст больного. Наиболее благоприятные прогнозы у детей. У них полного выздоровления удается достичь в 60% случаев. Наименее благоприятные прогнозы у людей старше 60 лет.
При своевременном лечении начальных стадий низкозлокачественных сарком мягких тканей, удается достичь 5-летней выживаемости у половины больных. При 4 стадии процесса, этот показатель не превышает 10%.
Эффективных методов профилактики саркомы мягких тканей нет. Общие рекомендации являются стандартными — отказ от вредных привычек, ведение здорового образа жизни.


Александр с женой Юлией. Фото: Yulia Bocharova / Facebook
19-летний Александр Бочаров, конечно, не был готов к ампутации левой ноги. Он старался избегать этой темы и менял врачей, как только те начинали говорить про операцию. С юношеским максимализмом и пафосом Александр заявлял маме, что хочет, опустив голову, видеть оба ботинка.
К тому моменту он уже несколько лет боролся с остеосаркомой. В левую ногу вместо сустава, который пришлось удалить вместе с опухолью, ему поставили эндопротез — искусственный сустав, но, как это часто бывает, возникло инфицирование. Пока врачи боролись с инфекцией, случился рецидив опухоли, она поразила больший участок, появились метастазы в легких, и ампутация ноги, причем на достаточно высоком уровне, была уже вопросом жизни, а не желания. К тому же опухоль росла и доставляла сильную боль.
Сразу после операции он почувствовал облегчение. Год ходил на костылях, а потом попросил самый простой в использовании протез, чтобы как можно быстрее научиться им пользоваться.
— Давай сделаем тебе получше? — предлагали врачи.
— Нет, я хочу, чтобы встал и пошел. Чтобы дорогу можно было перейти, пока горит зеленый свет светофора.
Первый протез Александра был по сути палкой, сгибающейся в области колена, и как научился он ходить на этой палке — неправильно, резко — так и продолжает ходить неправильно уже на суперсовременном протезе за три миллиона рублей. На самом деле была еще одна причина, почему Бочаров не думал о качестве протезирования — три года после операции, до 2010-го, он был пациентом паллиативного отделения.

Сейчас у Александра современный электронный протез
— Прогноз неблагоприятный, я скоро умру, зачем мне этот протез? Я такие соображения никому, конечно, не озвучивал, особенно маме. Пока я занимался метастазами в легких. И в принципе, так как я уже на костылях адаптировался и так как мне убрали основной источник боли и дискомфорта, для меня это уже была свобода.
Я жил в 60 километрах от Москвы, в деревне, но при этом на этих костылях ездил в Москву — идти мне 400 метров до остановки, потом ехать полтора часа в автобусе, потом эскалаторы, метро, час пик. Сначала я просил друзей сопровождать меня, потом подумал, что они же не могут быть постоянно со мной, у них свои дела, а мне надо справляться самому. Иногда в метро в час пик меня толкали, я падал. Правда, не всегда помогали подняться. Сначала меня это удивляло, а потом я спокойно стал к этому относиться — у каждого свое видение проблемы.
Когда, вопреки прогнозам, Александр Бочаров вошел в ремиссию, друзья-благотворители помогли ему купить электронный протез. Еще через несколько лет он получил протез от государства.
— Когда тебе дают протез, кажется, что все просто — наденешь и пойдешь, ты же раньше ходил, знаешь, как это делать на двух ногах. Но оказывается, здесь давит, тут жестко, там неудобно, и тогда ты думаешь — на нем стоять-то невозможно, как на нем ходить вообще? — рассказывает Александр. — Потом протезисту говоришь, где тебе мешает, и он исправляет эти моменты, потому что иначе будет постоянно натирать и образуется рана на культе. Дальше учишься ходить: сначала брусья, ты вдоль них ходишь с двумя опорами, тебе рассказывают, как ставить ногу, как плечи держать. Лучше это делать перед зеркалом, потому что мозг автоматически идет по пути наименьшего сопротивления — протезом ты неосознанно делаешь короткий шаг, а своей ногой длинный. Надо мозг переучивать.
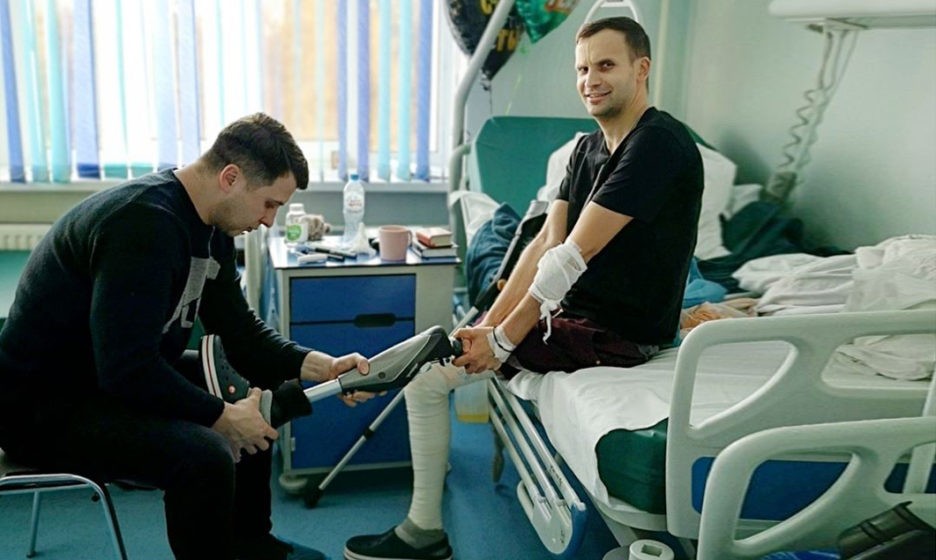
Настройка протеза
Все зависит от того, насколько человек хочет научиться ходить, говорит Бочаров. Кто очень хочет, может освоить протез за месяц, кто ленится, как он, тому нужно больше времени, а кто-то совсем отказывается от протеза или использует его возможности по минимуму, в основном передвигаясь на костылях, потому что считает, что не справится.
— Вообще научиться ходить на протезе — это как научиться ездить на велосипеде, не нужна ни физическая подготовка особенная, ни особые усилия. Нужно понять технику и научиться держать баланс, но, конечно, лучше, когда занимаешься с реабилитологом и поддерживаешь в тонусе не только мышцы ампутированной ноги, но и все тело, — рассказывает Александр.
Государство предоставляет бесплатно два протеза — для душа и основной, основной можно менять раз в три года. В случае с онкологическими больными государство оплачивает дорогой электронный протез, только если человек пять лет прожил в ремиссии. Почему именно такая цифра, Бочаров не знает, ведь рецидив может возникнуть и на шестой год. Неэлектронные, которые тоже очень активны, но стоят до миллиона рублей, можно получить сразу.
Протез ноги — модульная конструкция, то есть состоит из нескольких частей: стопа, она компенсирует нагрузку на спину, смягчает удары, потом голень, коленный модуль и культеприемная гильза, которая уже крепит протез к культе. Есть еще поворотный модуль, удобная, маленькая, но очень дорогая штука. За счет этого можно подогнуть ногу под себя или, наоборот, поднять на уровень рук, чтобы, например, завязать шнурки. Выглядит не очень приятно, поэтому Александр всегда предупреждает, когда собирается это сделать. Устройство культеприемной гильзы позволяет носить протез неограниченное количество времени. Ощущение, говорит Бочаров, такое же, как когда долго ходишь в обуви — теоретически в ботинках можно даже спать, но какое облегчение чувствуешь, когда снимаешь их после долгого дня.
Современный электронный протез — это практически собственная нога. Он, конечно, стоит, как дорогой автомобиль или однокомнатная квартира в недалеком Подмосковье, зато почти полностью обеспечивает качественную жизнь, только получить его непросто — придется как минимум сразиться с бюрократической машиной. Чтобы государство оплатило протез за три миллиона, Бочаров прошел повторное медицинское освидетельствование и подтвердил инвалидность.
— Несмотря на то что у меня есть все документы, там проверили все, вплоть до того что измерили рост, объем груди. Они выясняют, насколько он тебе нужен, так как есть определенные показания и противопоказания, и они парадоксальны, — рассказывает Александр. — На электронном протезе легче и безопаснее ходить, ему можно больше доверять, это позволяет снизить нагрузку на здоровую ногу, позволяет активнее ходить по лестницам и тратить на это меньше энергии. И наоборот, чтобы ходить на неэлектронном протезе, нужен определенный навык, там идет сильная нагрузка на суставы, перекос по спине, поэтому возникают проблемы с позвоночником и сердечно-сосудистой системой. А по закону человеку, у которого и так уже есть проблемы с этим, положен протез, на котором тяжело ходить.
На своем электронном протезе Бочаров передвигается без проблем. Более того, сейчас у него сломана нога, поэтому протез берет на себя основную нагрузку. Александр надевает его с утра, как только просыпается. Чтобы умыться, наклоняется над раковиной, зафиксировав положение коленного модуля так, как если бы это была его собственная коленка. Он спускается и поднимается по лестнице, ходит в походы в горы, ездит на велосипеде, катается на коньках, серфит и занимается фехтованием.

Александр на тренировке
В ответ на вопрос, что нельзя делать, если у тебя протез ноги, Александр смеется:
— Не знаю, придумайте что-нибудь. Мне ничего в голову не приходит.

Подзарядка протеза в машине
А недавно Александр встал на беговой протез:
— Нельзя передать эти ощущения, когда ты 12 лет не прыгал и не бегал. Я забыл, как прыгать на двух ногах, сначала мне даже помогали — держали за руки. Прыгаешь как дурачок и не можешь остановиться, набегаться, напрыгаться. Я же раньше, как Форест Гамп, всегда бежал. Такое счастье было снова испытать эти ощущения.
Еще 10 лет назад, когда Александр шел по улице в шортах и светил новеньким механическим протезом, люди оборачивались и едва не показывали пальцем. Сейчас человеком с протезом руки или ноги никого уже не удивишь, но даже в те не самые простые времена у Александра не было главного, что мешает жить полноценно, — синдрома инвалида.
— Я не ощущал себя инвалидом благодаря моим друзьям. Невзирая на то, что я был на химии, без волос и ресниц, на костылях, прятался от солнца, они проводили со мной время и прекрасно справлялись с тем, чтобы меня никто не пнул, не толкнул в толпе. Без сожаления, без жалости, они относились спокойно к моей болезни, а о помощи зачастую не надо было даже просить — они сами видели, что мне нужно, — рассказывает Александр.

С протезом Александр Бочаров ведет активный образ жизни
— Некоторые настолько боятся ампутации, что 15 лет мучаются с этими инфекциями, врачи кульбиты делают, пытаются сохранить ногу, а она уже нормально не функционирует. Одна девушка так 14 лет жила, потом все-таки решилась на операцию, причем ей ампутировали ногу с вычленением бедра из таза. Протезист спрашивает меня через какое-то время, где она, почему не приходит делать протез. А ей некогда, нога ей не мешает, она зажила — конкурсы красоты для инвалидов, мероприятия разные, у детей олимпиады.
Для своих детей Александр придумал историю — говорит, что пират. Сын-второклассник доказывает друзьям, что папа воевал на море, сражался с Саркомотом, тот его ужалил, другой пират наступил на ногу. А крови много было? — спрашивают дети. — Много! — отвечает, — но потом доктор на корабле все зашил.
Читайте также:





