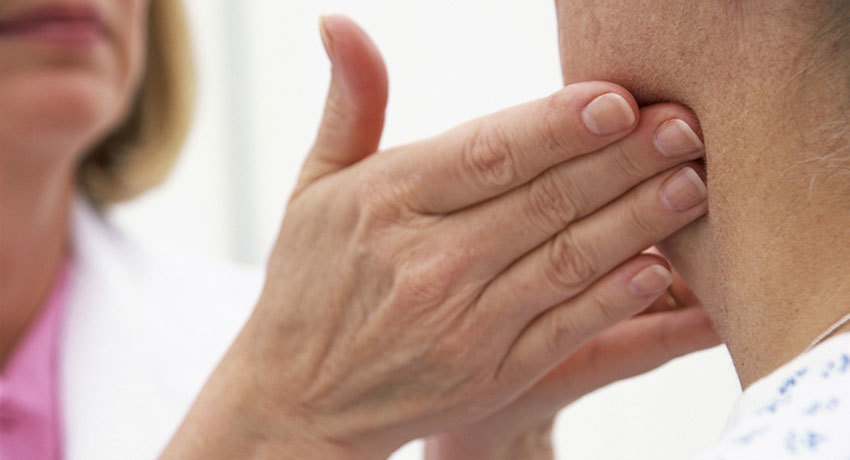
Американские исследования фолликулярной лимфомы

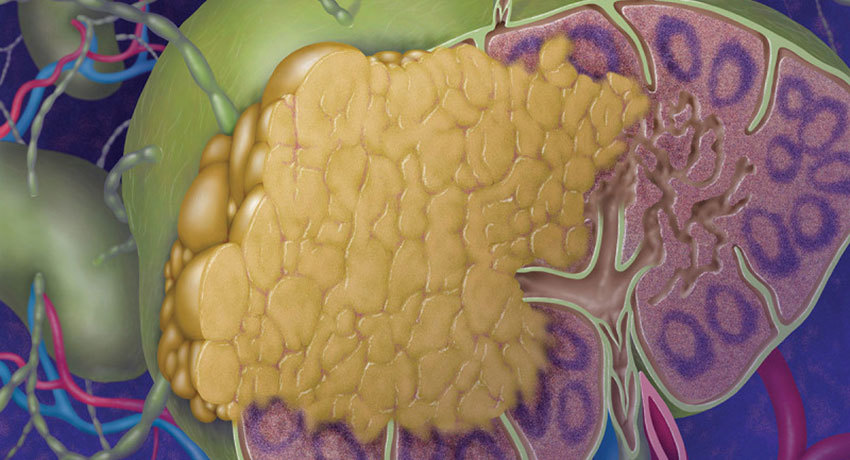
Фолликулярная лимфома костного мозга
Ed Uthman / flickr
Это уже второй подобный случай: 30 августа 2017 года впервые было одобрено использование генной терапии для лечения острого лимфобластного лейкоза у детей и молодых пациентов до 25 лет, более двух месяцев не поддающегося другим видам лечения. Для этого был разработан и протестирован препарат тисагенлеклусел, выходящий под торговой маркой Kymriah. Изначальная заявленная компанией Novartis цена генной терапии с помощью Kymriah составила 475 тысяч долларов (что дешевле, чем пересадка костного мозга), и ее разработчики обещали не брать денег с пациентов, которым она не помогает в течение первого же месяца. В ходе испытаний выздоравливали 83% пациентов. Подробнее об этой терапии можно почитать здесь.
Теперь FDA одобрило новый препарат, который зарегистрирован под торговой маркой Yescarta; его международное название - аксикабтаген цилолейкел (KTE-C19, Axi-cel). Он был разработан и представлен компанией Kite Pharma (незадолго до этого купленной Gilead Sciences за 12 миллиардов долларов). Цена генной терапии в этой компании на данный момент более чем на сто тысяч долларов дешевле по сравнению с их конкурентами, и составляет 373 тысячи долларов — с другой стороны, Gilead Sciences не обещают возврата денег в случае неудачи. По словам экспертов, однако, все эти цифры относительны, и в конечном итоге все этапы подобного лечения пока что могут обойтись пациенту более, чем в миллион долларов.
Действие обоих препаратов основано на технологии CAR-T. В ходе лечения у пациента берут T-лимфоциты и отсылают их для модификации в компанию, предоставляющую соответствующие услуги. При помощи безвредного вирусного вектора в геном этих клеток встраивают кассету, кодирующую химерный антигенный рецептор против специфических белков, представленных на поверхности B-лимфоцитов (в данном случае, против белка CD19). После этого клетки высылают обратно, и в клинике они вновь вводятся в кровь пациента. Там они начинают атаковать собственные B-лимфоциты, уничтожая злокачественные клетки. Здоровые B-клетки при этом тоже гибнут, но это не является критическим побочным эффектом.
Препарат Yescarta, в отличие от Kymriah, предназначен для взрослых пациентов. Терапия направлена против диффузной В-крупноклеточной лимфомы, первичной медиастинальной В-крупноклеточной лимфомы, В-клеточной лимфомы высокой степени злокачественности и диффузной В-крупноклеточной лимфомы, развившейся из фолликулярной лимфомы.
Согласно данным клинических испытаний, 72% пациентов продемонстрировали положительную реакцию на терапию с применением Yescarta, а для 51% удалось добиться полной ремиссии. По словам директора компании, разрешение на применение генной терапии — важнейший шаг в борьбе с рецидивными и рефрактерными лимфомами. Он также полагает, что этот шаг — лишь начало для противораковых технологий CAR-T. Действительно, недавние исследования позволяют надеяться на скорую возможность применения генной терапии не только для борьбы с раком крови, но и для лечения плотных опухолей.
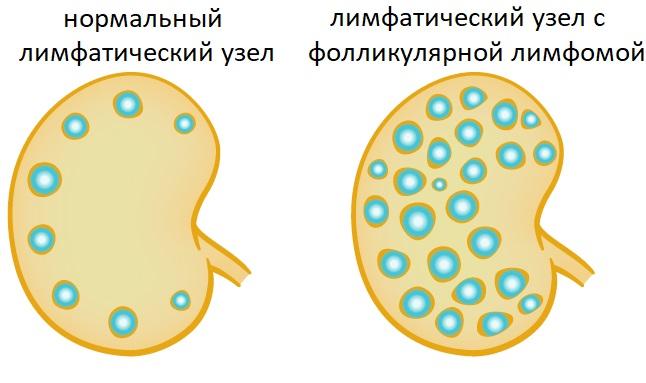
Фолликулярная лимфома — распространенная разновидность неходжкинской лимфомы, представляет собой злокачественную опухоль лимфоидной ткани. Она возникает в результате того, что в организме образуются аномальные , которые накапливаются в лимфатических узлах и других органах.
Этот тип злокачественных опухолей прогрессирует медленно. Некоторым пациентам не требуется лечение, они могут в течение нескольких месяцев или даже лет просто наблюдаться, нужно регулярно посещать врача и сдавать кровь на анализ.
В клинике Медицина 24/7 работают высококвалифицированные врачи, которые имеют большой опыт лечения разных типов лимфом. Наши доктора применяют препараты последних поколений, назначают их в соответствии с современными международными рекомендациями.

Классификация и стадии
Существует несколько классификаций заболевания, и от того, к какому типу оно относится, может зависеть лечение.
В первую очередь, все неходжкинские лимфомы делят на две большие группы:
- С низкой степенью злокачественности — медленно прогрессирующие.
- С высокой степенью злокачественности — быстро прогрессирующие.
Обычно фолликулярные лимфомы относят к первой группе, так как они растут медленно. В свою очередь, они, в зависимости от того, как опухолевые клетки выглядят под микроскопом (оценивают количество центробластов — незрелых форм лейкоцитов), делятся на несколько типов:
- Фолликулярные лимфомы 1, 2 и 3A цитологического типа относят к лимфомам с низкой степенью злокачественности.
- Тип 3B характеризуется высокой степенью злокачественности.
Кроме того, когда опухолевую ткань изучают под микроскопом, оценивают характер её роста:
- фолликулярная лимфома с фолликулярным типом роста;
- лимфома;
- преимущественно диффузный тип роста.
В соответствии с Международной классификацией болезней 10 пересмотра, выделяют следующие типы фолликулярной лимфомы:
- нодальная фолликулярная лимфома (нодулярная);
- мелкоклеточная фолликулярная лимфома с расщепленными ядрами;
- крупноклеточнаяи смешанная мелкоклеточная лимфома с расщепленными ядрами;
- крупноклеточная фолликулярная лимфома;
- фолликулярная неходжкинская лимфома других типов;
- неуточненная фолликулярная неходжкинская лимфома.
Выделяют также классическую форму заболевания у взрослых и педиатрическую форму у детей.
Для определения стадии фолликулярной лимфомы существует классификация Ann Arbor:
- Стадия 1: опухоль в одном лимфоузле или в одном органе, не относящемся к лимфатической системе.
- Стадия 2: опухоль в двух и более лимфатических узлах или в одном органе и его регионарных лимфатических узлах. При этом все очаги находятся только по одну сторону от диафрагмы — выше или ниже.
- Стадия 3: опухолевые очаги находятся по разные стороны диафрагмы.
- Стадия 4: множественные очаги в одном органе, или поражение органа и отдаленных лимфатических узлов, или поражение печени, костного мозга.
К стадии приписывают различные буквы:
- A — если нет симптомов, перечисленных в следующем пункте.
- B — повышение температуры тела более 38 градусов, либо сильная потливость по ночам, либо потеря 10% и более массы тела за последние полгода (эти проявления называют ).
- E — поражение органа, не относящегося к лимфатической системе, при стадиях .
- S — очаги в селезенке при стадиях заболевания.
- X — опухоль больше 10 см в диаметре или значительное увеличение средостения — тканей внутри грудной клетки, которые находятся между легкими.
Современные методы лечения
Примерно один из пяти пациентов с фолликулярной лимфомой не нуждается в лечении и может просто наблюдаться в течение многих лет. Определяя необходимость лечения и выбирая тактику, врач учитывает стадию заболевания, размер и расположение опухолей, симптомы, общее состояние здоровья больного и другие факторы.
Если есть хотя бы один из перечисленных ниже признаков, нужно немедленно начинать лечение фолликулярной лимфомы:
- Поражение более чем трех групп лимфатических узлов, если лимфоузлы имеют диаметр более 3 см.
- Любые опухоли (в лимфатических узлах или других органах), диаметр которых более 7 см.
- : лихорадка, обильная потливость по ночам, потеря более 10% веса за последние 6 месяцев.
- Увеличение селезенки.
- Плеврит — воспаление плевры, тонкой пленки из соединительной ткани, которая выстилает изнутри грудную полость и покрывает легкие.
- Асцит — скопление жидкости в брюшной полости.
- Низкое содержание лейкоцитов (менее 1*109/л) или тромбоцитов (менее 100+109/л) в крови.
- Высокое содержание в крови опухолевых клеток — более 5*109/л.
При фолликулярных лимфомах применяют таргетные препараты и классические химиопрепараты, лучевую терапию, препараты глюкокортикостероидов, проводят пересадку костного мозга.
Действие таргетных препаратов направлено против отдельных , которые необходимы для выживания опухолевых клеток и активируют их быстрое размножение. При фолликулярной лимфоме чаще всего применяют ритуксимаб (Мабтера). Этот препарат связывается с белком на поверхности и активирует иммунные реакции, которые приводят к разрушению опухолевых клеток.
Ритуксимаб выпускается в виде раствора, который вводят внутривенно или под кожу. Обычно его назначают вместе с химиопрепаратами. Если пациент хорошо отвечает на терапию ритуксимабом и химиопрепаратом, поддерживающее лечение можно продолжать до 2 лет.
Химиотерапия обычно применяется в комбинации с ритуксимабом. Такое лечение может привести к ремиссии — состоянию, когда в организме пациента больше не обнаруживается признаков наличия злокачественной опухоли.
Применяют разные виды химиопрепаратов: одни из них вводят внутривенно, другие принимают в виде таблеток. Схема лечения может включать только один химиопрепарат, два или более:
- R-CHOP: ритуксимаб + доксорубицин + циклофосфамид + винкристин + преднизолон.
- R-CVP: ритуксимаб + циклофосфамид + винкристин + преднизолон.
- RB: ритуксимаб + бендамустин.
- R-CEPP: ритуксимаб + циклофосфамид + этопозид + прокарбазин + преднизолон.
Среди всех опухолей лимфатической системы человека, фолликулярная лимфома является заболеванием, которое диагностируется реже всего. Клетки новообразования отличаются наименьшей агрессивностью, что делает данную патологию самой благоприятной в плане прогноза. Несмотря на хорошие результаты терапии, почти всегда лимфома данного вида рецидивирует в течение первых 5 лет.
Нодулярная лимфома, как еще называется это образование, это поражение, затрагивающее лимфатическую ткань и органы, в которых есть фолликулы. Протекает патология довольно медленно. Среди больных фолликулярной лимфомой практически не встречается детей и людей до тридцатилетнего возраста. Чаще заболевание наступает в старческом возрасте. Обычно, это характерно для лиц мужского пола после шестидесяти лет. Так как фолликулярные центры есть не только в лимфоузлах, а и в других органах, таких как селезенка, гортань, миндалины, кишечник и желудок, возникновение и начало прогрессирования опухоли может произойти в любом отделе организма, а симптоматика может быть самой разнообразной.
Причины
Точных причин, способных привести к развитию фолликулярной опухоли, не установлено. Ученым удалось прийти к выводу, что формирование лимфоидного новообразования связано с некоторыми хромосомными аномалиями, но одного этого фактора недостаточно. С высоким риском развития патологии могут столкнуться:
- люди с различными генетическими отклонениями,
- курильщики с многолетним стажем,
- контактирующие с пестицидами и канцерогенами,
- проходящие терапию препаратами, подавляющими иммунитет после трансплантации органов,
- подвергающиеся частому ионизирующему излучению,
- проживающие в местах с плохой экологией,
- люди с аутоиммунными заболеваниями.

В одной третьей части случаев фолликулярной опухоли, болезнь начинается из-за врожденных или приобретенных патологий, связанных с работой иммунной системы.
Классификация
Исходя из строения, лимфома данной разновидности может быть нескольких типов:
- Фолликулярной – семьдесят пять процентов ее клеток – фолликулярные,
- Фолликулярно-диффузной – фолликулярных клеток не более двадцати семи процентов,
- Диффузной – менее двадцати пяти процентов фолликулярных клеток в составе.
Первые две разновидности патологии очень трудно лечатся и почти в ста процентах случаев рецидивируют. От диффузной лимфомы можно полностью избавиться посредством консервативной терапии, однако, такая онкопатология самая агрессивная.

Развитие неходжкинской фолликулярной лимфомы связано с патологическим изменением B-клеток и T-клеток иммунной системы. Изначально поражению подвергается один лимфоузел, после чего патология расходится на остальные лимфатические узлы.
В зависимости от того, какую локализацию имеет лимфома, она может:
- Зарождаться в слизистом слое узла, при этом, не поражая костный мозг,
- Изначально поражать костный мозг.
Если лимфома локализована в тканях лимфоузлов, то она называется нодальной, остальные фолликулярные опухоли являются экстранадальными.
B-клеточная фолликулярная опухоль является самой распространенной среди лимфом. Наиболее часто докторам приходится сталкиваться с диффузной B-крупноклеточной лимфомой.
Помимо нее еще есть:
- мелкоклеточная лимфоцитарная опухоль,
- B-клеточное медиастинальное новообразование,
- лимфома Беркитта,
- волосатоклеточный лейкоз
Данный тип фолликулярных новообразований очень агрессивный и отличается стремительным ростом, однако если вовремя начать терапию, в большинстве случаев удается полностью избавиться от заболевания.
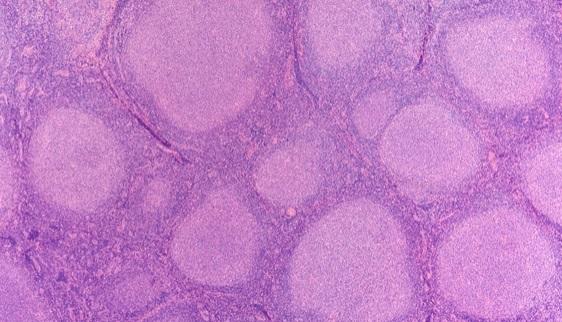
Морфологическое строение лимфом практически одинаково, поэтому доктора разделяют их по гистологическим и цитологическим признакам.
Существует три типа фолликулярных новообразований:
- При первом типе в строении лимфомы имеются разрозненные клетки,
- При втором типе в опухоли отмечается совокупность крупных и мелких клеток,
- Образования третьего цитологического типа имеют в строении фолликулы гигантских размеров.
Во время того как болезнь развивается, тип новообразования может изменяться. Лимфомы, имеющие второй тип, очень агрессивны, они быстро растут и уже в начале клинического течения выдают себя признаками. Терапия при таких лимфомах проводится комплексная, но упор делается на максимальные дозы химических препаратов.
Лимфомы, относящиеся к третьему цитологическому типу, считаются самыми неблагоприятными в сравнении с остальными онкологическими патологиями лимфатической системы. Исследования над группой наблюдения показали, что даже после того как больной пройдет оперативное вмешательство по пересадке костного мозга и полный курс химической терапии, у опухоли есть очень большой риск рецидива. Благодаря некоторым лекарственным препаратам, например, Доксорубицину, можно улучшить прогностические данные, однако это не является стопроцентной защитой от возвращения фолликулярного новообразования.
Стадии
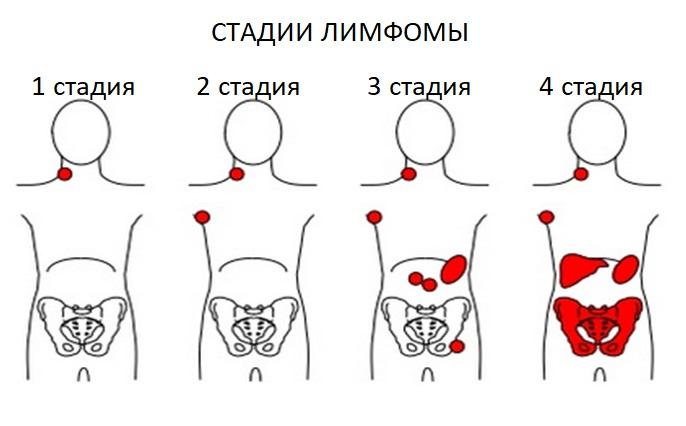
За время своего развития фолликулярное новообразование лимфатической системы проходит четыре стадии:
- На начальной стадии симптоматика лимфомы отсутствует. В крайнем случае, возможно практически незаметное увеличение размеров одного лимфатического узла либо одной группы узлов.
- На второй стадии лимфома поражает сразу несколько групп лимфоузлов, а также ткани и органы, находящиеся за пределами лимфатической системы. Фолликулярная патология локализуется по одной стороне от диафрагмы, а видимые признаки могут как присутствовать, так и отсутствовать.
- Третья стадия характеризуется поражением лимфатических узлов выше и ниже диафрагмы. На данном этапе уже есть внешняя симптоматика болезни.
- Последняя четвертая стадия протекает с поражением центральной нервной системы, любых тканей, органов, костей, а также костного мозга.
Развитие лимфомы, как правило, имеет медленное течение, во время которого чередуются периоды обострений и ремиссий.
Симптомы
На первых двух стадиях заболевания возможно бессимптомное течение. Человек хорошо себя чувствует, его ничего не беспокоит. Часто симптомы фолликулярной лимфомы начинают проявляться на этапе, когда патология уже затронула костный мозг.

Третья стадия болезни протекает со следующими признаками:
- происходит увеличение паховых, подмышечных и шейных лимфатических узлов,
- узлы становятся очень болезненными, особенно, если к ним прикасаться,
- в ночное время суток больной сильно потеет,
- нарастает усталость и быстрая утомляемость,
- возникает гипертермия тела,
- если новообразование поразило селезенку, то она становится увеличенной (спленомегалия),
- при поражении миндалин, человеку становится трудно глотать.
Из-за вовлечения в онкопроцесс кроветворных органов, таких как селезенка и костный мозг, развивается анемия. Поражение нервной системы на четвертой стадии приводит к различным невралгическим нарушениям и соответствующим признакам.
Диагностика
Для того чтобы поставить диагноз, установить тип лимфомы и ее стадию, врач-онколог назначает ряд исследований и анализов. Проведение диагностики начинается со внешнего осмотра больного, пальпации лимфоузлов и сбора анамнеза. Обязательным является проведение пункционной биопсии с последующим гистологическим и цитологическим исследованием.
Также при подозрении на опухоль лимфатической системы необходимо проведение:
- биопсии костного мозга,
- магнитно-резонансной томографии,
- компьютерной томографии,
- ультразвукового исследования.
В обязательном порядке пациентам берется кровь из вены на наличие онкомаркеров, а также на проведение биохимического анализа.
Лечение
При фолликулярной лимфоме терапевтические мероприятия назначаются с учетом стадии онкопатологии. На первых этапах развития лечение фолликулярной опухоли подразумевает проведение химиотерапии и радиолечения. Также проводится лучевая терапия на первично вовлеченные зоны. Для того чтобы восстановить иммунную систему после негативных последствий химических препаратов, больному необходим прием иммуностимуляторов и моноклональных антител. А также пребывание в полностью стерильных условиях. На третьей и четвертой стадии патологии целесообразно проведение одной лишь химиотерапии и то, только в случаях, если это позволяет состояние больного. При вторичном лейкозе во время течения фолликулярного новообразования, проводится трансплантация костного мозга. Идеальным донором для такой процедуры может стать ближайший кровный родственник.
Осложнения и рецидивы
К осложнениям, которые могут быть вызваны лимфомой, относятся:
- язвы слизистых оболочек внутренних органов,
- утомляемость даже при незначительных физических нагрузках,
- выпадение волос,
- плохая свертываемость крови и повышенная склонность к кровотечениям,
- недостаточность иммунитета и восприимчивость к различным инфекциям,
- понижение аппетита и потеря массы тела.
Во время лечения химической терапией возможен распад новообразований, что приводит к поражению почек, сердечно-сосудистой, а также центральной нервной систем. Самым частым осложнением при фолликулярном новообразовании является рецидив, который наступает в ранние сроки после проведения терапии.
Прогноз и профилактика
При лимфоме выживаемость без последствий возможна только в том случае, если патология была диагностирована на первой стадии. Тогда у докторов есть достаточно времени для разработки индивидуальной схемы лечения. На начальном этапе фолликулярной опухоли положительного прогноза можно добиться в девяти случаях из десяти. Вторая стадия болезни сокращает процент пятилетней выживаемости на десять. При обнаружении онкопатологии на третьей стадии развития выживает только половина больных.

Четвертая стадия болезни практически не встречается, так как уже на третьей возникают симптомы, с которыми человек обращается к доктору и начинает терапию. Но если же лимфома по каким-то причинам была диагностирована на завершающем этапе развития, то шансы на излечение крайне малы. При лимфоме 4 стадии прогноз на пятилетнюю выживаемость могут рассчитывать только десять процентов больных. Все лечебные мероприятия могут лишь немного продлить жизнь пациенту, и то не всегда. Как правило, летальный исход при лимфоме наступает от осложнений, которые ослабленный организм не может побороть.
Полностью уберечься от заболевания невозможно. Но можно сократить риск его возникновения, если придерживаться здорового образа жизни, правильно питаться, отказаться от вредных привычек, укреплять иммунную систему. Плановый осмотр доктором один раз в год является не последним моментом в плане профилактики онкопатологий.
Фолликулярная лимфома
Фолликулярная лимфома (ФЛ) или лимфома фолликулярных центров является второй по частоте подгруппой В-клеточных неходжинских лимфом (НХЛ) (15-30% от всех НХЛ).
В настоящее время наблюдается повышение заболеваемости ФЛ во многих странах.
Течение заболевания характеризуется длительной общей выживаемостью при одновременном наличии системных рецидивов.
Мужчины и женщины заболевают с одинаковой частотой при среднем возрасте больных в момент установления диагноза 50-60 лет. Клинически фолликулярная лимфома имеет вялотекущий характер в большинстве случаев; симптоматика в целом скудная и зависит от топики лимфоаденопатии.
Заболевание наиболее часто начинается с увеличения периферических лимфоузлов или селезенки, лимфоузлы средостения увеличиваются редко. Увеличение парааортальных лимфоузлов вызывает ощущение дискомфорта в брюшной полости или появление других локальных симптомов. Экстранодальная локализация наблюдается у 10% пациентов, в основном в желудочно-кишечном тракте; редко поражается кожа. Менее чем у 20% больных выявляется интоксикационный синдром.
Костный мозг вовлекается в процесс примерно в 50% случаев с картиной типичной нодулярной инфильтрации. У 10% больных отмечается лимфоцитоз и циркуляция опухолевых клеток в периферической крови.
Гистологически при ФЛ структура лимфоузла напоминает нормальные зародышевые центры. Центроциты и центробласты формируют неопластические терминальные центры. Характер роста обычно фолликулярный, но в редких случаях носит диффузный характер. Цитогенетически у 90% пациентов с фолликулярной лимфомой определяется t (14; 18) (q32; q21).
Эта транслокация ведет к гиперэкспрессии протеина BCL-2. Однако общая выживаемость больных коррелирует не с гиперэкспрессией генов в клетках опухоли, а с гиперэкспрессией генов в инфильтрирующих опухоль иммунных лимфоцитах. В 85% случаев при ФЛ встречается t (16; 20) (q32; q21). Клетки ФЛ (суспензия клеток опухоли или гистологические препараты) имеют фенотип CD19+, CD20+, CD10+, CD3-, CD5-.
Стадия фолликулярной лимфомы устанавливается с учетом количества пораженных лимфатических зон и с учетом количества бластов:
стадия I - количество бластов менее 5%,
стадия II - количество бластов 5-15%,
стадия III - количество бластов более 15%.
Более поздние стадии расцениваются как IIIа стадия (сочетание центроцитов и бластов) или IIIб (диффузное преобладание бластов). Клинически стадии протекают более медленно с рецидивами, в то время как стадии III и IIIа имеют более агрессивное течение и поэтому при них терапия должна проводиться по протоколам лечения диффузной В-крупноклеточной лимфомы (ДВККЛ).
Факторами риска (ФНП) при ФЛ являются: мужской пол, пожилой возраст, большая масса опухоли, интоксикационный синдром, инфильтрация костного мозга, повышение лактатдегидрогеназы (ЛДГ) выше 700 Ед/л или повышение уровня р2-микроглобулина.
Согласно рекомендациям FLIPI (Follicular lymphoma international prognostic index) выделяют три прогностические группы в соответствии с наличием ФНП: группа благоприятного прогноза (0-1 ФНП), промежуточная (2 ФНП), неблагоприятного прогноза (более 3 ФНП).
Несмотря на отнесение больных к группе благоприятного прогноза в момент установления диагноза, в 40% случаев ФЛ в финале трансформируется в диффузную крупноклеточную иммунобластную лимфому, требующую проведения терапии по соответствующим протоколам. При этом часто выявляется del (6); возникновение мелкоклеточной лимфомы ассоциируется с t (8; 14)(q24; q23)
Наблюдение показано у пациентов с отсутствием симптоматики в III-IV стадиях, которые не имеют интоксикационного синдрома или других осложнений, обусловленных лимфомой. Пациенты должны регулярно проходить обследование для уточнения активности процесса. Полихимиотерапия (ПХТ) начинается при признаках прогрессирования заболевания: нарастание интоксикации, увеличение лимфоузлов, поражение костного мозга.
Лучевая терапия показана в стадиях при отсутствии bulk disease: облучение вовлеченных в процесс зон в суммарной очаговой дозе (СОД) 40 Гр. Хотя такая терапия вызывает длительные ремиссии, рецидив неизбежен. Комбинированная терапия в начальных стадиях (ПХТ+лучевая терапия) вызывает более длительные ремиссии у пациентов с ФЛ, но общая выживаемость сравнима с таковой при проведении только лучевой терапии. Поэтому проведение комбинированной терапии не рекомендуется в ранних стадиях ФЛ.
ПХТ показана при появлении симптомов прогрессирования после периода наблюдения. Монохимиотерапия алкилирующими препаратами приемлема для пациентов с наличием противопоказаний для более агрессивной полихимиотерапии.
Применяются различные протоколы ПХТ: CHOP, R-CHOP, FCM, R-FCM или более интенсивные схемы ПХТ при наличии ранних рецидивов. Включение в схемы полихимиотерапии ритуксимаба (aнти-CD20-антител) приводит к уничтожению клеток лимфомы вследствие комплемент- и антитело-обусловленной клеточной цитотоксичности.
В комбинации ритуксимаба и ПХТ результаты сравнимы с эффектом от проведения миелоаблативной консолидации. Поддерживающая терапия rINF удлиняет безрецидивную выживаемость, но вызывает побочные эффекты. Новым направлением терапии является применение ингибиторов протеосом, блокаторов BCL-2 и адоптивной иммунотерапии.
Пациенты молодого возраста с наличием ФНП при наличии синдрома интоксикации или больших опухолевых масс являются кандидатами на проведение миелоаблативной химиоконсолидации с последующей ауто- трансплантации гемопоэтических стволовых клеток (ТГСК). Алло-ТГСК с проведением миелоаблации или редуцированного кондиционирования является единственным методом излечения при генерализованных стадиях фолликулярной лимфомы и рекомендуется при рецидивах заболевания.
Лимфомы маргинальной зоны
Лимфомы маргинальной зоны представлены:
Моноцитоидный тип лимфомы маргинальной зоны встречается преимущественно у лиц пожилого и старческого возраста, часто выявляется в I-II стадиях и не имеет тенденции к ранней диссеминации. Первыми проявлениями болезни могут быть поражение лимфоузлов или наличие локальных экстранодальных очагов опухоли.
Часто поражаются селезенка, печень, молочная железа, слюнные железы. Риск развития моноцитоидной НХЛ повышается у пациентов с аутоиммунными заболеваниями типа синдрома Сьегрена и тиреоидита Хашимото (не исключается, что данные заболевания могут быть ранними проявлениями моноцитоидной неходжинской лимфомы).
Иммунофенотип, формирование опухолевой ткани в лимфоидном органе и ее морфологические особенности позволяют считать, что эта опухоль формируется из В-клеток маргинальной зоны фолликула. Опухолевые клетки экспрессируют антигены CD5, CD10, CD11c, PCA-1. В лечении применяется спленэктомия; ПХТ по протоколам FC или FCR вызывает длительные ремиссии.
MALT-лимфомы
Согласно классификации ВОЗ, лимфомы, происходящие из мукозоассоциированной лимфоидной ткани, относятся к экстранодальным лимфомам маргинальной зоны MALT-типа и составляют 8% от всех НХЛ. Для них характерно развитие первичного очага в эпителиальной ткани (желудок, легкие, слюнные, щитовидная и паращитовидные железы, реже - тонкий кишечник), лимфоэпителиальная деструкция и вялое клиническое течение.
В эпителиоидных тканях в норме лимфоидные клетки отсутствуют и появляются там обычно при хронической инфекции. Установлена причинная связь (90%) MALT-лимфомы желудка с инфицированием Helicobacter pylori (HP). Эрадикация HP может привести к ремиссии MALT-лимфомы.
Средний возраст пациентов с MALT-лимфомой желудка около 60 лет с одинаковой частотой заболеваемости у мужчин и женщин. Наиболее частыми симптомами являются диспепсии и эпигастральный дискомфорт, очень редко - классический интоксикационный синдром. При ФГДС на слизистой желудка находят реактивные В-клеточные фолликулы с центроцитоидоподобными лимфоидными клетками мелких и средних размеров.
Наиболее часто опухоль локализуется в антральном отделе, мультифокальное поражение определяется в 35% случаев. В момент установления диагноза MALT-лимфома диссеминирована у 30% больных: выявляется поражение костного мозга, множественное поражение лимфоузлов, экстранодальные очаги; повышен уровень в2-микроглобулина. Типичные клетки лимфомы имеют фенотип CD20+, CD21+, IgM+, CD5-, CD10-, IgD-, циклин D-.
С MALT-лимфомой специфически ассоциированы транслокации: t (11; 18) (q21; q21), t (1; 14) (p22; q32) и t (14; 18) (q32; q21). В результате t (11; 18) образуется химерный сливной ген, который специфически связан с MALT-лимфомами, не отвечающими на эрадикацию HP; при этой транслокации значительно реже бывает трансформация в ДВККЛ. t (1; 14) и t (14; 18) соответственно, дерегулируют экспрессию BCL10 и MALT1.
Стадия I: опухоль локализована в желудочно-кишечном тракте (ЖКТ)
Стадия II: опухоль в ЖКТ выходит за пределы первичной локализации: вовлечение перигастральных или перимезентериальных лимфоузлов:
- II2: вовлечение парааортальных или паракавальных лимфоузлов
- II3: пенетрация серозных оболочек с вовлечением прилегающих органов или тканей
Стадия III при MALT-лимфомах не выделяется
Стадия IV: диссеминация процесса или вовлечение супрадиафрагмальных лимфоузлов
Вариант терапии MALT-лимфомы зависит от наличия HP, стадии заболевания, наличия t (11; 18) и признаков трансформации в ДВККЛ.
Эрадикация HP проводится во всех случаях комбинацией трех препаратов в течение 10-14 дней:
- омепразол 20 мг 2 раза в день,
- кларитромицин 500 мг 2 раза в день,
- амоксициллин 1,0 гр. 2 раза в день; при непереносимости препарата назначают метронидазол 500 мг 2 раза в день.
Пациентам в стадии генерализации проводит терапию как и при других вариантах вялотекущих лимфом: полихимиотерапия с включением ритуксимаба (протоколы R-CHOP, R-FCM). С учетом активации NF-kB протеина можно проводить таргентную терапию с применением ингибиторов протеосом.
Лимфомы зоны мантии
Клиническими проявлениями являются: генерализованная лимфоаденопатия, гепатоспленомегалия; у 60% больных имеет место поражение костного мозга, около 30% пациентов имеют интоксикационный синдром. У некоторых пациентов лейкемическая диссеминация может быть найдена в момент установления диагноза.
В 10% случаев поражается желудочно-кишечный тракт по типу множественного полипоза. В начальной стадии опухоль имеет нодулярный характер роста, который при прогрессировании процесса сменяется диффузным. При гистологическом исследовании выявляется мономорфная пролиферация лимфоидных клеток малой и средней величины в сочетании с фолликулярными дендритическими клетками.
Опухолевые клетки имеют фенотип CD19+, CD20+, CD5+, CD22+, CD24+, CD10-HLA-DR, циклин D1+ в сочетании с экспрессией IgM. Лимфомы зоны мантии имеют специфический маркер t (11; 14) (q13; q32); при этой транслокации происходит реаранжировка гена BCL-1 c последующей экспрессией циклина D1.
ЛЗМ имеют неблагоприятный прогноз в связи с относительной резистентностью клеток опухоли к химиопрепаратам. Терапия по протоколам R-CHOP и Hyper-CVAD в 90% случаев позволяет достичь ремиссии, но ее длительность невелика. Применение меченых антител (миелоаблативная радиохимиотерапия) повышает общую выживаемость у пациентов моложе 65 лет.
В редких случаях при локализованных стадиях с малой величиной лимфоузлов лучевая терапия может вызывать длительные ремиссии. Алло-ТГСК может быть рекомендована при рецидиве заболевания.
В последнее время большое внимание уделяется применению ингибиторов протеосом в терапии НХЛ при резистентности к проводимой ПХТ. Протеосомы являются ферментным комплексом, необходимым для деградации протеинов, вовлеченных в процесс роста и выживания клеток, в частности, вовлеченных в процесс контроля клеточного цикла.
Они модулируют уровень циклина, циклинзависимых киназ и их ингибиторов р21, р23, р53; играют центральную роль в транскрипции, контролируя уровень NF-kB. Аномальная активация NF-kB при гиперэкспрессии обратных киназ может привести к прогрессированию лимфом, а также к резистентности опухолевых клеток к ПХТ и радиационному воздействию.
В частности, подтип В-активированной ДВККЛ характеризуются накоплением NF-kB белка в ядрах клеток. Обычно регулируемые NF-kB протеины блокируют апоптоз, воздействуя на гены семейства BCL-2 и на гены семейства ингибиторов апоптоза. NF-kB влияет на процесс пролиферации, вовлекая такие таргентные гены, как циклин-D2 и c-myc, а также индуцирует продукцию IL-6 и IL-10 при неходжинских лимфомах.
Ингибирование протеосом вызывает антинеопластический эффект, воздействуя на различные регуляторные механизмы, включая апоптоз, подавляет клеточный рост и снижает экспрессию генов, участвующих в процессе клеточной адгезии, миграции и ангиогенеза.
Высокоактивным ингибитором протеосом, связывающим активные центры фермента, является бортезамид (велкейд). Его антилимфомный эффект при ЛЗМ обусловлен различными механизмами, включая подавление прогрессии клеточного цикла, индукцию апоптоза и подавление ангиогенеза. Он ингибирует экспрессию NF-kB и циклина-DL.
При применении бортезамида получены хорошие результаты в терапии лимфом зоны мантии и ДВККЛ (подтип из активированных В-лимфоцитов). Возможна комбинация бортезамида в комбинации с полихимиотерапией ингибиторами гистондеацетилазы (HDAC) и активаторами апоптоза. Изучается эффект применения в терапии ЛЗМ более мощного ингибитора протеосом - карфилзомида.
Новое направление в терапии лимфом зоны мантии - применение ингибиторов HDAC, которые восстанавливают экспрессию генов тумор-супрессоров и/или генов-регуляторов клеточного цикла в клетках НХЛ и блокируют пролиферацию этих клеток. Терапия ЛЗМ препаратом этой группы - субероиланилидингидроксаликовой кислотой - SAHA (вориностат) вызывает остановку митоза в G1 или G2 фазе, а также дерегулирует циклин-D1 hD2, активируя р53, р21, р27.
Дериваты рапамицина - темзиралим и эверолим - вызывают остановку клеточного цикла путем снижения уровня циклина D1. Возможно их применение в виде монохимиотерапии или в сочетании с ритуксимабом и другими препаратами при прогрессировании или рецидиве лимфом зоны мантии.
Еще одним направлением в терапии ЛЗМ является применение иммуномодуляторов - талидамида и леналидамида. Они оказывают прямое цитотоксическое действие на некоторые типы клеток, модулируют иммунитет посредством изменения продукции цитокинов и клеточных изменений опухолевых клеток, реактивных Т- и NK-клеток, вызывая индукцию апоптоза путем обратной регуляции сосудистого эндотелиального фактора роста (VEGF).
Леналидамид как иммуномодулятор и ингибитор протеосом, является высокоэффективным препаратом в лечении лимфомы из малых лимфоцитов, ЛЗМ, ФЛ, множественной миеломы, периферической Т-клеточной лимфомы и ДВККЛ.
В качестве терапии второй линии или при рефрактерности к проводимой ПХТ при НХЛ высокой степени злокачественности рекомендуются следующие протоколы:
винкристин 1,4 мг/м2 в/венно в 1-й день,
преднизолон 60 мг/м2 внутрь 1-5 дни,
этопозид 100 мг/м2 в/венно 1-3 дни,
новантрон 10 мг/м2 в/венно в 1-й день.
Протокол применяется при НХЛ низкой степени злокачественности с интервалом в 28 дней.
блеомицин 10 мг/м2 в/венно 1,5 дни,
адрибластин 50 мг/м2 в/венно в 1-й день,
циклофосфан 750 мг/м2 в/венно в 1-й день,
винкристин 1,4 мг/м2 в/венно в 1-й день,
преднизолон 60 мг/м2 внутрь 1-5 дни.
Протокол применяется при неходжинских лимфомах высокой степени злокачественности с интервалом 21 день.
Pro-MACE-Cyta-BOM:
циклофосфан 650 мг/м2 в/венно в 1-й день,
адрибластин 25 мг/м2 в/венно в 1-й день,
этопозид 120 мг/м2 в/венно в 1-й день,
преднизолон 60 мг/м2 внутрь 1-15 дни,
цитарабин 300 мг/м2 в/венно в 8-й день,
блеомицин 5 мг/м2 в/венно в 8-й день,
винкристин 1,4 мг/м2 в/венно в 8-й день,
метотрексат 120 мг/м2 в/венно в 8-й день,
лейковорин 100 мг внутрь 9-10 дни.
Протокол применяется при НХЛ высокой степени злокачественности с интервалом 21 день.
MIME:
метилгаг 500 мг/м2 в/венно 1,14 дни,
ифосфамид 1000 мг/м2 в/венно 1-5 дни,
метотрексат 30 мг/м2 в/мышечно в 3-й день,
этопозид 100 мг/м2 в/венно 1-3 дни.
Интервал между курсами - 21 день.
цитарабин 300 мг/м2 в/венно 1, 8, 15 дни,
блеомицин 6 мг/м2 в/венно 1, 8, 15 дни,
этопозид 120 мг/м2 в/венно 1-3 дни,
прокарбазин 100 мг/м2 внутрь 10-21 дни.
Интервал между курсами - 35 дней.
пентостатин 2-1 мг/м2 в/венно в 1-й день,
циклофосфан 600 мг/м2 в/венно в 1-й день,
ритуксимаб 375 мг/м2 в/венно в 1-й день.
Интервал между курсами - 21 день.
Применяется для лечения рефрактерных форм хронического лимфолейкоза (ХЛЛ).
Курсы 1, 3, 5, 7:
циклофосфан 300 мг/м2 в/венно 2 раза в сутки - 1-3 дни,
месна 6500 мг в/венно инфузоматом в течение 72 часов,
винкристин 2 мг/м2 в/венно 4, 11 день,
адриамицин 50 мг/м2 в/венно 4-й день,
дексаметазон 40 мг внутрь 1-4, 11-14 дни.
Курсы 2, 4, 6, 8:
метотрексат 1000 мг/м2 в/венно инфузоматом в течение 24 часов - в 1-й день,
цитарабин 3000 мг/м2 в/венно 2 раза в сутки - 2, 3 день,
лейковорин 15 мг/м2 в/венно через 12, 18, 24 часа после завершения инфузии,
метотрексата.
В отсутствие цитопении курсы 2, 4, 6, 8 начинаются сразу после окончания курсов 1, 3, 5, 7; если есть цитопения, то введение гранулоцитарного колониестимулирующего фактора (Г-КСФ) в дозе 10 мкг/кг подкожно начинают с первого дня перерыва после 1, 3, 5, 7 курсов; Г-КСФ вводится до выхода из агранулоцитоза.
Введение месны начинают одновременно с инфузией циклофосфана и завершают через 72 часа. Одним из осложнений лечения неходжинских лимфом является развитие вторых злокачественных новообразований - примерно в 12% случаев.
Риск развития острого миелоидного лейкоза (ОМЛ) наиболее высок при ПХТ с включением алкилирующих агентов, препаратов нитрозомочевины и высокодозной ПХТ. Заболеваемость ОМЛ достигает максимума через 5-7 лет, чаще как исход миелодиспластического синдрома (МДС) и не поддается лечению. Частота солидных опухолей - рак молочной железы, легких - начинает нарастать через 5-7 лет наблюдения и достигает максимума через 20 лет после проведения лучевой терапии.
Контрольные осмотры при НХЛ проводятся каждые три месяца на протяжении первых 2-х лет, каждые 6 месяцев в течение последующих трех лет, затем - один раз в год. Развернутый анализ периферической крови и определение уровня ЛДГ проводятся на 3, 6, 12, 24 месяцах наблюдения, а затем при появлении подозрительных симптомов.
Оценку функции щитовидной железы проводят больным, получавшим лучевую терапию на область шеи на 1, 2, 5 годах наблюдения. Компьютерную томографию исходных очагов поражения проводят на 6, 12, 24 месяцах после окончания лечения.
После проведения лучевой терапии на область грудной клетки в пременопаузальном возрасте, а также в возрасте до 25 лет женщин следует подвергать скринингу для исключения индуцированного рака молочной железы, сначала по клиническим данным, а после 40-50 лет - с помощью маммографии.
Читайте также:





