Американцы о раке простаты
РАК ПРОСТАТЫ – ЛЕЧЕНИЕ В США
Лечение в США - EuroDoctor.ru
Предстательная железа – это орган мужской половой сферы, который располагается под мочевым пузырем. Он производит часть семенной жидкости.
Рак простаты (предстательной железы) — злокачественное новообразование, возникающее из эпителия альвеолярно-клеточных желез.
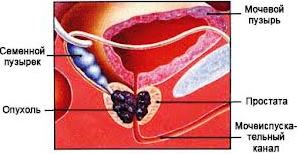
Большинство раковых опухолей простаты растут медленно.
Несмотря на то, что этот вид рака не отличается быстрым ростом и ранним метастазированием, несвоевременная его диагностика может привести к распространению заболевания (как правило с метастазами в костях), что значительно усложняет лечение и ухудшает прогноз полного выздоровления.
Опухоль предстательной железы может развиваться по разным причинам. Во-первых, играет роль фактор наследственности и возраста (чаще это заболевание встречается у пожилых мужчин), неправильно питание (потребление жирной пищи), низкая сексуальная активности и аденома простаты.
СИМПТОМЫ РАКА ПРОСТАТЫ
Ранние клинические признаки заболевания идентичны доброкачественной гиперплазии предстательной железы (аденоме), что может значительно усложнить своевременную диагностику.
Основными симптомами рака простаты являются:
Прогрессирующее нарушение мочеиспускания - ослабление струи, частые позывы на мочеиспускание, чувство неполного опорожнения
Кровотечение при мочеиспускании
Наличие крови в семенной жидкости (сперме)
Острая задержка мочеиспускания – невозможность выделения мочи, требующая экстренной катетеризации мочевого пузыря с целью предотвращения тяжелых осложнений
Недержание мочи и парадоксальное мочеиспускание – непроизвольное выделение небольших порций мочи в следствие хронической задержки и избыточном наполнении мочевого пузыря
Осложнения со стороны мочевыводящих путей и почек, связанные с хроническими уродинамическими нарушениями – рецидивирующие инфекции и почечная недостаточность
Признаки прогрессирования заболевания – боли в области промежности и таза (при прорастании опухоли в соседние ткани), боли в костях, спине, патологические переломы и опасное повышение уровня кальция в крови (при метастазах в кости), а также признаки метастатических поражений других органов.
Появление первых симптомов заболевания требует немедленной дифференциальной диагностики в центрах, специализирующихся на лечении рака простаты.
ДИАГНОСТИКА РАКА ПРОСТАТЫ
Среди основных методов современной диагностики рака предстательной железы, нужно отметить:
Анализ крови на уровень специфического антигена предстательной железы (PSA) – является основным методом ранней диагностики заболевания, а также важным параметром для контроля эффективности лечения
Ректальное исследование специалистом-проктологом позволит обнаружить увеличенную предстательную железу, а оценка ее консистенции помогает заподозрить злокачественный процесс
Трансректальное ультразвуковое исследование, а также УЗИ органов таза позволит судить о размерах опухоли и вовлечении в процесс соседних органов
Биопсия предстательной железы с последующим гистологическим исследованием образцов поможет установить точный диагноз и определить гормональную зависимость опухоли, что поможет в правильном выборе лечения.
Оценка распространения рака осуществляется при помощи КТ, ПЭТ-КТ, МРТ и изотопного сканирования костей
ЛЕЧЕНИЕ РАКА ПРОСТАТЫ
Радикальное удаление предстательной железы позволяет полностью удалить опухоль, а также региональные лимфатические узлы, предупредив развитие рецидива заболевания. Существует несколько современных методик проведения этой операции.
Специалисты в клиниках США отдают предпочтение лапароскопическим вмешательствам (лапароскопическая простатэктомия), а также роботизированным операциям на предстательной железе, что значительно повышает эффективность процедуры и уменьшает вероятность осложнений
В США при лечении рака предстательной железы чаще всего используется система Да Винчи. По многим причинам, именно эта роботизированная система является номером 1 в области лечения рака простаты. Она значительно упрощает лечение и последующую реабилитацию пациента.
Операции при раке простаты с сохранением нервных окончаний. При применении этой инновационной методики полностью сохраняется иннервация органов малого таза, предотвращая развитие неврологических нарушений, в том числе проблем с эрекцией у пациентов после удаления опухоли
Малоинвазивные процедуры, разрушающие клетки опухоли и препятствующие росту и распространению рака – ультразвуковая и крио- абляции. Эти эффективные методы показаны при наличии противопоказаний к радикальному удалению простаты
Лучевая терапия применяется как основной или дополнительный метод лечения. Наряду с бесконтактными методами облучения области малого таза, при раке предстательной железы с успехом применяется брахитерапия – введение радиоактивного материала непосредственно в ткани опухоли с целью ее разрушения при минимальных побочных эффектах
Химиотерапия применяется при распространенной форме рака самостоятельно или в комбинации с другими методами лечения
Гормональная терапия эффективна при некоторых формах заболевания и позволяет остановить рост опухоли даже при наличии отдаленных метастазов. Этот вид лечения назначается при метастазировавшем раке простаты. Гормональная терапия позволяет контролировать рост и распространение раковой опухоли и применяется в сочетании с другими методами противоопухолевого лечения на поздних стадиях рака простаты.
Симптоматическое лечение рака предстательной железы направлено на уменьшение болевого синдрома и снижение уровня кальция в крови, критически повышающегося при распаде костной ткани
В онкологических центрах США собраны специалисты всех направлений по борьбе с онкологией: радиологи-онкологи, терапевты-онкологи, хирурги всех специализаций, рентгенологи, интервенционные радиологи, и т.п.. Вся система помощи сфокусирована на том, чтобы предоставить каждому пациенту максимально эффективное лечение.
Лечение в клиниках США – это качественная медицинская помощь, самое современное оборудование, высококвалифицированный персонал, комфортное обустройство палат (что очень важно, если необходима восстановительная реабилитация).
+7 (925) 66-44-315 - бесплатная консультация по лечению в Москве и за рубежом

Новость о том, что у госсекретаря США Колина Пауэла был обнаружен рак простаты, не вызвала бурных обсуждений в американском обществе. Для обследования и лечения высокопоставленного чиновника не созывался консилиум из лучших мировых специалистов, и ни у кого не возникли мысли об отставке Пауэлла. Как считает известный онкоуролог, заведующий кафедрой урологии Московского государственного медико-стоматологического университета профессор Дмитрий Юрьевич Пушкарь, все дело в отношении американцев и европейцев к раку, которое значительно отличается от российского.
В России рак простаты — нередкое заболевание. Он встречается у каждого шестого мужчины в возрасте старше 60 лет, причем занимает второе место по уровню смертности среди всех злокачественных опухолей. В нашей стране за последнее время выросло как количество заболевших, так и число умерших от этой опухоли.
Высока заболеваемость раком и на Западе, однако там к этой болезни по-другому относятся. По словам профессора Пушкаря, в Америке известные широкой публике персоны, не скрывают своих болезней. Так, операцию по поводу рака простаты в свое время перенесли знаменитый актер Роберт Де Ниро, соперник Клинтона на выборах 1996 года сенатор-республиканец Боб Доул и мэр Нью-Йорка Рудольф Джулиани. Это происходит потому, что американцы рака не боятся — они научились с ним справляться. Не боятся его и европейцы — подобную операцию, например, в свое время перенес бывший президент Франции Франсуа Миттеран, причем было это в восьмидесятых годах, после чего он долго еще оставался активным политиком.
А вот в России говорить о подобных болезнях не принято. И дело даже не в официальной цензуре, которая обычно накладывается на сообщения о состоянии здоровья руководителей страны. Дело в другом — у нас вплоть до недавнего времени онкологическим больным, даже самым высокопоставленным, не принято было сообщать, что у них рак, потому что такой диагноз фактически приравнивался к смертному приговору.
Более того, в России и ранняя диагностика рака предстательной железы, в отличие от США, остается на низком уровне. Почти каждый пожилой американец знает свой ПСА — уровень простат-специфического антигена, который на сегодняшний день является самым специфичным онкомаркером для этой разновидности раковых заболеваний. Российские мужчины соответствующего возраста о таком, как правило, и не слышали, причем о правильных методах анализа мало что знают даже врачи, и зачастую анализ на ПСА не включается ни в перечень услуг страховой медицины, ни в скрининг-исследования. Лишь недавно в Москве на базе городской клинической больницы ? 50, в клинике урологии МГМСУ, где работает профессор Пушкарь, заработал первый бесплатный кабинет ранней диагностики заболеваний предстательной железы, куда может обратиться каждый житель столицы. Но только в столице, по оценке профессора, таких кабинетов должно быть как минимум два-три. Что же говорить о России в целом.
Есть еще одно специфическое отличие между подходом к раковым больным в США и в России. Средняя продолжительность жизни у мужчин в Америке в 2002 году составляла 77,2 года, во многих европейских странах этот показатель еще выше, а наш соотечественник в среднем доживает до 55 с половиной лет. Поэтому к нашим пациентам, приблизившимся к пороговому возрасту в 55-60 лет, когда возрастает риск заболевания раком предстательной железы, зачастую относятся как к старикам, к которым поздно уже принимать профилактические меры. Не удивительно, что в России рак диагностируют, как правило, в стадии клинических проявлений, когда лечение становится малоэффективным.
Впрочем, отчаиваться россиянам все же не следует, потому что и в нашей стране ситуация пусть медленно, но меняется в лучшую сторону. Та же клиника урологии МГМСУ, рассчитанная на 200 коек, добивается мирового уровня диагностического и операционного обслуживания пациентов. Помимо создания кабинета ранней диагностики, коллеги профессора Пушкаря исповедуют самый современный подход к лечению заболеваний предстательной железы у мужчин. Во-первых, здесь не принято скрывать от больных их диагноз — напротив, считается, что пациент должен знать о своем состоянии, чтобы мобилизовать свои силы и тем самым помочь врачу. Во-вторых, к 50-60-летним больным здесь относятся как к молодым людям, у которых еще все впереди, и после проведения радикальной простатэктомии продолжают следить за ними еще в течение, как минимум, пяти лет (создан даже специальный клуб людей, перенесших эту операцию). В-третьих, благодаря помощи Департамента здравоохранения Москвы, личным связям за рубежом и энергии работающих здесь врачей операционные блоки клиники снабжены самым современным оборудованием, позволяющим лечить больных с наименьшими травматическими последствиями.
Результаты говорят сами за себя: радикальную простатэктомию в клинике урологии МГМСУ выполняют с 1993 года, за это время здесь прооперированы тысячи больных. Ни один из них не умер на операционном столе, количество полностью излечившихся в результате операции приближается к 85 процентам, при этом в 60 процентах случаев у больных сохраняется сексуальная функция, 95 процентов пациентов после операции не страдают недержанием мочи. Помимо собствено рака простаты, хирурги из клиники урологии МГМСУ (а всего здесь работает 70 человек) специализируются по целому ряду других заболеваний: недержанию мочи у женщин и у мужчин, раку почки и раку мочевого пузыря.
По словам профессора Пушкаря, подобный положительный опыт накоплен и в ряде других российских клиник, хотя у каждой из них своя специфика и свои области специализации. Всем им, как обычно, не хватает финансирования, оборудования и медикаментов, но они работают, лечат больных и ждут, когда Министерство здравоохранения примет меры, чтобы переломить ситуацию в целом: повсеместно ввести раннюю диагностику раковых заболеваний и перестать смотреть на шестидесятилетних мужчин, как на отработанный материал. В конце концов, у людей, перенесших радикальную простатэктомию, действительно, все еще впереди — как и у Колина Пауэлла, который, излечившись от рака, вполне может остаться в большой политике и когда-нибудь даже стать президентом Соединенных Штатов, если, конечно, супруга будет не против.
Одним из наиболее спорных вопросов считается различие расовых групп населения мира как фактора риска для развития рака простаты. Этот сложный аспект иногда приобретает окраску политической подоплеки. Вместе с тем, имеются неопровержимые свидетельства неодинаковой частоты встречаемости заболевания в разных этнических группах. Каждая раса подвержена в неодинаковой степени риску клинического диагноза рака простаты. Существенные различия в показателях риска этого заболевания связаны также с местом обитания, например, в Японии (Y. Yohi Chang, 1999; Nakasj, 2000).
Явные отличия способствовали выяснению молекулярных, генетических и диетических особенностей многих расовых групп с целью определения потенциальных причин характерных уровней риска для рака простаты (С. McDonald, 1999). Заметная разница в частоте рака простаты отмечена R.M.Merrill et al. (1997), показавших, что появление его у чернокожих мужчин соответствует 234 % таковой у мужчин всех других рас, рассматриваемых вместе.
Хотя по-прежнему нет объяснения различиям частоты рака простаты у белых и черных пациентов, высокая смертность среди последних от этого заболевания зависит от поздней диагностики. G.Dhom (1999) приводят сведения о 5-летней выживаемости у 57% белых и только 46,2% — среди черных. Соответственно, частота обнаруживаемого рака у черных ниже, чем у белых. Однако это только одна сторона вопроса.
Эпидемиология
Эпидемиологические исследования показывают большую разницу показателей частоты рака в разных регионах мира. К примеру, она у белых американцев приблизительно в 10 раз выше, чем у их ровесников в Японии. Отчетливо видны различия между севером и югом Европейского континента, так, частота выявляемости рака простаты в Швеции достигает 50,2 случая на 100 тысяч мужчин, в Португалии — 11,8. Что это означает? Вероятнее всего, на первый план выходят окружающая среда и питание, обусловившие эти отличия.
Испанцы, коренные американцы, жители Азии имеют самый низкий риск развития рака простаты. По сравнению с чернокожими мужчинами у испанцев отмечается вполовину меньшая частота развития этого заболевания, а среди азиатов и коренных обитателей Америки этот показатель в 3 раза ниже.
Интересно, что это различие в частоте для каждой группы рас отмечается только при клиническом раке простаты. W. A.Sakr et al. (1998) показали на примере аутопсийного материала, что у чернокожих мужчин мультифокальный рак чаще выявляется в пределах одного образца. Пациенты с многоочаговыми новообразованиями теоретически имеют более высокую вероятность преодоления последующих клеточных превращений, ведущих к прогрессии опухоли и, следовательно, клинически поддающуюся обнаружению болезнь.
Американские исследователи H.Shimzu et al. (1991) сравнивали зависимость возрастной заболеваемости раком простаты у иммигрантов с японскими и испанскими фамилиями в районе Лос-Анджелеса и частоту этого вида опухоли у представителей коренного населения п рожденных в иммиграции. Частота рака простаты у иммигрантов в Лос-Анджелесе была намного выше, чем у коренного населения.
Подтверждением этому служит и тот факт, что при переезде японцев из Японии на Гавайи, риск возникновения рака простаты возрастает, а при поселении в Калифорнии частота этого вида опухоли у них сходна с таковой у американцев (D. L.Zaridze etal., 1984).
Андрогенная стимуляция
Развитие и рост рака предстательной железы зависит от андрогенной стимуляции. Хотя нет подтверждения тому, что нормальные уровни тестостерона способствуют развитию заболевания, ясно, что введение этого гормона активизирует существовавший ранее тип латентного рака. Известно, что опухолевые образования в простате — аденома и рак — при отсутствии поступающего в кровь тестостерона не возникают.
Случаи возникновения рака предстательной железы у кастрированных мужчин неизвестны. Подтверждением этой теории служат и драматические примеры евнухов — мужчин, которые лишились яичек до пубертатного возраста, либо наблюдения за лицами с редко встречающимися дефектами или отсутствием выработки тестостерона. Влияние этого гормона доказано многочисленными исследованиями в экспериментальных опытах и клинических наблюдениях.
Риск возникновения рака прямо пропорционален андрогенной активности эпителия простаты. Здесь необходимо обратить внимание на весьма важное обстоятельство: вовсе не обязательно должна быть констатация высокого уровня свободного или связанного тестостерона в крови. Наоборот, у 25% мужчин определяется андрогенный дефицит. Андрогенная активность может возрастать вследствие периодически возникающей высокой эндогенной экскреции, и она расценивается как компенсаторный механизм. Высокая активность может объясняться и интенсивным преобразованием тестостерона в дигидротестостерон, а также транскрипцией андрогенных рецепторов.
Все эти процессы происходят на молекулярном уровне, и их уникальные особенности важны для оценки риска возникновения рака простаты. Многие отклонения нарушенной экскреции андрогенов еще не означают их ведущей роли в развитии рака простаты: эти различия у большинства мужчин связаны с метаболизмом андрогенов. В частности, замена в гене 5а-редуктазы в человеческом предстательном типе II позволяет этому ферменту с увеличенной продуктивностью преобразовывать тестостерон в дигидротестостерон.
С 1994 г. в США проводится рандомизированное исследование, охватывающее 18882 мужчины старше 55 лет, которые добровольно принимают ингибитор 5а-редуктазы. У всех участвующих в эксперименте предстательная железа имеет нормальные размеры, уровень простатспецифического антигена (ПСА) менее 3 нг/мл. Пациенты в течение девяти лет получают 5 мг финастерида в сутки или плацебо, у них ежегодно проводится пальцевое ректальное исследование и измеряется уровень ПСА.
Финастерид блокирует энзиматическое превращение тестостерона в активный метаболит дигидротестостерона и широко применяется для лечения аденомы предстательной железы. Профилактический прием финастерида на 25% снижает опасность появления раковых клеток в простате. Результаты широкомасштабного исследования будут опубликованы в 2004 г. и позволят ответить на интригующий вопрос — играет ли ведущую роль сдвиг гормонального равновесия в возникновении рака простаты?
Несмотря на накопленные знания многих аспектов молекулярно-генетических нарушений при раке предстательной железы, мы все еще далеки от разработки оптимального подхода в лечении. Неодинакова роль гормонов, которые определяют течение или управление различными стадиями. В первую очередь, это касается основного гормона — тестостерона.
В литературе продолжают активно вестись дебаты относительно влияний больших концентраций тестостерона на развитие рака простаты. P.H.Gann et al. (1996) поддерживают мнение, многими оспариваемое, что существует явная взаимосвязь между уровнями андрогена сыворотки и раком простаты. Еще один фактор, вызывающий всеобщее беспокойство, — это противоречивые сообщения, рассматривающие означенную связь. Любопытным подтверждением тому стал обзор S. Slater et al. (2000), которые сосредоточили свое внимание на роли тестостерона как причинного фактора развития рака простаты.
И все же современный мета-анализ констатирует, что у мужчин с наивысшими уровнями тестостерона в сыворотке заболеваемость раком простаты вероятнее, чем у мужчин с самыми низкими уровнями (T.Shanayfclt et al., 2000). Авторы считают, что подавляющее количество данных не подтверждают концепцию о способности тестостерона, имеющего нормальные уровни в сыворотке крови, хоть как-то влиять на повышение риска развития злокачественных опухолей предстательной железы.
Несмотря на множество сведений, подтверждающих явную связь между половыми гормонами и ростом злокачественных опухолей, существует ряд озадачивающих вопросов, касающихся особым образом рака простаты, которые и до настоящего времени остаются нерешенными. На экспериментальном уровне показано, что клеточная линия рака простаты (LNCaP), которая вначале требует для своего роста начальной активизации андрогенами, в конечном итоге ими же и подавляется.
Не у всех пациентов, находящихся под длительным наблюдением, фиксируется существование явной связи между развитием рака и уровнем тестостерона, более того, ряд исследователей доказывают, что во время установления диагноза рака простаты уровни бывают скорее низкими, чем высокими (М.Е. Harper et: al., 1984). Несколько проведенных ранее клинических исследований доказывают изменчивую реакцию существующих форм рака простаты на введение половых гормонов.
Так, одни опухоли активизируются, в то время как другие подавляются. Подобные наблюдения еще сохранились в памяти старшего поколения урологов, занимающихся проблемами лечения рака простаты. Эти противоречивые мнения привели к радикальной и очень спорной гипотезе, что пониженные (скорее, чем высокие) уровни андрогенов являются главными факторами, способствующими развитию рака простаты. Для ее доказательства нужны подтверждения многочисленных исследований.
За последние несколько лет пересмотрена роль тестостерона в генезе рака предстательной железы. И действительно, концепция генетических нарушений, на разных этапах участвующих в развитии заболевания, позволяет по-новому осветить место этого гормона в новообразовательном процессе. До недавнего времени поддерживалось мнение, что тестостерон несет прямую ответственность за возникновение рака простаты.
Но теперь уже хорошо известно, что онкогенез рака предстательной железы проходит в несколько этапов, в которых принимают участие:
М. Pollard et al. (1989) образно сравнивают взаимосвязь тестостерона с ростом рака простаты с ролью кислорода в процессе горения. Полное прекращения доступа кислорода гасит пожар, точно так же, как и исключение андрогенов тормозит или вовсе останавливает рост рака простаты. Однако кислород не является причиной огня, а андрогены не вызывают развития рака простаты. Некоторые специалисты называют такое сравнение спорным, поскольку при специфических экспериментальных условиях на клеточных культурах была показана возможность возникновения рака простаты с помощью вводимого тестостерона (L.I.Gooren, 1999; M.T.Story, 1994).
С другой стороны, H.Y.Zhau et al. (1996) обнаружили, что андрогенный дефицит может стимулировать прогрессию андрогеннезависимого рака простаты in vitro, полагая, что предраковые изменения клеток наиболее отчетливо поддаются гормональному влиянию с последующим превращением их в истинно раковые клетки.
Переход осуществляется в цени непрерывных молекулярных превращений прежде нормальных простатических клеток в состояние интраэпителиальной простатической неоплазии. Все это, в конечном счете, ведет к развитию различной степени раковой дифференциации. Данная гипотеза исходит из того, что не все простатические клетки с интраэпителиальной неоплазией принимают участие в развитии раковых клеток предстательной железы.
Механизмы эндогенной регуляции рака предстательной железы
Разработка методов лечения опухолевых заболеваний предстательной железы на протяжении более двух веков проходила в русле поиска механизма гормональной зависимости этого органа. Впервые связь роста предстательной железы с функцией яичек была подмечена J. Hunter в 1786 г., однако в его исследованиях не упоминаются эндокринные факторы. A. A. Bcrthold (1849) высказал предположение об эндокринной связи, полагая, что вырабатываемые яичками вещества влияют на рост предстательной железы.
Но только спустя более 100 лет идея уменьшения массы увеличенной предстательной железы (полагаем, что это была аденома) оказалась реализованной в клинике путем кастрации. J.W.White (1895) доказал эффективность лечения старческого разрастания предстательной железы на анализе историй болезни 111 мужчин. Заметное уменьшение увеличенной предстательной железы наблюдалось у 87% оперированных, а смертность составила 18%. Выявляемые вскоре тяжелые психические расстройства по типу выраженной депрессии оказались несоизмеримыми со степенью увечья.
Отчасти по этой причине, а также из-за отсутствия сведений о химическом строении выделяемого яичками субстрата врачи отказались от процедуры кастрации для лечения увеличенной предстательной железы. Новый всплеск интереса к этому радикальному методу наблюдался после привнесения в урологическую практику сильнодействующего андрогенного соединения, выделенного в 1935 г. David et al. из свежей тестикулярной ткани и названного тестостероном. Открытие этого гормона снова привлекло внимание к потенциальному использованию кастрации, но уже как метода лечения рака предстательной железы.
Опыт клинического применения кастрации в качестве эффективного метода лечения злокачественной опухоли простаты в последующем был обобщен в работе С.Huggins и C.V.Hodges (1941). Одновременно с проведением кастрации, они осуществляли и инъекцию эстрогенов для лечения метастатического рака предстательной железы, заложив, по существу, общепринятый теперь принцип максимальной андрогенной блокады.
Параллельно с разработкой методов лечения рака уточнялись сложные взаимоотношения предстательной железы с иными гормонально активными органами и системами. Было выяснено, что источником секреции андрогенов, которые на 95% вырабатываются в яичках, являются также и надпочечники (5%). Резидуальные андрогены сетчатой зоны коры надпочечников — андростендиол и андростендион, обладая в нормальных условиях низкой эффективностью, при раке предстательной железы превращаются в активные соединения, стимулирующие рост раковых клеток.
Процентное соотношение малоактивных адренальных андрогенов, согласно исследованиям F. Labrie (1991), заметно меняется за счет усиления роли эндокринной ткани предстательной железы, трансформирующей неактивные стероидные предшественники в активный дигидротестостерон. По данным того же автора, содержание в плазме крови взрослого мужчины дигидроэпиандростеронсульфата в 100— 500 раз выше, чем тестостерона, что создает значительный субстрат для превращения его во внутриклеточный тестостерон простаты.
В сложном процессе регуляции тестостерона задействована гипоталамо-гипофизарно-гонадная ось. В упрощенном варианте ее функционирующий механизм можно представить следующим образом. Под влиянием гипоталамического нейромедиатора норэпинефрина в Area praeoptica сецернируется гонадотропный рилизинг-гормон (ГРГ), который через портальные сосуды гипофиза достигает его передней доли, где стимулирует выработку лютеинизирующего (ЛГ), а также фолликулостимулирующего (ФСГ) и адренокортикотропного (АКТГ) гормонов.
Лютеинизирующий гормон в свою очередь побуждает клетки Лейдига к образованию тестостерона. Другие андрогены, такие, как дитидроэпиандростерон или дигидротестостерон, а также слабый эстроген андростендиол сецернируются, как указывалось ранее, в значительно меньшем количестве, однако они тоже превращаются в тестостерон. Андрогены имеют различную степень влияния на отдельные органы и системы. Тестостерон оказывает прямое действие на центральную нервную систему, семенной эпителий и скелетную мускулатуру; на предстательную железу, кожу гениталий или волосяные фолликулы он действует только как прогормон. Для предстательной железы как органа-мишени дигидротестостерон является важнейшим андрогеном.
Благодаря новейшим исследованиям различных патомеханизмов возникновения рака предстательной железы получило подтверждение знание того, что тестостерон играет центральную роль в патогенезе этого заболевания.
Различают четыре основных пути воздействия на регуляцию клеточных изменений предстательной железы:
1. Аутокринная регуляция эпителиальных клеток.
2. Паракринная регуляция между эпителиальными и стромальными клетками.
3. Автономная экспрессия онкогенов.
4. Потеря супрессорных генов.
В более подробном освещении отдельных механизмов регуляции этот процесс выглядит следующим образом:
1) аутокринная регуляция означает рост эпителиальных клеток за счет их освобождающихся субстанций. Примером может служить аутостимуляция простатических клеток посредством фибробластического фактора роста (FGF) и трансформирующего фактора роста Вi (TGF-Вi), которые продуцируются эпителиальными клетками. Их влияние на рост различно и зависит от концентрации андрогенов: при их отсутствии или очень низких значениях усиливается программированная клеточная смерть, а в случаях повышенного содержания андрогенов отмечается усиление пролиферации;
2) паракринная (межклеточная) регуляция означает рост за счет освобождающихся субстанций между эпителиальными и стромальными клетками простаты. Типичным примером является образование и секреция в стромальных клетках таких факторов, как кератиновый фактор роста (KGF) и трансформирующий фактор роста (TGF-В). Эти медиаторы влияют через KGF или TGF-В-рецепторы на эпителиальную пролиферацию. При этом оказывается, что высокий уровень KGF и уменьшенный TGF-В усиливают пролиферацию простатических эпителиальных клеток. Этот андрогеннезависимый рост наблюдается как в нормальной простате, так и при аденоме предстательной железы, а также при некоторых формах рака этого органа;
3) механизмы роста могут действовать за счет сверхэкспрессии генов факторов роста или активации онкогенов. К примеру, усиление образования рецепторов для трансформирующего фактора роста (TGF-a) или эпидермального фактора роста (EGF-R), которые могут активизировать аутокринные механизмы или процессы фосфорилирования, приводит к так называемому вторичному предвестнику каскада роста эпителиальных клеток. Подобным образом может действовать и интерлейкин 6 (IL-6), влияя паракринно на стромальные клетки либо аутокринно — на эпителиальные;
4) следующий механизм пролиферации роста возникает из-за потери супрсссорных генов. Пример - ингибиция пролиферации за счет гетеромерных рецепторов для TGF-В (TpRI и TВRII). Оба они необходимы для сигнальной индукции. Мутация в TВRI-гене ведет к потере супрессорной активности и вместе с тем к пролиферации.
Перечисленные механизмы не объясняют всех возможностей роста раковых клеток, но приближают к более точному пониманию этих сложных молекулярно-генетических процессов.
Разработка и внедрение в клиническую практику молекулярно-генетических методов способствовали широкому использованию урологами генетической терминологии, как-то: супрессия, мутация, ингибиция, экспрессия, деления, транскрипция и др.
Понимание терминологии и молекулярно-генетических процессов онкогенеза в предстательной железе становится неотъемлемой частью современной урологии. Их правильное восприятие представляется важнейшим условием управления ранней диагностикой и эффективностью лечения рака простаты.
Читайте также:

