Актуальность проблемы рака толстой кишки
Рак прямой и ободочной кишки (колоретальный рак) сегодня можно без преувеличения обозначить как проблему мирового масштаба.
Известно, что на 1-м месте по заболеваемости, среди мужчин, стоит рак легкого, среди женщин – рак молочной железы. Колоректальный рак постепенно выходит на 2-е место, имея тенденцию к непрерывному росту заболеваемости. Эта тенденция особенно выражена в индустриально развитых странах. Являясь центром современного глобализованного мира, они вовлекают в свою орбиту страны с менее развитой економикой навязывая им в числе многих факторов свой, „индустриальный” образ жизни. Одной из характеристик такого образа жизни является питание. Именно с его особенностями большинство учених связывают быстрый рост заболеваемости и смертности от колоректального рака.
Приведем некоторые данные, позволяющие представить масштаб проблемы. Так, по данным ВООЗ, ежегодно в мире регистрируется около одного миллиона новых случаев больных КРР, при этом более 150 тысяч случаев заболевания приходится на США. В этой стране ежегодно от КРР умирает 55 тысяч больных. В США смертность от КРР находится на 3 месте. Подобная картина отмечается и в странах Европейского Союза, Российской Федерации, где уровень заболеваемости составил в 1997 году 16,2 на 100 тысяч населения. В крупных мегаполисах (Москва, Санкт-Петербург) заболеваемость составляет 30,3 и 33,6 случаев. Экономические потери от лечения больных КРР в США составляют 6,5 миллиарда долларов в год. Среди других локализаций злокачественных опухолей КРР имеет очень высокие темпы роста, по которым находится на 2 месте в мире.
В Украине, в 2003 году, зарегистрированный показатель заболеваемости КРР - 38 случаев на 100 тисяч населения, что соответсвует европейским и мировым тенденциям. В чем причина такого стремительного роста этой патологии и почему возникает рак прямой и ободочной кишки? Ответ на этот вопрос находится в плоскости характера питания больных, условиях их жизни, определяемых стремительной урбанизацией и глобализацией технократического общества. КРР неравномерно распространён среди жителей планеты.
Так, в странах Западной Европы и США заболеваемость составляет 30-40 случаев на 100 тысяч населения, а в странах Африки и Азии – всего – 3-4 случая. И как показали дальнейшие исследования, дело здесь не в этническом факторе, среди эмигрантов из стран Азии и Африки заболеваемость раком прямой и ободочной кишки соответствует заболеваемости коренного населения этих стран. Какие же особенности питания отмечены в странах с высоким уровнем заболеваемости раком прямой и ободочной кишки? Это прежде всего избыточность потребления продуктов питания над потребностью человека, или проще говоря переедание. Установлено, что риск развития рака прямой и ободочной кишки повышается на 2,3% с каждыми 100 калориями, потребленными сверх нормы. Установлено, что большое значение при этом имеет и состав пищи – большую роль играет употребление животных жиров, мяса и клетчатки. Употребление животных жиров и мяса стимулирует развитие рака прямой и ободочной кишки, в то время как употребление клетчатки снижает риск заболеваемости.
Многими научными работами доказано, что избыток желчных кислот в кишечнике, возникший как реакция на животные жиры и белки, является строительным материалом для эндогенного синтеза канцерогенов. Большое значение в этом процессе имеет и микрофлора кишечника, которая из сапрофитной (при питании преимущественно богатом клетчаткой) становится патогенной анаэробной (при питании, содержащем животные белки и жиры). Продукты распада белков, желчные кислоты и анаэробная микрофлора кишечника, которая интенсивно их разрушает, и являются главными составляющими эннного синтеза канцерогенов. Доказано значение наследственной предрасположенности к возникновению рака прямой и ободочной кишки. Современная генетика выделяет ряд генов, высокая экспрессия которых в клетках слизистой оболочки толстой кишки, позволяет определять неблагоприятный прогноз для возникновения рака прямой и ободочной кишки. Канцерогенные соединения приводят к мутациям генов, в частности гена АРС (аденоматозного полипоза кишечника), а в дальнейшем МСС (мутированного колоректального ракового гена), группы ras-генов, что в конце концов и приводит к появлению клона атипичных клеток опухоли. Опухоль развивается медленно, проходя стадию аденоматозного полипа с последующим, достаточно длительным процессом малигнизации.
Большое значение имеют размеры, и морфологическое строение аденоматозных полипов. Так, по морфологической структуре выделяют тубулярные, тубулярно-ворсинчатые и ворсинчатые (вилезные) аденомы. Количество малигнизированных аденом при этом соответственно составляет 5% , 23% и более 40-45% соответственно. Индекс малигнизации одиночных полипов составляет 2-4%, множественных (более 2) – 20%. Такое же значение имеет и
размер опухоли: так при размере ворсинчатой опухоли до 1см частота озлокачествления составляет около 10%, а при размере более 2 см – 53%.
Факторы риска в заболеваемости раком прямой и ободочной кишки
На сегодняшний день выделены факторы риска заболевания колоректальным раком. Это:
- Возраст пациентов старше 50 лет;
- Особенности питания;
- Генетические синдромы – диффузный семейный полипоз, синдром Гарднера-Тернера, синдром Пейтца-Эгерса, болезнь Тюрка;
- Наличие аденом ободочной кишки;
- Язвенный колит;
- Болезнь Крона;
- Наличие в анамнезе КРР у родственников, ранее перенесенный рак молочной железы и/или женских половых органов.
У больных с хроническими воспалительными заболеваниями прямой кишки, особенно с язвенным колитом, частота рака прямой кишки значительно выше, чем в общей популяции. На степень риска возникновения рака влияют длительность и клиническое течение заболевания. По данным литературы, риск возникновения рака прямой кишки при длительности заболевания до 5 лет состави от 0 до 5 %, до 15 лет – 1,4 – 12%, до 20 лет 5,4 – 20 %, до 30 лет – 50%.
Скрининг в диагностике рака прямой и ободочной кишки
Принцип онкологии – чем раньше выявлен опухолевый процесс, тем эффективнее его лечение, в полной мере относится и к КРР. На ранних стадиях развития аденоматозные полипы и колоректальные карциномы являются безсимптомными. Наиболее доступным, дешевым и простым методом их выявления служит гемоккультный тест или исследование кала на скрытую кровь. Он основывается на том, что колоректальные карциномы травмируются и выделяют в просвет кишки кровь, которая часто не определяется макроскопически, но может быть определена специальными методами исследования – гемокульттестом. Исследования формально здорового населения показывают положительный гемоккультный тест у 3-6% обследованых. При этом рак выявляется в 10% cлучаев, а полипы – в 20-40%. Однако в 50-70 % случаев он бывает ложноположительным. Несмотря на низкую специфичность этого теста, массовое его использование, по мнению специалистов, может позволить снизить смертность от КРР на 30%. Себестоимость этого метода в США составляет 15 $.
Другим методом ранней диагностики рака прямой и ободочной кишки является эндоскопическое исследование толстой кишки – колоноскопия. Этот метод позволяет выявить колоректальный рак в І стадии у 80 % больных. Своевременно предпринятая эндоскопическая эксцизия полипов, является профилактикой их малигнизации, а эндоскопическое лечение аденокарцином в I стадии приводит к 15-летней выживаемости у 90% больных. Американская ассоциация врачей рекомендует проведение гемоккультного теста 1 раз в год, а колоноскопию раз в 3-5 лет у лиц переступивших порог 50 летнего возраста. Современные методики видеоколоноскопии позволяют документировать все изменения со стороны слизистой оболочки толстой кишки и архивировать материал. Дальнейшее совершенствование колоноскопии привело к появлению хромоколоноскопии – методе, позволяющем выявлять на фоне окрашенной слизистой оболочки кишечника очень маленькие полипы – 0,1-0,2 см, которые не выявляются при обычной колоноскопии. Для удаления таких образований разработана методика эндоскопической мукозэктомии.
Еще одно направление в раннем выявлении рака прямой и ободочной кишки основано на определении РЕА – раково-эмбрионального антигена – пептида, выделенного из эмбриональных клеток желудочно-кишечного тракта. Было установлено, что его повышение (более 6 мкг/литр) отмечено у больных со злокачественными опухолями толстой кишки, матки, молочной железы. В исследованиях российских ученых было показано, что повышение уровня РЕА в крови было отмечено у 38% больных с полипами и увеличивалось по мере нарастания анаплазии и увеличения размеров опухоли.
Так при 1-2 стадиях (по классификации UICC) увеличение уровня РЕА было уже у 52% больных, а при 4 стадии – у всех больных. Определение РЕА нашло широкое применение в динамическом наблюдении за больными – резкое повышение его уровня в сыворотке крови больного находящегося под наблюдением свидетельствует о появлении рецидива заболевания и должно побуждать врача к его клинической и морфологической верификации.
Будущее в ранней диагностике колоректального рака очевидно будет принадлежать генетическому неинвазивному скринингу КРР, который основан на том, что клетки рака прямой и ободочной кишки выделяются с калом из которого их можно выявить и провести исследование мутантных генов (К-RAS, TP-53 и др.) в выделенной и умноженной с помощью полимеразной цепной реакции ДНК опухолевых клеток.
Реально же, КРР диагностируется в 3-4 стадиях (по классификации международного противоракового союза - UICC) в 70 % случаев, что требует признания ранней диагностики этого заболевания неудовлетворительной.
Клиника рака прямой и ободочной кишки
Наиболее характерными симптомами рака прямой кишки являются кишечные кровотечения, нарушения стула, боль в животе и тенезмы. Кишечное кровотечение, примесь крови к стулу или наличие скрытой крови отмечаются практически в у всех больных раком прямой кишки.
Выделение алой крови типично для рака анального канала и прямой кишки. Темная кровь более характерна для левой половины ободочной кишки. При этом кровь, смешанная с калом и слизью, является более достоверным признаком. При раке правой половины обычно наблюдается скрытое кровотечение, сопровождающееся анемией, бледностью кожных покровов и слабостью.
Нарушение стула, чаще в виде затруднения дефекации, характерно для поздних форм рака левой половины ободочной и прямой кишки. Иногда рак прямой кишки сразу проявляется острой кишечной непроходимостью, требующей срочного оперативного вмешательства.
При раке прямой кишки больные, как правило, жалуются на чувство неполного опорожнения или ложные позывы на дефекацию. Нередко абдоминальные боли отсутствуют, больных в основном беспокоят слабость, потеря аппетита, снижение массы тела. В поздних стадиях заболевания присоединяются гепатомегалия и асцит.
Диагностика рака прямой и ободочной кишки
Для рака прямой кишки очень важным является предоперационное стадирование, которое осуществляется с помощью трансректального УЗИ. При наличии подозрения или выявлении метастатического поражения печени и/или легких обязательным является выполнение компъютерной томографии (КТ).
Алгоритм диагностики рака прямой кишки:
- Анализ жалоб и анамнеза (следует помнить, что у лиц старше 50 лет риск возникновения рака прямой кишки очень высок)
- Клинические исследования
- Пальцевое исследование прямой кишки
- Ректороманоскопия
- Анализ кала на скрытую кровь
- Колоноскопия
- Ирригоскопия (при сомнительных данных колоноскопии или их отсутствии)
- Ультразвуковое исследование органов живота и малого таза
- Трансректальное УЗИ
- Биопсия обнаруженной опухоли
При анализе жалоб и анамнеза необходимо обращать внимание на особенности кишечной симптоматики. Для заболеваний прямой кишки характерна некоторая монотонность симптоматики. Большинство из них проявляются либо нарушениями дефекации, либо примесью крови и слизи к стулу, либо болью в животе или прямой кишке. Часто эти симптомы сочетаются между собой. Те же симптомы и даже в тех же сочетаниях наблюдаются у больных раком прямой кишки.
Нет ни одного специфического признака этого заболевания. Данное обстоятельство следует учитывать врачам всех специальностей, к которым могут обратиться больные с жалобами на кишечный дискомфорт. Любая кишечная симптоматика должна расцениваться как возможный признак рака прямой кишки, особенно у лиц старше 50 лет.
Большинство опухолей (до 70%) локализуется в дистальных отделах толстой кишки (прямая и сигмовидная), именно поэтому роль таких простых диагностических приемов, как пальцевое исследование, ректороманоскопия, нельзя преувеличить. Например, для выявления рака нижнеампулярного отдела толстой кишки практически достаточно одного пальцевого исследования. Для использования всех диагностических возможностей применяемых методик очень важна правильная подготовка прямой кишки и исследование. В противном случае возможны грубые диагностические ошибки.
Важным методом диагностики распространенности опухолевого процесса является ультразвуковое исследование. С его помощью устанавливается не только наличие отдалённых метастазов, но и степень местного распространения опухоли, а также наличие или отсутствие перифокального воспаления. Целесообразно использовать четыре вида ультразвукового исследования: чрескожный, трансректальный, эндоскопический, интраоперационный.
В случаях прорастания опухоли в окружающие органы и ткани рекомендуется компьютерная томография и ядерно-магнитный резонанс.
Классификация рака прямой и ободочной кишки
Для определения степени распространенности колоректальный рак классифицирован по стадиям. Наибольшего распространения на Украине получило стадирование колоректального рака по системе ТNM в 6-й редакции 2002 года.
По классификации ТNM рассматривают три критерия распространения опухоли:
- Т – распространение на стенку толстой кишки и окружающие ткани;
- N – распространение опухоли по лимфатическим путям, в частности метастатическое поражение лимфоузлов;
- М – наличие или отсутствие отдаленных метастазов.
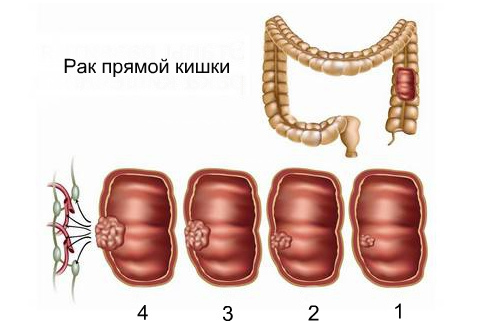
Отмечают такие возможные варианты критерия Т:
- Тх – первичная опухоль не может быть оценена,
- Т0 – первичная опухоль не найдена,
- Тis – наличие внутриэпителиальной опухоли в том числе с инвазией базальной мембраны,
- Т1 – опухоль прорастает в подслизистый слой,
- Т2 – опухоль прорастает в мышечный слой,
- Т3 – опухоль прорастает в субсерозную ткань и серозную оболочку.
- Т4 – опухоль прорастает в висцеральную брюшину или врастает в окружающие органы.
Критерий N может иметь следующие значения:
- Nх – регионарные лимфоузлы не могут быть оценены;
- N0 – отсутствие метастазов в регионарных лимфоузлах;
- N1 – выявлены метастазы в 1-3 регионарных лимфоузлах;
- N2 – метастазы в 4-х или более регионарных лимфоузлах.
Критерий М может быть таким:
- Мх – не уточнено наличие отдаленных метастазов;
- М0 – отдаленные метастазы не определяются;
- М1 – выявляются отдаленные метастазы;
Довольно распространенной классификацией КРР, которая часто используется в странах Евросоюза и США, является классификация по Дюксу, согласно которой выделяют 3 стадии опухолевого процесса, обозначаемые буквенными латинскими символами А, В, С D. Стадия А – опухоль не инфильтрирует серозной оболочки кишки, стадия В – опухоль прорастает в серозную оболочку, стадия С – опухоль с поражением регионарных лимфоузлов, независимо от степени прорастания опухоли в стенку кишки, стадия D – опухоль любых размеров при наличии отдаленных метастазов.
Осложнения
Наиболее частыми осложнениями рака прямой и ободочной кишки являются нарушение кишечной проходимости, вплоть до острой кишечной непроходимости, кишечные кровотечения, перифокальное воспаление и перфорации кишки, либо в зоне опухоли, либо так называемые дилятатические, из-за перерастяжения кишечной стенки при непроходимости. При правосторонней локализации у больных нередко возникает анемия из-за длительно продолжающихся кишечных кровотечений.
Все осложнения требуют соответствующего лечения, иногда срочных и даже экстренных оперативных вмешательств для спасения жизни больных, например, при диффузном кровотечении, острой кишечной непроходимости и перфорации. У больных с запущенными формами колоректального рака перечисленные осложнения могут сочетаться, значительно увеличивая риск и ухудшая прогноз хирургического лечения.
Профилактика осложнений состоит в своевременной ранней диагностике рака прямой кишки.
Изучение клинической картины степеней нарушения кишечной проходимости и разработка алгоритма лечебной тактики в зависимости от клинических, лучевых и функциональных проявлений. Критерии объективной оценки эндогенной интоксикации, оценка ее эффективности.
| Рубрика | Медицина |
| Вид | автореферат |
| Язык | русский |
| Дата добавления | 19.01.2018 |
| Размер файла | 255,1 K |
- посмотреть текст работы
- скачать работу можно здесь
- полная информация о работе
- весь список подобных работ
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
- 1
- 2
- 3
Автореферат
диссертации на соискание ученой степени
доктора медицинских наук
Оптимизация хирургического лечения рака толстой кишки, осложненного кишечной непроходимостью
Шишкина Галина Андреевна
Научный консультант
доктор медицинских наук, профессор Топузов Эскендер Гафурович
Официальные оппоненты
член-корреспондент РАМН, заслуженный деятель науки РФ, доктор медицинских наук, профессор Поташов Лев Васильевич
доктор медицинских наук, профессор Лемехов Владимир Григорьевич
доктор медицинских наук, профессор Борисов Александр Евгеньевич
Ученый секретарь Диссертационного совета доктор медицинских наук, профессор Команденко М.С.
Общая характеристика работы
кишечный проходимость интоксикация клинический
Актуальность проблемы. В последние годы отмечается постоянный рост заболеваемости и смертности от рака толстой кишки. По данным Популяционного ракового регистра, в структуре онкологической заболеваемости населения Санкт-Петербурга в 2006 году колоректальный рак занимал II место (Борисов А.Е., 2007; Мерабишвили В.М., 2007). Рост показателей заболеваемости обусловлен увеличением числа больных старше 60 лет (Мартынюк В.В., 2000; Шелыгин Ю.А. и др., 2007). Обращает на себя внимание низкая выявляемость заболевания на ранних стадиях.
Большая часть больных госпитализируется в общехирургические отделения по скорой помощи, в связи с нарушением кишечной проходимости. Все это определяет актуальность выбранного исследования (Яицкий Н.А. и др., 2004; Васильев С.В. и др., 2005; Воробьев Г.И. и др., 2007; Федоров В.Д. и др., 2007; Becker H., 1995; Yasutomi M., 1997; Hojo K., 1998; Guillen J.G., и др. 1999).
Лечение рака ободочной кишки, осложненного непроходимостью, является сложной проблемой. При плановых операциях послеоперационная летальность за последние годы снизилась и составляет 2,5-6,6% (Воробьев Г.И. и др., 2002; Чиссов В.И. и др., 2002; Яицкий Н.А. и др., 2002; Стойко Ю.М. и др., 2003; Топузов Э.Г. и др., 2006). В то же время при раке, осложненном кишечной непроходимостью, послеоперационная летальность достигает 20-60% (Петров В.П., Ерюхин И.А., 1989; Иноятов И.М. и др., 1991; Виячки Ив., 1993; Земляной А.Г. и др., 1993; Champaut и др., 1983; Zlatarski и др., 1991; Iversen L.H. и др., 2008).
Еще хуже результаты лечения диастатических перфораций толстой кишки, возникающих на фоне нарушения проходимости. Тяжесть клинического течения развивающегося при этом перитонита обусловливает высокую летальность, которая по данным различных авторов составляет от 40 до 80% (Яновой В.В. и др., 1995; Алиев С.А., 1999; Зубрицкий В.Ф. и др., 2007; Koperna T. и др., 1997). Это вызвано тем, что не существует четкой позиции относительно показаний и способов завершения субтотальной колэктомии, когда оптимально заканчивать эту операцию формированием анастомоза, а в каких случаях созданием илеостомы.
Остаются не вполне выясненными вопросы патофизиологии, диагностики и лечения эндотоксикоза, возникающего при осложненном раке толстой кишки.
Очевидно, что для эффективного лечения больных осложненным раком толстой кишки необходима разработка рациональной тактики диагностики и лечения. Она должна основываться на критериях, определяющих выбор адекватного хирургического вмешательства и стандартизации принципов лечебной помощи.
Цель исследования
Целью исследования является разработка и обоснование системы оптимизации диагностики и лечения рака толстой кишки, осложненного нарушением кишечной проходимости, с учетом патофизиологии эндотоксикоза и использованием энтеро- и колоносорбции в предоперационном периоде и интраоперационной декомпрессии кишечника с сорбционным диализом.
Задачи исследования
1. Изучить клиническую картину степеней нарушения кишечной проходимости и разработать алгоритм лечебной тактики в зависимости от клинических, лучевых и функциональных проявлений.
2. Выработать критерии объективной оценки эндогенной интоксикации.
3. Усовершенствовать методы и проанализировать результаты дооперационной детоксикации путем энтеро- и колоносорбции.
4. Осуществить интраоперационный толстокишечный сорбционный диализ и оценить его эффективность.
5. Разработать методику операции, предусматривающую интраоперационную декомпрессию кишечника, с целью улучшения его кровоснабжения, моторики и уменьшения эндогенной интоксикации.
6. Изучить ближайшие и отдаленные результаты лечения больных.
Научная новизна. Впервые на обширном клиническом материале проведен анализ состояния экстренной хирургической помощи больным с осложнениями рака ободочной кишки, разработаны методы лечения больных с учетом патофизиологии эндотоксикоза. Расширено представление об использовании энтеро- и колоносорбции при различных степенях нарушенной кишечной проходимости вследствие рака. Показано накопление веществ низкой и средней молекулярной массы (ВНиСММ) в плазме, эритроцитах и моче больных раком толстой кишки, осложненным нарушением кишечной проходимости. Установлено, что применение энтеро- и колоносорбции в предоперационном и интраоперационном периодах снижает выраженность воспалительных явлений и понижает уровень эндогенной интоксикации у больных, что сопровождается снижением частоты возникновения послеоперационных осложнений и летальности. Впервые показано, что энтеро- и колоносорбция способствуют более быстрому устранению общих воспалительных проявлений, восстановлению противоопухолевого иммунитета в послеоперационном периоде.
Впервые разработан метод хирургического лечения рака толстой кишки, осложненного острой кишечной непроходимостью, предусматривающий интраоперационную декомпрессию кишечника с целью улучшения его кровоснабжения, моторики и уменьшения эндогенной интоксикации.
Разработан алгоритм действий хирурга при диагностике и лечении рака толстой кишки, осложненного нарушением кишечной проходимости и перфорациями кишки. Впервые определены показания к хирургическому лечению в объеме субтотальной колэктомии при раке левой половины толстой кишки, осложненном декомпенсированным нарушением кишечной проходимости с диастатическими разрывами серозной оболочки проксимальных отделов. Разработана методика завершения субтотальной колэктомии формированием анастомоза или илеостомы в зависимости от выраженности перитонита.
Научно-практическая значимость. Разработаны принципы диагностики и лечения больных раком ободочной кишки, осложненным нарушенной кишечной проходимостью. Применение предложенных методик позволяет в значительной степени улучшить непосредственные и отдаленные результаты лечения, качество жизни и возвратить больных к активному труду и социально-полезной деятельности. Практическое значение имеет выбор разработанных методов лечения на основе выделенных интраоперационных критериев и их сочетаний, во многом определяемых степенью тяжести осложнений, общим состоянием и сопутствующими заболеваниями больных. Внедрение методов энтеро- и колоносорбции в программу комплексного лечения больных раком толстой кишки позволяет существенно улучшить непосредственные результаты и сократить сроки стационарного лечения, снизить частоту послеоперационных осложнений. Доказано, что применение энтеросорбентов в предоперационном периоде оказывает отсроченный противовоспалительный и иммунокорригирующий эффект в послеоперационном периоде. Разработан метод операции при декомпенсированном нарушении кишечной проходимости вследствие рака, предусматривающий резекцию левой половины ободочной кишки с интраоперационной декомпрессией кишечника и применением интраоперационного толстокишечного сорбционного диализа. В комплексе лечебных мероприятий метод сопровождается значительным снижением летальности и сокращением частоты осложнений. Дифференцированный подход к выбору хирургической тактики позволяет снизить послеоперационную летальность, уменьшить частоту послеоперационных осложнений и улучшить качество жизни больных.
Предложенная хирургическая тактика лечения больных с осложненным раком ободочной кишки внедрена в ряде лечебно-профилактических учреждений Санкт-Петербурга и Ленинградской области, в учебный и лечебный процессы кафедры госпитальной хирургии с курсом детской хирургии Амурской государственной медицинской академии.
Личный вклад автора. Автором лично выбрана тема работы, разработана программа, осуществлялось планирование, организация и исследования по всем разделам работы. Автор является основным участником экспериментальных и клинических исследований. Автор лично выполнял оперативные вмешательства при осложненном раке толстой кишки. Самостоятельно проведен анализ литературы по исследуемой проблеме, собран и проанализирован клинический материал. Отдельные исследования (эксперименты на животных, биохимические, иммунологические) выполнены совместно со специалистами лабораторий соответствующего профиля, за что автор выражает благодарность. Доля участия автора в накоплении материала составляет 80%, в анализе и обобщении материала - 100%
Основные положения, выносимые на защиту.
1. Результаты лечения осложненного рака ободочной кишки в значительной мере зависят от степени нарушения кишечной проходимости.
2. Степень нарушения кишечной проходимости определяет набор и последовательность применения специальных инструментальных методов исследования.
3. Выраженность эндогенной интоксикации определяется уровнем содержания веществ низкой и средней молекулярной массы в крови и моче, а также их соотношением.
4. Энтеро- и колоносорбция в пред- и интраоперационном периодах снижает выраженность воспалительных явлений, уменьшает уровень эндогенной интоксикации, что сопровождается снижением частоты возникновения послеоперационных осложнений и летальности.
5. Энтеро- и колоносорбция оказывают противовоспалительный и отсроченный иммунокорригирующий эффект в послеоперационном периоде.
6. Наиболее рациональным, как с хирургических, так и с онкологических позиций, представляется не только ликвидация нарушения проходимости, но и радикальное удаление опухоли при первом же вмешательстве. Это достигается путем первичной резекции толстой кишки вместе с опухолью, опорожнением переполненных приводящих петель кишки через удаляемый препарат, их санацией и формированием открытой плоской терминальной колостомы.
7. Операцией выбора при раке толстой кишки, осложненном острой кишечной непроходимостью и диастатическими перфорациями, является субтотальная колэктомия.
Публикации. По теме диссертации опубликованы 62 научные работы, в том числе 16 в ведущих рецензируемых журналах и изданиях, рекомендуемых ВАК.
Структура и объем диссертации. Диссертация изложена на 297 страницах машинописного текста, состоит из введения, 6 глав, заключения, выводов, практических рекомендаций, списка литературы и приложений. Работа содержит 75 таблиц и 14 рисунков. Библиографический указатель содержит 534 наименования (371 отечественных и 163 иностранных авторов).
Материалы и методы исследования
Работа выполнена на кафедре хирургических болезней № 1 с курсом детской хирургии Санкт-Петербургской государственной медицинской академии им. И.И.Мечникова и на базе научного центра сорбционных технологий Санкт-Петербургской медицинской академии последипломного образования (зав. центром - д.м.н. А.В. Соломенников).
Наблюдался 1071 больной с осложненным раком толстой кишки. Больные поступали в клинику хирургических болезней № 1 СПбГМА им. И.И. Мечникова и оперировались там же с 1986 по 2008 год. Больные были разделены на три группы в зависимости от степени нарушения проходимости согласно классификации Э.Г.Топузова (1986) и оценки состояния согласно SAPS. Компенсированное нарушение проходимости было у 713 (67%) больных, субкомпенсированное - 196 (18%), декомпенсированное - 162 (15%).
Исследование влияния колоносорбции в предоперационном периоде у больных с компенсированным и субкомпенсированным нарушением проходимости проведено у 76 больных. Из них 41 пациенту проводилась обычная предоперационная подготовка (группа сравнения), 35 - с применением колоносорбции (основная группа). Изучены данные 15 здоровых добровольцев.
Исследование влияния интраоперационного сорбционного диализа в сравнении с лаважем осуществлялось у 84 больных с острой толстокишечной непроходимостью вследствие рака. Основную группу составили 49 больных, которым был проведен интраоперационный толстокишечный сорбционный диализ. 35 больным был проведен интраоперационный лаваж толстой кишки (контрольная группа).
Экспериментальный раздел представлен: 1) стендовыми опытами (n = 21), проведенными с целью изучения влияния pH среды на интенсивность сорбции на лигносорбе различных компонентов содержимого желудочно-кишечного тракта; 2) опытами на 230 нелинейных половозрелых белых крысах для изучения возможности элиминации эндотоксинов из внутренних сред организма при использовании толстокишечного сорбционного диализа.
Основными методами исследования являлись методы клинического наблюдения. Их дополняли исследования: лабораторные, клинические, биохимические, морфологические, иммунологические, инструментальные. Сведения обо всех больных вносились в формализованную историю болезни. На ее основе данные вносились и обрабатывались с помощью современных систем обработки статистических данных. Достоверность различий считалась при р 1 (превалирование накопления ВНиСММ в крови над их содержанием в моче), третью - больные, К/М которых занимал промежуточное положение (от 0,57 до 1). Как показал анализ послеоперационных осложнений, наиболее адаптационно-устойчивыми в послеоперационном периоде оказались больные раком толстой кишки, имевшие показатель соотношения ВНиСММ крови и мочи > 0,57 и 1
Читайте также:

