Адренокортикальный рак акр iii стадии что это

-
6 минут на чтение

Адренокортикальный рак – злокачественное новообразование. Болезнь сопровождается повышенной гормональной активностью некоторых гормонов. В 50% прецедентов опухоль в надпочечниках является гормонально неактивной. Чаще всего такое новообразование возникает в преклонном возрасте, но прогрессирует оно быстрее, чем гормонально активные опухоли.
- Что собой представляет АКР
- Классификация
- Причины
- Симптомы
- Диагностика
- Лечение
- Прогноз
Что собой представляет АКР
Адренокоритикальный рак – это злокачественная опухоль, которая развивается из клеток коры надпочечников. Это очень редкая болезнь. Чаще всего ею страдают дети до 5 лет и взрослые от 45 лет. В 40% случаев болеют мужчины. Спровоцировать развитие опухоли может курение, а также приём гормональных противозачаточных средств.
Надпочечники – это парные железы, которые располагаются над верхним полюсом почек. Этот орган вырабатывает и поставляет в кровь гормоны, которые обеспечивают защиту внутренних систем путём создания воспалительного процесса. Благодаря им формируется реакция организма на любой возбудитель, в том числе и стресс. От работы надпочечников зависит артериальное давление, вторичные половые признаки. Этот орган связан с другими эндокринными железами.
Адренокортикальный рак развивается в поверхностном слое надпочечников, где происходит синтез многих гормонов. Опухоль влияет на выработку этих веществ. Гормоны продуцируются в неправильных количествах.
В ½ случаях клетки опухоли вырабатывает повышенное количество гормона кортизола, что приводит к появлению синдрома Иценко-Кушинга с типичными для такого состояния признаками.
- Онкоэндокринология
![]()
Наталья Геннадьевна Буцык- 29 ноября 2019 г.
Гиперпродукция андрогена, ещё одного гормона надпочечников, приводит к возникновению адрено-генитального синдрома. У взрослых чаще наблюдается сочетание гиперпродукции андрогена и кортизола. В 20% случаев синдром Кушинга и вирильный развивается изолировано.
Адренокортикальный рак характеризуется агрессивным течением. Заболевание встречается у 2-х человек на миллион населения. При небольшом очаге поражения и после радикального лечения долго прожить могут 70% заболевших.
При средних размерах опухоли пятилетняя выживаемость – 60%. При раке с метастазами пятилетний рубеж переживёт не более 10%.
Классификация
Новообразования могут быть доброкачественными и злокачественными. Эпителиальные опухоли коры надпочечников:
- аденома;
- карцинома.
Клиническая классификация злокачественного новообразования надпочечников:
- T1 – небольшие величины новообразования – до 5см;
- T2 – большая величина – больше 5см;
- T3 – любая величина новообразования с местным проникновением в окружающие ткани;
- T4 – любая величина с метастазированием в различные органы;
- N0 – лимфоузлы не увеличены;
- N1 – метастазы в лимфоузлы;
- N2 – поражение лимфоузлов других локализаций;
- M0 – нет отдаленного метастазирования;
- M1 – есть отдаленное метастазирование.
- Стадия 1 – T1/N0/M0.
- Стадия 2 – T2/N0/M0.
- Стадия 3 – T1/N1/M0, T2/N1/M0, T3/N0/M0.
- Стадия 4 – T4/N2/M0, T4/N2/M1.
Причины
АКР – редкое заболевание. Установить точные причины болезни затруднительно. Учёные выдвигают предположение, что развитие первичной опухоли из клеток коры надпочечников связано с наследственностью.
Вторичная опухоль возникает в результате проникновения в надпочечники метастаз из других органов.
Факторы, провоцирующие развитие онкопроцесса:
- генетическая предрасположенность (Беквита-Видемана, синдром Ли-Фраумени);
- плохая экологическая ситуация;
- вредные привычки;
- высокожировая диета;
- малоактивный образ жизни;
- аутоиммунные патологии;
- рак в других органах.
Надпочечники занимают 4 место по частоте метастазирования из других органов. Чаще всего в них проникает рак лёгких, молочных желез, реже – рак поджелудочной железы, почек, органов ЖКТ, меланома, семинома.
Симптомы
Адренокортикальный рак может никак себя не проявлять долгое время. Иногда опухоль находят при обследовании других органов брюшной полости.
Когда опухолевый процесс прогрессирует, больные жалуются на слабость, быструю утомляемость, отсутствие аппетита, тошноту, высокую температуру.
Постепенно развивается болевой синдром разнообразной интенсивности. Боль локализуется в верхних отделах живота и пояснице.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Адренокортикальный рак (АКР) – сравнительно редкое, но агрессивно протекающее заболевание, вопросы своевременной диагностики и лечения которого остаются до настоящего времени окончательно не решенными. Ежегодное выявление АКР, по данным зарубежной статистики, составляет 1–2 случая на 1 млн населения; распространенность не имеет какой-либо тенденции к увеличению, а доля АКР в структуре онкологической смертности не превышает 0,2% [1]. Женщины заболевают чаще мужчин, средний возраст больных составляет 50 лет, при этом отмечаются 2 возрастных пика заболеваемости: у детей до 15 лет (по некоторым данным, в первые 5 лет жизни) и у взрослых 40–60 лет [2].
Этиология и патогенез АКР неясны. К факторам, повышающим риск АКР, относят у женщин прием оральных контрацептивов, у мужчин – курение табака [3]. В большинстве случаев опухоль развивается спорадически, редко АКР ассоциируется с синдромами Беквита – Вайдемана, Ли – Фраумени, Гарднера, множественной эндокринной неоплазией I типа.
Основная проблема дооперационной диагностики АКР заключается в отсутствии четко сформулированных критериев этого заболевания. Клинические симптомы и данные лучевых методов диагностики позволяют лишь заподозрить АКР, притом что один из основных онкологических принципов – верификация диагноза на основании цито- или гистологического исследования биоптата опухоли до начала лечения в случаях АКР не соблюдается в связи с низкой информативностью исследования [4].
Клиническая симптоматика АКР определяется функциональной активностью, размером опухоли и степенью ее распространенности.
Гормонально-неактивный АКР на ранних стадиях протекает без специфических, присущих только этому заболеванию симптомов, что и является причиной его несвоевременного выявления. При прогрессировании опухолевого процесса пациенты предъявляют неспецифические жалобы на общую слабость, утомляемость, плохой аппетит, тошноту, снижение массы тела, лихорадку. Со временем развивается болевой синдром различной интенсивности с локализацией в верхних отделах живота и в пояснице, появляется пальпируемое новообразование в брюшной полости. Описано расширение вен семенного канатика как симптом АКР [6]. Также имеются и редкие наблюдения нефункционирующих карцином коры надпочечника, манифестирующих клиникой острого живота [7, 8].
Широкое внедрение в клиническую практику методов лучевой диагностики, таких как ультразвуковое исследование (УЗИ), мультиспектральная компьютерная томография (МСКТ), магнитно-резонансная томография, привело к резкому увеличению числа случайно выявленных опухолей надпочечников – инциденталом, среди которых доля АКР колеблется от 1,9 до 8% [9, 10].
Первичная лабораторная диагностика АКР заключается в выявлении гормональных нарушений, характерных для адреногиперкортицизма. Очень важно выявление субклинического гиперкортицизма (хотя и редкого при АКР), недооценка наличия которого связана с риском острой послеоперационной надпочечниковой недостаточности.
У больных гормонально-активным АКР мониторинг уровня соответствующих гормонов позволяет также оценивать эффективность лечения и в дальнейшем судить о течении заболевания. Так, Т.А. Бритвин и соавт. [6] у больных АКР с синдромом Кушинга после радикальной операции отмечали либо нормализацию уровня кортизола в крови и суточной экскреции его свободной фракции в моче, либо развитие надпочечниковой недостаточности. По данным этих авторов, в случаях рецидива опухоли или развития метастазов наблюдалась гиперкортизолемия, причем у некоторых больных она предшествовала появлению соответствующей клинической симптоматики синдрома Кушинга. С клинической точки зрения интерес представляют отдельные наблюдения АКР, в которых описан феномен изменения функциональной активности опухоли при ее прогрессии [11].
Наряду с исследованием уровня гормонов надпочечников и их предшественников в биологических жидкостях современная лабораторная диагностика располагает методами определения различных молекулярно-биологических факторов как для первичной диагностики новообразований, так и для мониторирования течения заболевания в процессе лечения или после завершения лечебной программы. И, несмотря на то, что применительно к АКР такие факторы достоверно не установлены, результаты отдельных исследований показали определенную эффективность некоторых из них, в частности фактора роста эндотелия сосудов [12, 13].
Методы лучевой диагностики на современном этапе имеют важнейшее значение для дооперационной верификации АКР. И если наличие прямых признаков злокачественности опухоли, таких как инвазия в окружающие органы, метастатическое поражение регионарных лимфоузлов, печени, легких, делает диагноз АКР практически очевидным, то их отсутствие ставит задачу по выявлению признаков, патогномоничных именно для этой опухоли.
В последние годы диагностические возможности УЗИ существенно возросли. В этой связи представляют интерес работы, в которых оценивалась информативность УЗИ с контрастным усилением в выявлении метастазов АКР в печени по сравнению с таким же показателем МСКТ, свидетельствующие о ее более высокой чувствительности и специфичности [15].
Еще одним из методов топической диагностики АКР является позитронно-эмиссионная томография (ПЭТ). Показано, что чувствительность ПЭТ с фтордезоксиглюкозой в отношении выявления АКР достигает 98,5%, специфичность – 92%, а выполнение исследования в режиме ПЭТ-КТ повышает специфичность до 98%. Отмечена высокая информативность ПЭТ и при выявлении рецидива и метастазов АКР [16], а также в оценке эффективности химиотерапии [17]. Для диагностики АКР с помощью ПЭТ предлагаются и другие радиофармпрепараты, например 11С-метомидат. Метомидат связывается с 11β-гидроксилазой надпочечников и таким образом позволяет уточнить органную принадлежность опухоли. Также данный метод может быть полезным для определения метастатических образований при АКР [18]. Несмотря на высокую точность ПЭТ, она имеет некоторые недостатки, которые связаны с ограниченной доступностью и высокой стоимостью исследования, а также со снижением точности при опухолях небольших размеров.
Ангиографические методики в настоящее время имеют ограниченное применение в диагностике АКР, что прежде всего связано с возможностью выполнения непрямой ангиографии при МСКТ с последующей 3D-реконструкцией. Гораздо большее клиническое значение имеют методики интервенционной ангиографии, направленные на эмболизацию питающих опухоль сосудов с целью предотвращения массивной кровопотери во время операции, а также химиоэмболизацию печеночных метастазов опухоли.
Как известно, лечебная тактика и прогноз при АКР зависят от степени распространенности опухолевого процесса, поэтому адекватное стадирование является необходимым условием при выборе лечебной программы и последующего диспансерного наблюдения. Для определения стадии АКР предложено несколько классификаций, наиболее применимыми из которых являются системы TNM (AJCC/UICC) и ENSAT, причем последней большинством специалистов отдается предпочтение как более клинически адаптированной и удобной. Следует отметить, что в 2014 г. была опубликована работа, авторы которой предложили усовершенствованный вариант классификации ENSAT, использование которого позволило выявить различия в показателях общей выживаемости не только между II–III, III–IV, но и между I–II стадиями АКР [19].
Единственным методом потенциально радикального лечения АКР является хирургический, причем наблюдаются максимальная 5-летняя выживаемость (61,7%) у оперированных больных с I–II стадией (ENSAT), а также улучшение 5-летней выживаемости у больных, имеющих местные и отдаленные метастазы (39,1 и 6,7% соответственно) [20]. Предпочтительной считается адреналэктомия единым блоком с опухолью и окружающей жировой клетчаткой. В опухолевый процесс могут быть вовлечены окружающие органы и сосуды: почки, печень, селезенка, поджелудочная железа, ободочная кишка, нижняя полая вена и аорта, соответственно, для радикального удаления опухоли могут быть необходимы их резекция, пластика или удаление. Сохранение целостности капсулы опухоли при ее удалении имеет принципиальное значение для предупреждения рецидива опухоли [21]. Некоторые авторы считают обязательным удаление лимфатических узлов паранефрального, парааортального, паракавального коллекторов. Преимущества лимфаденэктомии при АКР продемонстрированы в исследовании J. Reibetanz et al. [22], в котором доказано статистически значимое улучшение безрецидивной выживаемости и АКР-ассоциированной смертности у больных с выполненной Ro-резекцией.
Гистологическая верификация АКР основывается на выявлении макро- и микроскопических критериев малигнизации. В настоящее время наиболее распространена панель гистологических критериев при использовании световой микроскопии, предложенная в 1984 г. L.M. Weiss. Каждый из 9 критериев оценивается в 1 балл: 1) высокий ядерный индекс, 2) митотическая активность (более 5% на 50 репрезентативных полей зрения), 3) атипичные фигуры митоза, 4) эозинофилия цитоплазмы опухолевых клеток (более 75% клеток в опухоли), 5) диффузная архитектоника опухоли (33% ткани опухоли), 6) некрозы, 7) опухолевая венозная инвазия, 8) опухолевая синусоидальная инвазия, 9) инвазия капсулы. При наборе 4 и более баллов верифицируется АКР. В 2002 г. система L.M. Weiss была модифицирована, при этом предложено учитывать 5 критериев (митотическая активность (более 5% на 50 репрезентативных полей зрения) – 2 балла, атипичные фигуры митоза – 1 балл, эозинофилия цитоплазмы опухолевых клеток (более 75% клеток в опухоли) – 2 балла, некрозы – 1 балл, инвазия капсулы опухоли – 1 балл), а АКР верифицируется при наборе 3 и более баллов.
Несмотря на высокую чувствительность шкалы L.M. Weiss, многими исследователями признается необходимость разработки более четких морфологических критериев злокачественности опухолей надпочечников, а также биомаркеров, которые могут использоваться в массовых анализах [1]. Для этих целей применяются цитогенетические, молекулярные методы, а также иммуногистохимическое исследование, которое имеет ведущее значение. Определяется экспрессия таких маркеров, как топоизомераза II-α, Ki-67, р53, E-cadherin, HER-2, p27, белки семейства IGF, SMAD4, SF-1, CYP2W1, кальретинин, цитокератины 8 и 18, виментин, ингибин А, мелан А, SRC-1, протеин S-100, Pax8, хромогранин А, рецепторы эстрогена [1, 24–28].
В исследовании С. Wang et al. [1] описано применение в комплексе генетического и иммуногистохимического методов (гибридизация): определение экспрессии микроРНК (miR483-3p) и иммуногистохимических маркеров (IGF-2, SMAD4, Ki-67), а также оценка их взаимодействия для разработки теоретических основ дифференциальной диагностики, прогностической оценки и таргетной молекулярной терапии. МикроРНК являются эндогенными, некодирующими РНК, состоящими приблизительно из 22 нуклеотидов, которые регулируют экспрессию гена, контролируя передачу информации матричной РНК. Сообщается, что повышенная экспрессия miR483-3p наблюдается при раке молочной железы, толстой кишки, печени, АКР [27, 29]. SMAD4 – медиаторная молекула в TGF-B сигнальном пути, который контролирует пролиферацию, клеточную дифференцировку и другие функции в большинстве клеток. В некоторых исследованиях показано, что ген, кодирующий SMAD4, является мишенью для miR483-3p. MiR483 закодирована в гене IGF2. В нескольких исследованиях выявлено, что нарушение регуляции экспрессии IGF2 является фактором развития АКР [29]. В работе С. Wang et al. [1], включившей 25 случаев АКР и 25 доброкачественных опухолей, показана повышенная экспрессия miR483-3p при АКР – 68% (17 из 25). Экспрессия miR483-3p была повышена только в 12% доброкачественных опухолей (3 из 25) (р 14 мг/л) продемонстрировано в многоцентровом европейском исследовании ADJUVO [29].
Лучевая терапия применяется для послеоперационного или паллиативного лечения метастазов АКР в кости и центральную нервную систему [20, 21].
Изучение онкогенеза АКР улучшило понимание молекулярных и генетических механизмов инициации и прогрессирования опухоли. Выявлены потенциальные биомаркеры для ранней диагностики, улучшения прогнозирования заболевания, разработаны механизмы воздействия новых лекарственных средств. Выявлено нарушение регуляции более чем 500 генов при АКР в сравнении с доброкачественными образованиями надпочечника. Среди них ген, кодирующий IGF-2, нарушение его экспрессии выявляется в 90% случаев АКР. Также выявлена повышенная экспрессия IGF-1R – рецептора IGF2. Понимание этого патологического пути позволило разработать антагонисты IGF-1R (figitumumab, cixutumumab), провести клинические испытания, в которых доказано подавление клеточной опухолевой пролиферации и роста опухоли [29, 30]. Разрабатываются также препараты, действующие на другие пути онкогенеза АКР: Wnt/β–catenin pathway, ингибиторы рецепторов тирозинкиназы, рецепторов эстрогена, антагонисты mTOR и др.
Только для зарегистрированных пользователей
Адренокортикальный рак (АКР) в 30-50% случаев не сопровождается выработкой гормонов.
В случае значительной продукции гормонов могут возникать следующие симптомы: избыточный вес, задержка жидкости в организме, раннее половое созревание у детей, рост волос на лице и теле у женщин.
Иногда такая опухоль достигает больших размеров, сдавливая органы брюшной полости. Обычно злокачественные опухоли надпочечника (НП) превосходят по размерам аденому.
Нужно помнить о том, что рак легкого, молочной железы и некоторые другие злокачественные новообразования часто метастазируют в НП.
Адренокортикальный рак — злокачественное новообразование, развивающееся из клеток коркового слоя НП.
Эпидемиология
Адренокортикальный рак является редкой опухолью как у взрослых, так и у детей. Истинная частота этой формы рака неизвестна. В то же время аденомы НП малых размеров довольно часто (5%) обнаруживаются у людей среднего и пожилого возраста при компьютерной или магнитно-резонансной томографии, выполненных во время обследования по иным причинам, АКР у детей составляет приблизительно 0,5% всех злокачественных опухолей и встречается с частотой 1 на 500 тыс. детей.
Заболеваемость АКР в США составляет около 0,5-2 случаев на 1 млн человек, ежегодно регистрируют 75-115 новых случаев данной патологии, В структуре онкологической заболеваемости АКР занимает менее 0,05% всех злокачественных эндокринных опухолей. В России точная заболеваемость данной патологией неизвестна.
Пик заболеваемости АКР приходится на два возрастных периода - до 5 лет и 40-50 лет. Чаще болеют женщины (4:3), кроме того, АКР, сопровождающийся гиперсекрецией гормонов, также чаще встречается у женщин (7:3), чем у мужчин (3:2). Билатеральное поражение НП наблюдается у 2-10% больных АКР.
Классификация
Для оценки злокачественности опухоли НП Weiss и соавт. предложена классификация, в которой следует учитывать следующие морфологические признаки:
1) гиперхромные ядра клеток;
2) количество митозов в ядрах клеток >5 на 50 полей высокого разрешения;
3) наличие атипичных митозов;
4) наличие в опухоли
Наиболее часто приходится дифференцировать опухоль от солитарной кисты почки, тем более что оба заболевания иногда сочетаются. В дифференциальной диагностике опухоли и кисты почки может оказать помощь нефротомография, при которой опухоль почки контрастируется, а киста отличается пониженной контрастн.
При осмотре и пальпации выявляются обычно опухоли почки в далеко зашедшей стадии. О большой опухоли почки свидетельствует деформация живота. Осмотр может выявить варикоцеле, а при обструкции нижней полой вены — расширение вен передней брюшной стенки, отечность нижних конечностей.
Поскольку опухоли почечной паренхимы и опухоли лоханки во многом отличаются как по структуре, так и по путям распространения и требуют различных оперативных методов лечения, оправданно их выделение в отдельные группы. В настоящее время принята следующая классификация опухолей почки.
Опухолевые заболевания почки разделяются на доброкачественные и злокачественные. Почечно-клеточный рак возникает из проксимального изогнутого канальца нефрона, является самым частым видом опухоли почки и составляет около 3% в структуре всех злокачественных заболеваний. Частота заболеваемости ежегодн.
Эпителиальные опухоли почечной лоханки и мочеточника представляют собой особую группу новообразований, значительно отличающихся от опухолей паренхимы почки как по клиническому течению, так и по методам лечения. Опухоли лоханки встречаются гораздо реже, чем опухоли почечной паренхимы, составляя приме.
Опухоль Вильмса встречается у детей любого возраста, начиная с новорожденного, но наиболее часто — в возрасте 2—7 лет. Девочки и мальчики заболевают с одинаковой частотой. У 5% больных опухоль Вильмса бывает двусторонней, как правило, у детей раннего возраста. Нередко у ребенка диагностируется.
В диагностике заболеваний почек, предстательной железы, яичка и его придатка, а также семенного пузырька нередко решающее значение приобретает пункционная биопсия. Пункционная биопсия почки может быть открытой и закрытой. Открытую биопсию почки производят при ее обнажении во время операции или специ.
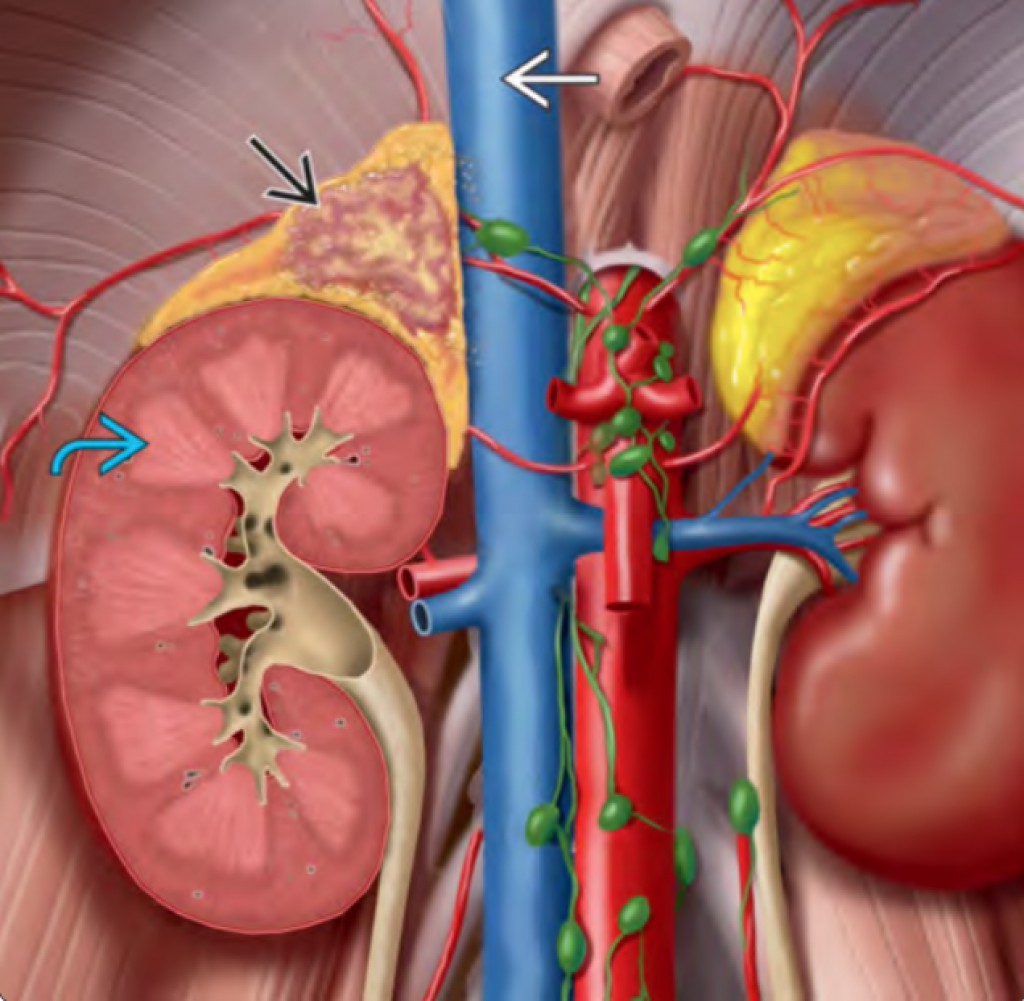
Адренокортикальный рак (англ. adrenocortical carcinoma) — рак коры надпочечника, редкая злокачественная опухоль, исходящая из коркового слоя надпочечников, характеризующаяся агрессивностью клинического течения и, до настоящего момента, неблагоприятным лечебным прогнозом. Адренокортикальный рак может быть гормонально-активным, являясь причиной синдрома Кушинга (в том числе субклинического), и/или вирильного синдрома, или может быть гормонально неактивным и проявляться общими, нехарактерными симптомами. Часть случаев адренокортикального рака может выявляться как инсиденталома надпочечника.
Морфологическая диагностика должна включать одну из принятых систем балльной оценки злокачественного потенциала опухоли и ее органной принадлежности. Морфологическая диагностика АКР основывается на изучении и оценке микроскопических критериев, с балльной оценкой и высчитыванием индекса по vanSlooten или Weiss. В настоящее время к широкому применению рекомендованы критерии Weiss, как наиболее информативные и простые для повсеместного использования. По системе Weiss оценивают 9 микроскопических критериев, любой из них оценивается в 1 балл:
При наборе 3 баллов и более по Weiss выставляется диагноз адренокортикального рака. Для оценки злокачественного потенциала опухоли применяются маркеры пролифера- ции, наиболее часто исследуют индекс Ki-67.
Для стадирования АКР долгое время применялись авторские классификации (MacFarlane,Sullivan, Icard, Lee). Классификация адренокортикального рака по UICC впервые издана в 2004г.
- Тх - первичная опухоль не может быть оценена
- Т0 - отсутствуют данные о первичной опухоли
- Т1- опухоль не более 5 см в наибольшем измерении без инвазии за пределы надпочечника
- Т2 - опухоль более 5 см без инвазии за пределы надпочечника
- Т3 - опухоль любого размера с очаговой инвазией, но без прорастания в прилежащие органы
- Т4 - опухоль любого размера с инвазией в смежные органы (почка, печень, диафрагма, поджелудочная железа, крупные сосуды); опухолевый тромбоз почечной вены или нижней полой вены
- Nx - регионарные лимфоузлы не могут быть оценены
- N0 - регионарные лимфоузлы не поражены
- N1 - метастазы в регионарные лимфоузлы
- M0 - Отдаленных метастазов нет
- M1 - Есть отдаленные метастазы
Стадии и прогностические группы согласно AJCC.
В некоторых учреждениях также используют классификацию (группировка по стадиям) по ENSAT (European Network for the Study of Adrenal Tumors) – европейской сети по изучению опухолей надпочечников (В).
Стадия по ENSAT
- I T1N0M0 Размер 5 см
- III T(1,2)N(1)M(0) T(3,4)N(0,1)M0 - Метастазы в лимфоузлах, опухолевая инфильтрация в соседние органы и почку и/или тромбоз нижней полой вены
- IV T(1-4)N(1-2)M1 - Отдаленные метастазы
Согласно классификации ENSAT к IV стадии относят только случаи с отдаленными метастазами. Местнораспространенные опухоли, в том числе с опухолевым тромбозом, относятся к III стадии.
Распределение метастазов по органам при первичной карциноме надпочечников согласно данным Bilimoria KY et al: Adrenocortical carcinoma in the United States: treatment utilization and prognostic factors. Cancer. 113(11):3130-6, 2008.
- Печень - 11%
- Легкое 9%
- Кости 3%
- Дистантные лимфатические узлы 2%
- Брюшина 1%
- ЦНС
Адренокортикальный рак (АКР) – редкое заболевание, характеризующееся поздним сроком выявления, быстрым прогрессированием и, при несвоевременном и неполном лечении, неблагоприятным лечебным прогнозом. АКР примерно в половине наблюдений может сопровождаться повышенным выделением в кровь гормонов надпочечников.
АКР – одна из самых редких и, следовательно, плохо поддающаяся изучению, опухолей человека. Ежегодно выявляют 0,5-2 случая АКР на миллион населения. Женщины болеют чаще мужчин, средний возраст больных составляет 46 лет, при этом отмечаются 2 возрастных пика заболеваемости: у детей до 15 лет и у взрослых 40-60 лет.
По данным Европейского Комитета по Орфанным Лекарственным Препаратам (Committee for Orphan Medicinal Products EMA) распространённость АКР в Европе составляет 1 на 100 000 человек населения, что позволяет отнести данное заболе- вание к категории редких (орфанных) заболеваний.
В связи с отсутствием национального регистра по данному заболеванию, количе- ство больных с АКР в России точно не известно и цифры противоречивы. Эксперты в этой области говорят о 150-200 больных. С другой стороны, основываясь на мировых данных по выявляемости и распространенности, можно предположить появление от 71 до 286 новых пациентов в год, при общем количестве пациентов около 1000 человек.
Причины появления заболевания
Причины появления и развития АКР неясны. В большинстве случаев опухоль развивается спонтанно без каких-либо выявленных причин. Достаточно редко (до 15% случаев и особенно у детей) возможная причина – это врожденный генетический дефект. АКР описан, как одно из проявлений при синдромах Линча, Беквита-Вайдемана, Ли-Фраумени, Гарднера, множественной эндокринной неоплазии I типа, при семейном аденоматозном полипозе. Четкой связи между возникновением АКР и образом жизни или внешними факторами ученые не отмечают. Некоторые исследователи к факторам, повышающим риск АКР, относят у женщин прием оральных контрацептивов, у мужчин – курение табака.
Проявление заболевания, симптомы
Гормонально-активные опухоли наблюдаются у 60% взрослых. В данном случае опухоль в повышенном количестве выделяет в кровь кортикостероиды (гормоны коры надпочечников), а именно:
- глюкокортикоиды (кортизол и кортизон);
- минералокортикоиды (альдостерон, кортикостерон и дезоксикортикостерон);
- половые гормоны (андрогены и эстрогены).
У детей гормональная активность АКР встречается чаще, чем у взрослых, – в 90% случаев. Большинство опухолей изолированно секретирует кортизол (55%) или андрогены в комбинации с кортизолом (30%).
Проявления АКР крайне разнообразны и связаны со следующими факторами:
- развитием опухолевого процесса (жалобы на общую слабость, утомляемость, плохой аппетит, тошноту, снижение массы тела), может повышаться температура тела вследствие сопутствующего распада опухоли;
- наличием образования в брюшной полости (боль в животе или спине, ощущение переполнения в животе, наличие объемного образования в брюшной полости, определяемого врачом или самостоятельно пациентом при ощупывании живота);
- повышенной продукцией гормонов:
- кортизола (общая слабость, головные боли, ожирение, с типичным отложением жировой клетчатки в области лица, шеи, груди, живота. Лицо при этом выглядит округлым, лунообразным. На щеках появляется пурпурный румянец. Руки и ноги наоборот становятся тонкими из-за уменьшения массы мышц. На коже появляются угревые высыпания. Раны и порезы заживают медленно. Возникают боли в костях и склонность к переломам, бесплодие, повышение артериального давления и др.);
- альдостерона (повышение артериального давления, слабость мышц вследствие потери калия);
- тестостерона (рост нежелательных волос на теле, понижение тембра голоса, увеличение клитора у женщин, повышение жирности и нечистота кожи);
- эстрогенов (увеличение грудных желез у мужчин, импотенция, маточные кровотечения у женщин в постменопаузе).
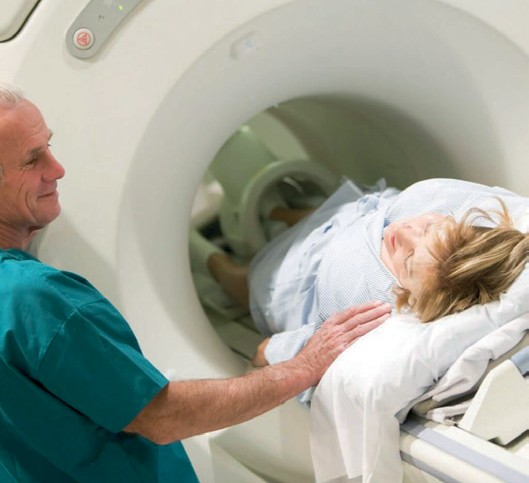
Широкое внедрение в клиническую практику методов лучевой диагностики, таких как ультразвуковое исследование (УЗИ), мультиспиральная компьютерная томография (МСКТ), магнитно-резонансная томография (МРТ), привело к резкому увеличению числа случайно выявленных опухолей надпочечников. Случайно выявленная опухоль надпочечника может оказаться как гормонально-неактивной, так и активно производить различные гормоны (смотри выше); исходить из различных частей надпочечника, быть злокачественной или доброкачественной. Среди всех случайно выявленных опухолей надпочечника АКР встречается только в 8% случаев.
При подозрении на АКР проводится лабораторная диагностика, которая заклю- чается в выявлении гормональных нарушений, характерных для гормонально-активного АКР. Для подтверждения/исключения гормональной активности опухоли рекомендованы следующие методы лабораторной диагностики:
- определение кортизола в ранние утренние часы на фоне подавляющего теста с 1 мг дексаметазона;
- при отсутствии физиологического подавления уровня кортизола – определение адренокортикотропного гормона в утренние часы;
- всем пациентам с выявленной опухолью надпо- чечника для исключения другой опасной опухоли – феохромоцитомы, рекомендовано определение норметанефрина и метанефрина в суточной моче или плазме;
- при наличии у больного с опухолью надпочечника артериальной гипертензии рекомендовано определение соотношения между уровнем альдостерона и активностью ренина плазмы для исключения первичного гиперальдостеронизма;
- при подозрении на изолированную или сочетанную (с гиперкортицизмом) опухолевую гиперпродукцию половых гормонов рекомендовано определение стероидных гормонов сыворотки крови (дегидроэпиандростерон-сульфат, 17-оксипрогестерон, андростендион, тестостерон, 17-β-эстрадиол у мужчин и женщин в менопаузе).
Методы лучевой диагностики на современном этапе имеют важнейшее значение для дооперационного подтверждения диагноза АКР. И если наличие прямых при- знаков злокачественности опухоли, таких как прорастание в окружающие орга- ны, метастатическое поражение лимфоузлов, печени, легких, делает диагноз АКР практически очевидным, то их отсутствие ставит задачу по выявлению признаков, характерных именно для этой опухоли.
Ультразвуковое исследование (УЗИ) используется довольно часто в качестве первичного диагностического метода. УЗИ очень хорошо опре- деляет опухоль, но, к сожалению, не всегда может точно определить происхождение этой опухоли. УЗИ может быть использовано для первичной диагностики опухолей надпочечников в случае невозможности выполнения компьютерной томографии.
Магнитно-резонансная томография (МРТ) рекомендована для первичной диагностики опухолей надпочечников, а также для исключения метастазов в головном мозге. МРТ обладает высокой чувствительностью в выявлении опухолей надпочечников, оценки состояния опухоли, в том числе поражения соседних органов. Однако точность данного метода пока ниже, чем КТ.
Остеосцинтиграфия рекомендована при подозрении на метастазы костей скелета.
Позитронно-эмиссионная томография (ПЭТ) с дезоксифторглюкозой (ФДГ) рекомендуется для определения стадии и распространенности процесса, а также в качестве диагностического метода, позволяющего определить злока- чественный потенциал при небольших размерах опухоли (до 4 см).
Пункционная биопсия в случае АКР не имеет доказанных преимуществ, обладает низкой чувствительностью, недостаточной информативностью и высокой вероят- ностью осложнений, поэтому ее проведение не рекомендуется.
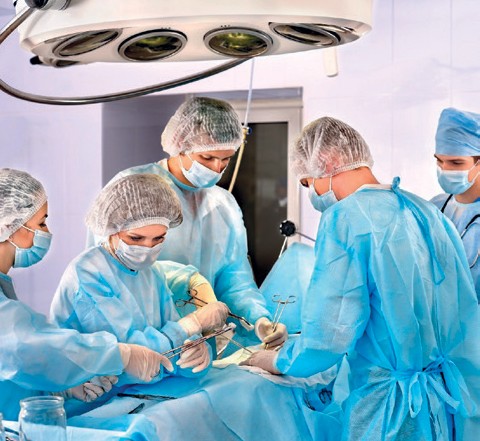
Диагностика и лечение рака надпочечников должно происходить с участием эндокринолога, онколога и хирурга в специализированном отделении.
1. Хирургическое лечение
Традиционно хирургический метод является основным в лечении больных АКР. Правильно выполненная, с соблюдением всех онкологических принципов операция, может излечить или по крайней мере привести к длительной ремиссии у многих больных с локализованным АКР. Оперативное лечение рекомендовано провести в кратчайшие сроки после проведения адекватной диагностики в виду быстрого роста опухоли и распространения метастазов. Выполнение операций с попыткой сохранения ткани надпочечника недопустимо. Единственным возможным вариантом полного излечения при АКР в настоящее время является полное хирургическое удаление опухоли сразу после ее обнаружения. Предпочтительной считается удаление надпочечника единым блоком с опухолью и окружающей жировой клетчаткой. В опухолевый процесс могут быть вовлечены окружающие органы и сосуды: почки, печень, селезенка, поджелудочная железа, ободочная кишка, нижняя полая вена и аорта, соответственно, для полного удаления опухоли могут быть необходимы их частичное или полное удаление во время операции. Сохранение целостности капсулы опухоли при ее удалении имеет принципиальное значение для предупреждения повторного возникновения опухоли.
Эндоскопическое удаление опухоли при АКР рекомен- довано выполнять только в учреждении, обладающем достаточным опытом подобных вмешательств. Такой малотравматичный вариант удаления ограничен I и II стадиями заболевания. При большей распространенности опухоли эндоскопическая операция противопоказана, так как возможность оценки поражения соседних органов и их удаления очень ограничена. Основная проблема удаления опухоли при помощи эндоскопа – высокая частота распространения опухоли по брюшине после операции, вследствие интраоперационного повреждения капсулы опухоли. Часть экспертов придерживается мнения, что при размере опухоли более 5 см и/или подозрении на злокачественность опухоли по результатам предоперационного обследования – вероятность распространения опухоли при нарушении капсулы значительно выше при эндоскопических технологиях, чем при открытой операции.
5-летняя выживаемость при АКР после радикального хирургического лечения достаточно высока. Рецидивы после операции бывают как местными (в зоне удаления опухоли), так и в виде отдаленных метастазов. Местный рецидив большей частью зависит от особенностей операции: когда опухоль удаляют с нарушением ее целостности, резко повышается риск рецидива. При возникновении рецидива или метастазов хирургический метод лечения также является основным.
Лекарственная терапия рака коры надпочечника достаточно сложна, и в настоящее время не считается безнадежной, как всего лишь пару десятилетий назад. Разработаны и внедрены в клиническую практику достаточно эффективные специализированные препараты, которые подавляют рост раковых клеток. Эти препараты эффективны у многих пациентов, известны случаи, хотя и редкие, полного излечения. Как правило, эти препараты должны правильно дозироваться под контролем уровня препарата в крови при помощи лабораторных исследований. При достижении необходимого уровня препарата в крови достаточно часто наблюдаются побочные эффекты. Интенсивность и выраженность побочных эффектов нарастает с накоплением дозы, но эти проявления исчезают с отменой препарата.
При хирургическом лечении опухоли у части больных рекомендуется вспомогательная дополняющая (адъювантная) химиотерапия. При невозможности хирургического лечения, наличии распространённого метастатического процесса после удаления первичной опухоли, при быстром прогрессировании заболевания рекомендуется назначать комбинированную химиотерапию несколькими препаратами по определенным схемам. Пациенты с небольшими опухолями и медленной прогрессией могут в качестве первичного лечения находиться на терапии одним специализированным препаратом в комбинации с радиологическими методами.
3. Другие методы лечения
Таргетная терапия в настоящее время не рекомендована для лечения больных распространенным АКР, т.к. в ряде исследований возможности применения препаратов этого класса при распространенных формах АКР были продемонстрированы неудовлетворительные результаты.
Дистанционная лучевая терапия (ДЛТ) рекомендована в качестве паллиативной терапии при метастазах АКР в кости и центральную нервную систему.
Без хирургического лечения прогноз неблагоприятный. Прогноз в основном зависит от стадии заболевания, адекватности хирургического лечения и последую- щего назначения специализированных препаратов химиотерапии.
В настоящее время в России наибольшим опытом лечения адренокортикального рака обладают следующие медицинские центры:
Адрес: 115478, г. Москва, Каширское шоссе 23.
Адрес: 117036, г. Москва, ул. Дмитрия Ульянова, д. 11.
Московский научно-исследовательский онкологический институт (МНИОИ) имени П.А. Герцена
Адрес: 125284, Москва, 2-й Боткинский пр., д. 3.
Отделение эндокринной хирургии Северо-Западного центра эндокринологии
Адрес: 190103 г. Санкт-Петербург, наб. реки Фонтанки, д. 154 (на базе Клиники высоких медицинских технологий им. Н.И. Пирогова Санкт-Петербургского государственного университета).
Научные исследования адренокортикального рака в России не проводятся, наиболее известными центрами изучения АКР на настоящий момент являются Мичиганский университет, а также Национальный институт онкологии (США) и Вюрцбургский университет в Германии.
Врачи на основании клинических симптомов могут заподозрить болезнь. Затем проводятся лабораторные тесты и инструментальное исследование. СГХС обычно первоначально распознается по аномально высоким уровням ХС ЛПНП, определяемым по данным теста на холестерин. Кроме того, для подтверждения диагноза может быть выполнено генетическое тестирование. В анализе крови (развернутая липидограма), как правило, выявляют: повышение уровня общего холестерина, липопротеидов низкой плотности (ЛПНП), нормальный уровень липопротеидов высокой плотности (ЛПВП) и триглицеридов.

Семьям очень важно посетить врача генетика. Лечащие врачи не всегда имеют возможность поговорить с семьей и рассказать о всех рисках и возможностях, которые может предоставить современная генетика. У врача генетика можно узнать риск рождения больного ребенка в данной семье, пройти обследование родственникам, если это необходимо.
Где в России занимаются диагностикой и лечением можно прочитать в разделе КОНТАКТЫ
Читайте также:


