Современные возможности диагностики рака молочной железы
Представлена обзорная информация о современных методах диагностики заболеваний молочных желез и возможных диагностических критериях рака молочной железы.
Survey information about the modern methods of diagnostics of mammary glands diseases and possible diagnostic criteria of breast cancer were represented.
Актуальность проблемы заболеваний молочных желез обусловлена прежде всего неуклонным ростом этой патологии во всем мире [5, 7]. Так, в популяции нераковые заболевания молочных желез встречаются у 30–70% женщин, а при одновременно имеющих место гинекологических заболеваниях их частота возрастает до 76–97,8% [7]. В России ежегодно выявляется более 34 000 новых случаев рака молочных желез, при этом отмечается значительное снижение возраста заболевших. У 25% женщин до 30 лет и у 60% после 40 лет диагностируются дисгормональные заболевания молочных желез (мастопатии) [3]. Несмотря на то, что мастопатии не являются облигатным предраком, рак молочной железы встречается в 3–5 раз чаще на фоне диффузных дисгормональных доброкачественных заболеваний молочных желез и в 30–40 раз чаще при узловых формах мастопатии с явлениями пролиферации эпителия молочных желез [3]. В связи с этим значительно возрос интерес к доброкачественным заболеваниям, а снижение заболеваемости мастопатией — реальный путь к снижению частоты рака молочной железы. В целом рак молочной железы не является предметом изучения и лечения врачей акушеров-гинекологов, но к ним часто обращаются женщины с проблемами, напрямую не связанными с содержанием специальности, в том числе и с проблемами, касающимися молочных желез. Поэтому акушеры-гинекологи могут существенно улучшить работу по сохранению здоровья женщины при экстрагенитальной патологии и при некоторых формах онкозаболеваний, в частности, при раке молочной железы. Несомненно, приоритетными для гинекологов являются вопросы диагностики и лечения доброкачественных заболеваний молочных желез. Поскольку молочные железы являются неотъемлемой частью репродуктивной системы женщины, решение проблемы ее оздоровления невозможно без наблюдения и исследования молочных желез, что несомненно должно входить в круг обязанностей акушеров-гинекологов. Выявление диффузной и очаговой патологии молочных желез и правильная трактовка полученных результатов обследования позволяют своевременно направить женщин на комплексное обследование и сориентироваться в правильном выборе метода лечения.
Традиционно в России и ряде других стран заболеваниями молочных желез занимаются в основном хирурги, онкологи и маммологи. В связи с этим акушеры-гинекологи не могли уделять должного внимания обследованию и лечению молочных желез в режиме скрининга (как это, например, проводится при заболеваниях шейки матки) [5, 7]. А без их участия врачами вышеназванных специальностей зачастую недооценивается весь спектр функциональных и органических нарушений репродуктивной системы в целом [6, 7]. Кроме того, следует отметить, что низкая выявляемость заболеваний молочных желез на ранних стадиях зачастую обусловлена недостатком знаний в области клинической маммологии у врачей акушеров-гинекологов, так как именно данная категория врачей является наиболее часто посещаемой среди женщин. При профилактическом осмотре акушером-гинекологом состояние молочных желез в схему осмотра и сбора анамнеза пациентки часто не включается. Вышеперечисленное свидетельствует о том, что ранняя диагностика патологии молочной железы представляется затруднительной. Важной задачей является организация взаимодействий врачей гинекологов и онкологов-маммологов. Участие врачей первичного звена в направлении женского населения на маммологический скрининг является важным инструментом снижения смертности от рака молочной железы.
Цель нашей статьи — дать краткую обзорную информацию о современных методах диагностики заболеваний молочных желез и возможных диагностических критериях рака молочной железы.
Доступность молочных желез для обследования и кажущаяся простота диагностики часто приводят к неправильной интерпретации результатов клинического исследования, которое зачастую проводится малоподготовленными в этом вопросе специалистами. Все это ведет как к гипо-, так и к гипердиагностике.
Поэтому мануальное обследование должно дополняться комплексным рентгенологическим, ультразвуковым (УЗИ), радиотермометрией (РТМ-диагностика), электроимпедансной маммографией (ЭИМ), другими видами инструментальных исследований.
Основным на сегодняшний день методом объективной оценки состояния молочных желез является рентгенологическая маммография. Эта методика рентгенологического исследования позволяет своевременно распознать патологические изменения в молочных железах в 95–97% случаев [8]. Именно это качество в отличие от других методов диагностики позволяет рассматривать маммографию как ведущий метод скрининга. В настоящее время во всем мире общепринято (ВОЗ, 1984) начиная с 40 лет проводить маммографическое исследование 1 раз в 2 года (при отсутствии показаний для более частого обследования), после 50 лет — 1 раз в год. Исключением являются женщины до 35 лет, кормящие, беременные женщины и подростки, которым маммография противопоказана.
Маммография — это рентгенография молочной железы без применения контрастных веществ. Метод простой, безопасный для обследуемых, отличается высокой диагностической эффективностью.
Маммографию проводят в двух проекциях (прямой — краниокаудальной и боковой) на 5–10 день менструального цикла, когда паренхима молочной железы менее отечна и болезненна, а при отсутствии менструаций — в любой день. Также можно использовать дополнительную боковую проекцию с медиолатеральным ходом луча (косая проекция). На боковых снимках при правильной укладке должны визуализироваться частично грудная мышца, ретромаммарная клетчатка, переходная складка. В прямой проекции — сосок, выведенный на контур железы, все структурные элементы молочной железы, в 20–30% — грудная мышца.
При необходимости уточнения состояния определенного участка молочной железы необходимо проводить прицельную рентгенографию с помощью специальных тубусов различной площади. Это лучше отграничивает патологический участок, а использование дозированной компрессии повышает четкость изображения. С помощью прицельных рентгенограмм удается вывести опухоль в край железы. При этом она выявляется более отчетливо, лучше определяется лимфатическая дорожка и состояние кожи в прилегающих участках. Прицельные снимки позволяют избежать ошибок, обусловленных проекционными эффектами суммации теней. В ряде случаев целесообразно использовать прицельную рентгенографию с прямым увеличением рентгеновского изображения.
Рентгеновская картина молочной железы у каждой женщины индивидуальна. Важно ориентироваться врачам первичного звена в признаках злокачественности при описании маммограмм. При маммографии различают первичные и вторичные признаки злокачественности.
К вторичным (косвенным) рентгенологическим признакам рака молочной железы относят симптомы со стороны кожи, соска, окружающей ткани молочной железы, усиленная васкуляризация и т. д.
Несмотря на эффективность рентгенологического метода, у ряда больных разрешающая способность маммографии резко снижается: при выраженных диффузных формах мастопатии, у молодых пациенток с плотными молочными железами, при наличии имплантатов, выраженных воспалительных изменениях, отеке железы и фоновых заболеваниях типа фиброаденоматоза. В этом случае на помощь приходит УЗИ молочных желез.
Основные преимущества маммографии, используемые при диагностике заболеваний молочной железы: возможность получения позиционного изображения молочной железы, высокая информативность при обследовании, возможность визуализации непальпируемых образований, возможность сравнительного анализа снимков в динамике. Недостатки метода, ограничивающие применение: дозовая нагрузка, хотя она и ничтожно мала; в 1,8–6% случаев по данным литературы имеет место рентгенонегативный рак. По данным большинства авторов процент достоверности маммографического исследования в диагностике рака составляет от 75% до 95%. Достоинства новой технологии не ограничиваются только клиническими аспектами. Появление цифровых приемников изображения позволило методу маммографии развиваться в контексте фундаментальных изменений, происходящих во всех разделах медицинской визуализации и в самой системе организации медицинской службы.
По общепринятому мнению, УЗИ является основным методом диагностики заболеваний молочных желез у женщин до 35–40 лет, при беременности, лактации, а в более позднем возрасте предпочтение следует отдавать рентгенологической маммографии. Ультразвуковая диагностика постоянно наращивает свой потенциал благодаря совершенствованию уже имеющихся и разработке новых методик диагностики. Сканирование выполняется на ультразвуковых аппаратах линейным датчиком с частотой 7,5–10 МГц при коэффициенте увеличения изображения 1,5, с использованием иммерсии — наличия слоя геля на соприкасающихся поверхностях кожи и датчика — для уменьшения содержания между ними воздуха.
Преимуществами ультразвуковых исследований молочных желез являются: безопасность в плане дозовой нагрузки, что позволяет обследовать беременных и кормящих; высокая разрешающая способность, что важно при плотном фоне молочной железы у молодых женщин (возможность визуализации рентгенонегативных опухолей, образований, расположенных вблизи грудной стенки); дифференциальная диагностика солидного и полостного образования (практически 100% диагностика кист любого размера); оценка состояния силиконовых имплантантов молочных желез, особенно при их разрывах и утечке содержимого; обследование молочных желез в острый период травмы или воспаления; визуализация регионарных лимфатических узлов; проведение прицельных пункционных биопсий под объективным визуальным контролем пальпируемых и непальпируемых образований в молочной железе; многократное динамическое исследование в процессе лечения.
Несмотря на все достоинства УЗИ молочных желез, практические врачи в большинстве случаев при назначении лечения пациенткам любых возрастных групп ориентируются в основном на данные рентгеновской маммографии. Недоверие к УЗИ молочных желез связано с тем, что молочная железа является одним из наиболее трудных объектов для ультразвуковой диагностики, так как соотношение составляющих ее тканей постоянно меняется в зависимости от возраста, фазы менструального цикла, физиологических периодов жизни, массы тела, наличия патологических процессов. Поэтому специалист, проводящий УЗИ, должен уметь не только правильно идентифицировать различные тканевые компоненты, составляющие молочную железу, но и иметь достаточный опыт, чтобы составить себе представление, какой должна быть в норме структура молочной железы у каждой обследуемой пациентки с учетом отмеченных выше факторов. В настоящее время еще не существует единого подхода к идентификации различных тканей, образующих молочную железу, поэтому одна и та же эхографическая картина разными специалистами часто оценивается по-разному [4]. Кроме того, если врач не имеет четкого представления обо всем диапазоне структурных особенностей молочной железы, выявляемых при УЗИ в норме, то он может некоторые отклонения в пределах спектра нормального развития расценить как патологические. По-видимому, этим можно объяснить удивительно высокую частоту такого диагноза, как фиброзно-кистозная болезнь (ФКБ). Большинство публикаций посвящено ультразвуковой диагностике различных новообразований молочной железы как доброкачественного, так и злокачественного характера. И здесь не возникает принципиальных разночтений эхограмм, поскольку разработана четкая эхосемиотика узловых образований молочной железы [4]. Другое дело ультразвуковая диагностика такого заболевания, как ФКБ, суть которого состоит в дисплазии молочной железы доброкачественного характера с различной степенью выраженности пролиферативных и регрессивных изменений ее тканевых элементов. Учитывая очевидную гипердиагностику ФКБ по данным УЗИ, вновь встает вопрос о необходимости разработки корректной эхографической идентификации тканевых компонентов молочной железы в норме [4]. Отдельным пунктом стоит масталгия, диагностика которой существующими методами визуализации молочных желез представляется абсурдной. А своевременная дифференциальная диагностика масталгии разной этиологии предполагает правильный выбор дальнейшей тактики ведения женщин. Разночтения в интерпретации одной и той же эхографической структуры молочной железы разными авторами диктуют необходимость совершенствовать старые методы и проводить разработку новых методов исследования молочных желез.
К эхографическим критериям рака молочной железы относят: неправильную форму, нечеткие контуры, гипоэхогенную неоднородную структуру, гиперэхогенные включения разной величины, акустические тени, преобладание переднезаднего размера образования.
Новой технологией измерения температуры тканей молочной железы и ее цифрового изображения является метод микроволновой радиотермометрии (РТМ-исследование) с использованием компьютеризированного диагностического комплекса (РТМ-01-РЭС), предназначенного для измерении интенсивности собственного электромагнитного излучения внутренних тканей пациента в диапазоне сверхвысоких частот, которое пропорционально температуре тканей (рис. 1).
.jpg)
В настоящее время в дополнение к существующим методам диагностики появилась возможность визуализации тканей молочной железы с помощью электроимпедансной томографии (рис. 2), метода получения изображения распределения импеданса в тканях. Для визуализации тканей молочной железы используется многочастотный 256-электродный электроимпедансный маммограф (МЭМ), разработанный Институтом радиотехники и электроники РАН, на частотах 10 кГц и 50 кГц.
С целью реализации метода электроимпедансной маммографии разработана измерительная система и алгоритм реконструирования изображений, которые позволяют, используя набор электродов, располагающихся в виде двумерной матрицы на плоской поверхности, визуализировать статические распределения электропроводности среды, прилегающей к поверхности с электродами. Результатом визуализации является набор изображений поперечных сечений среды плоскостями, параллельными плоскости электродов и располагающимися на разной глубине от поверхности среды [1, 2, 9–12].
Во время обследования матрица прижимается к молочной железе в направлении ребер, так что максимальное количество электродов оказывается в контакте с телом пациента, а толщина обследуемых тканей минимальна. Два отводящих электрода, один из которых используется как общий электрод источника тока, а второй — как опорный электрод измерителя разности потенциалов, состыкованы между собой и располагаются на запястье пациентки (рис. 3).
.jpg)
Последовательность работы измерительной системы следующая. Измеритель разности потенциалов подключается мультиплексором к первому электроду матрицы, выполняется процедура компенсации контактной разности потенциалов, а затем источник тока последовательно подключается к каждому из оставшихся электродов матрицы и производятся измерения. После этого цикл повторяется для другого регистрирующего электрода. Полный набор данных, используемых для реконструирования трехмерных распределений электропроводности, состоит из 65 280 результатов измерений. Обработка данных и инициирование процесса измерения осуществляется с помощью персонального компьютера, соединенного с прибором по универсальной последовательной шине (USB).
Результатом реконструирования являются электроимпедансные изображения семи поперечных сечений исследуемой среды, параллельных плоскости с электродами, взятых с шагом 0,7 см по глубине (рис. 4).
.jpg)
Длительность процедуры реконструкции составляет около 15–20 секунд для персонального компьютера с тактовой частотой порядка 1 ГГц.
В распоряжении врачей, занимающихся диагностикой заболеваний молочных желез, появился новый, доступный, безопасный и высокоинформативный метод электроимпедансной маммографии, существенно дополнивший существующий арсенал современных методов обследования, который можно использовать как метод скрининга у женщин всех возрастных периодов, так и в качестве надежного контроля состояния молочной железы при приеме комбинированных оральных контрацептивов и препаратов заместительной гормонотерапии без ограничения числа процедур обследования.
Метод ЭИМ существенно расширяет возможности акушеров-гинекологов и врачей других клинических специальностей в отношении инструментальной диагностики заболеваний молочных желез и дает им уникальные возможности объективной оценки их состояния как составной части неотъемлемого звена единой репродуктивной системы.
Предлагаемая программа многочастотного электроимпедансного обследования позволяет выделить четкие диагностические критерии различной диффузной и очаговой патологии молочных желез, дифференцировать масталгию различной этиологии, что важно для правильного выбора тактики ведения женщин с заболеваниями молочных желез.
Для рака молочной железы характерно:
- На электроимпедансных томограммах в месте вероятного расположения опухоли появляются гипоимпедансные районы с нечеткими размытыми контурами, распространяющиеся на несколько плоскостей сканирования с высокой электропроводностью (чаще всего более 0,95 усл. ед.).
- При использовании дополнительного контрастирования участки с высокой электропроводностью окрашиваются красным цветом.
- При визуализации в режиме цветной шкалы зоны расположения рака выделяются белым цветом с ярким красным контуром.
- Разница в изображениях в зависимости от стороны сканирования из-за нарушения архитектоники внутренних структур пораженной молочной железы при неизмененной здоровой молочной железе.
- Разница в показателях электропроводности в пораженной молочной железе в зависимости от позиции при исследовании.
- Наличие деформаций контуров изображения пораженной молочной железы и четкие недеформированные контуры здоровой молочной.
- Смещение внутренних структур.
- Резкое смещение графика частотного распределения электропроводности вправо по сравнению с непораженной молочной железой и с графиком распределения электропроводности пораженной молочной железы
Несмотря на огромный арсенал методов диагностики рака молочной железы в практике акушера-гинеколога, необходимо помнить, что только комплексное обследование пациенток и цитологическая или гистологическая верификация диагноза, осуществляемые в специализированных лечебных учреждениях, позволяет квалифицированно оказать необходимый перечень медицинских мероприятий. Если есть хоть минимальные подозрения на возможность малигнизации, пациентку необходимо отправить в онкологическое учреждение. В такой ситуации гипердиагностика и ложная тревога может в худшем случае стать тактической ошибкой, однако это может позволить избежать стратегической ошибки, что значительно важнее.
Литература
Ч. Н. Мустафин*, кандидат медицинских наук, доцент
О. В. Троханова**, доктор медицинских наук, доцент
*ГБОУ ДПО РМАПО МЗ РФ, Москва
**ГБОУ ВПО ЯГМА МЗ РФ, Ярославль
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
В статье представлены данные о современных методах неинвазивной лучевой диагностики рака молочной железы
Для цитирования. Гажонова В.Е., Ефремова М.П., Дорохова Е.А. Современные методы неинвазивной лучевой диагностики рака молочной железы // РМЖ. 2016. No 5. С. 321–324.
Введение
Рак молочной железы (РМЖ) сохраняет лидирующие позиции среди онкологических заболеваний у женщин в РФ. Заболеваемость РМЖ на сегодняшний день составляет 20,4% от общей онкологической заболеваемости женского населения в стране. Темпы роста заболеваемости РМЖ, по данным российской статистики, составляют 4−7% в год, по данным общемировой статистики − 1−2% [1−3].
Принимая во внимание высокую социальную значимость РМЖ в современном обществе, необходимо все усовершенствования преинвазивных и малоинвазивных методов диагностики поставить на службу своевременного обнаружения РМЖ, т. к. прогноз и исход заболевания напрямую зависят от стадии процесса.
Ионизирующие методы неинвазивной лучевой диагностики
Рентгеновский томосинтез (РТ)
Это особый тип маммографии, при котором создается трехмерное изображение молочной железы. Рентгеновское излучение сканирует молочную железу под разными углами, информация в цифровом виде передается на компьютер с построением 3D-изображения. Исследователь получает возможность оценить внутреннюю архитектонику тканей молочной железы, наличие микрокальцинатов, плюс-тканей, асимметричных структур в различных анатомических плоскостях в результате лишь одного сканирования. Доза рентгеновского излучения при томосинтезе со стандартным количеством сканирующих проекций сопоставима с дозой при обычной маммографии.
Диагностическая эффективность томосинтеза достигает высокого уровня. По данным Рафферти (2007), при сравнении томосинтеза со скрининговой РМГ в двух проекциях установлено, что в 89% случаев радиологи сочли томосинтез более эффективным в отношении определения объема образования и нарушения архитектоники, в 88% случаев визуализация микрокальцинатов также улучшилась.
По данным Теертстра и соавт. (2010), чувствительность цифрового томосинтеза груди (digital breast tomosynthesis (DBT)) при выявлении РМЖ составила 93%, специфичность − 84%, в 3% случаев результат был ложноотрицательным, а в 7% случаев – ложноположительным.
Потенциал использования РТ достаточно широк − от скрининга до уточняющего метода диагностического поиска. Показаниями к применению РТ служат необходимость дифференциальной диагностики объемных образований РМЖ, выявленных другим методом, а также динамическое наблюдение пациенток на этапах неоадъювантной химиотерапии.
Методика цифрового томосинтеза с ограниченным углом сканирования в последнее время все чаще используется для скрининга за рубежом [9].
Так как цифровой томосинтез является высокотехнологичной и довольно дорогой методикой, мы считаем его применение более целесообразным в качестве дополнительного, уточняющего метода, т. е. в спорных клинических случаях, на этапе перед проведением биопсии.
Рентгеновская компьютерная томография
Говоря об ионизирующих неинвазивных лучевых диагностических методах, стоит упомянуть о рентгеновской компьютерной томографии (РКТ). На современном этапе для выполнения РКТ используют методику динамического спиралевидного мультисрезового сканирования. Чувствительность и специфичность данной методики составляют 98% и 84% соответственно [4]. Особенно оправданно применение РКТ для дифференциальной диагностики отечной формы РМЖ и для оценки метастатического поражения аксиллярных лимфоузлов.
По причине того, что РКТ плохо отображает архитектонику молочной железы, ранняя диагностика форм РМЖ, проявляющихся в виде тяжистой перестройки стромальных структур, трудноосуществима.
Метод РКТ преимущественно применяется в качестве дополнительного в силу высокой стоимости, высокой лучевой нагрузки, имеющихся ограничений со стороны пациентки (клаустрофобия, невозможность применения контраста), сложности визуализации малых форм РМЖ. Словом, РКТ целесообразно применять у пациенток с объемными образованиями диаметром >1 см, которые с высокой долей вероятности являются РМЖ по результатам предыдущего исследования.
Позитронно-эмиссионная томография
В качестве первичной диагностики РМЖ и для определения распространенности процесса в последнее время применяют метод позитронно-эмиссионной томографии (ПЭТ). Метод основан на применении Tc-99m, который преимущественно накапливается в тканях, пораженных неопластическим процессом, вследствие различий со здоровыми тканями в величинах митохондриальных и мембранных клеточных потенциалов, а также вследствие особенностей неоваскуляризации [10]. По данным Ханцерлиогулари и соавт., чувствительность, специфичность, положительный прогностический и негативный прогностический результаты в первичной диагностике РМЖ составили соответственно 77, 50, 77 и 22%. Относительно невысокая специфичность ПЭТ сцинтиграфии объясняется тем, что повышенное накопление Tc-99m тканями может иметь место в т. ч. и при воспалительных, инфекционных и доброкачественных процессах, таких как фиброаденомы, протоковые аденомы. Адлер и соавт. в своем исследовании показали зависимость дифференцировки (Grade) опухоли от величины накопления Tc-99m [4]. Медленнорастущие и хорошо дифференцированные опухоли, такие как протоковая и дольковая карциномы или carcinoma in situ, показывают низкие значения накопления препарата [11, 12], что может приводить к ложноотрицательным результатам, т. е. для метода ПЭТ сцинтиграфии диагностика малых размеров опухоли составляет определенные трудности. По данным ряда исследователей, процент ложноотрицательных результатов колеблется в пределах 10–20%, что статистически сопоставимо с данными УЗИ и РМГ (Hancerliogullari O. et al.). Чувствительность ПЭТ для диагностики метастатического поражения подмышечных лимфоузлов достаточно высока (до 90%), хотя ложноотрицательные результаты могут иметь место при диагностике лимфоузлов диаметром Литература
Образование злокачественных клеток может происходить в различных частях тела. Женщины наиболее подвержены появлению опухолей в груди. Именно поэтому диагностика рака молочной железы является обязательным исследованием. Как распознать заболевание? Какие методы современной диагностики существуют? Почему нужно вовремя проходить обследование и не затягивать с визитом к маммологу?

Важность своевременной диагностики рака груди
Медики рекомендуют каждой женщине, которая перешагнула тридцатипятилетний возрастной рубеж, проходить плановое исследование молочной железы раз в полгода. Иногда исследования могут понадобиться и мужчине. Обнаруживать рак молочной железы могут и у представителей сильного пола.
Специальное обследование включает:
- маммографию
- МРТ
- УЗИ
- биопсию
- цитограмму
- флюорографию
Не стоит забывать и о самообследовании в ванной комнате перед зеркалом после принятия душа. Прощупывание протоковых тканей поможет обнаружить уплотнения внутри железы и оценить степень болезненности.
Своевременная диагностика онкозаболевания груди на 55% снижает смертность среди пациенток с этим заболеванием. Как показывает статистика, в 90% случаев при раннем диагностировании рака можно успешно излечить даже у пожилых людей. Борьба с раком молочной железы при вовремя выявленной патологии имеет более благоприятный прогноз. Проверка здоровья особенно важна при подготовке к операции.
Впервые следует показаться маммологу еще в подростковом возрасте. Далее взрослая женщина должна проходить профилактические осмотры у врача ежегодно. После 35 лет усиливается вероятность появления рака, нужно не забывать осуществлять диагностику состояния молочных желез. Показывать врачу грудь требуется как можно чаще при лактации.
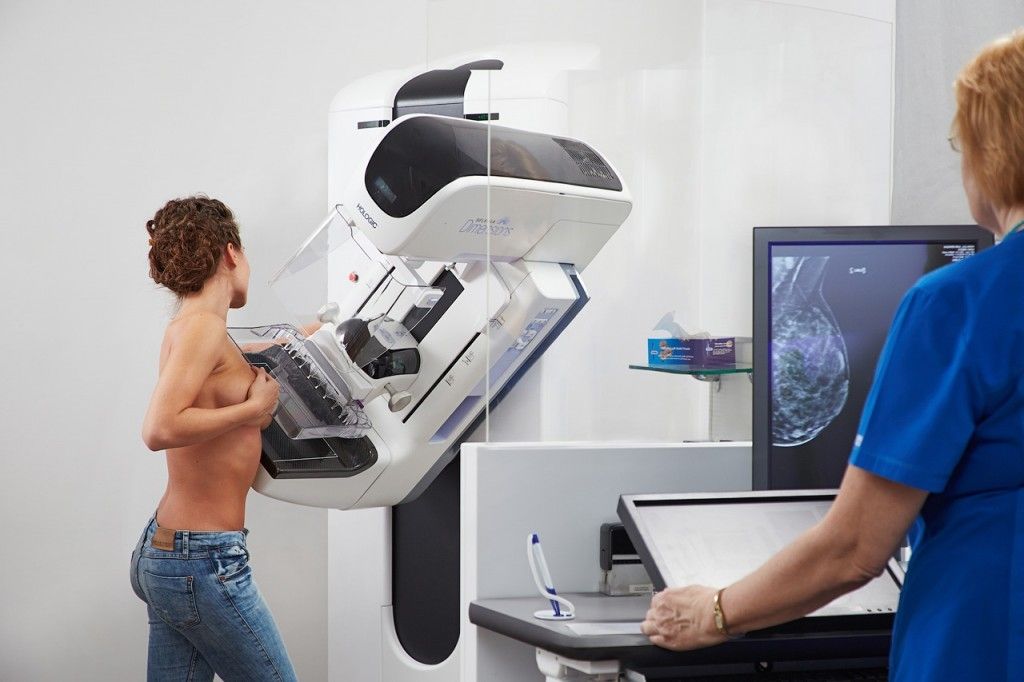
Распознавание рака на ранних стадиях
Рак характеризуется прорастанием злокачественных клеточных структур в ткани, даже, если не наблюдается метастазирования. В пораженной молочной железе происходят злокачественные изменения, которые могут прогрессировать и проявляться болью.
Важно распознавать развитие рака на ранней стадии, поскольку онкология может распространяться стремительно. Ранний раковый очаг легче вылечить. Поэтому необходимо проверять состояние желез при прогрессировании рака. Следует учитывать показатель СОЭ и эритроцитов при сдаче общего анализа крови. При необходимости выполняется сцинтиграфия – неспецефическое исследование груди.
Женщине важно прислушаться к сигналам своего организма. Пальпация позволит выявить в толще груди опухоль. Твердое уплотнение хорошо ощущается. На онкологическое заболевание указывают:
- общая слабость
- тяжесть в молочной железе
- выделение секрета из соска
- тянущая боль в груди и подмышках
- уплотнение в толще груди
Распознать РМЖ на ранней стадии помогут маммография и УЗИ молочных желез. Сканирование выявляет начальные степени рака.
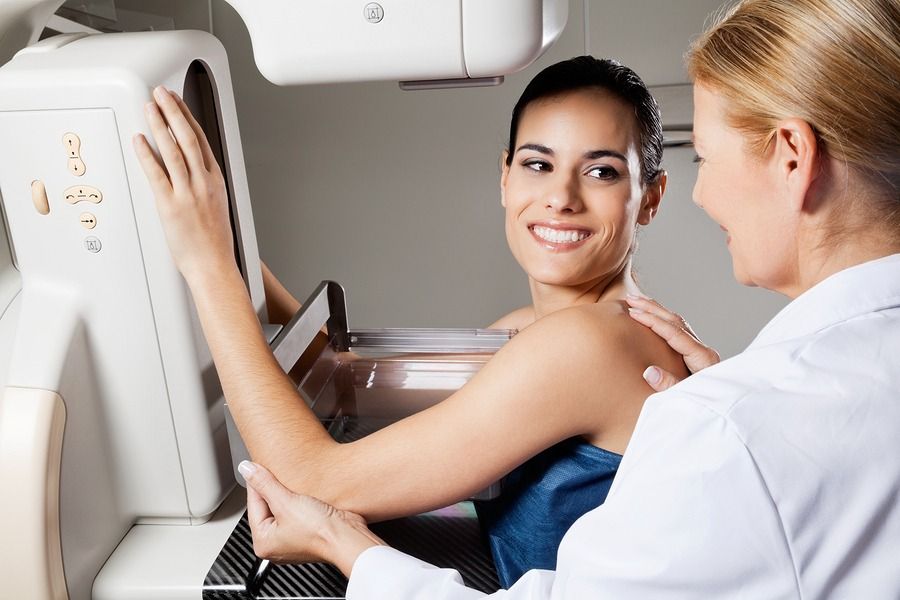
При диффузной форме рака уплотнения не имеют четких очертаний. Очаг на ощупь больших размеров. При самостоятельной пальпации может прощупываться большая шишка в основной толще молочной железы. Определять опухоль можно по симптомам. Внешне болезнь проявляется покраснением груди, болью и дискомфортом.
Основные проявления рака — характерная отечность, может повыситься температурный показатель тела. Кожа груди становится красной, возникает сильная боль. Эти признаки рака нельзя оставлять без внимания. Кожа над раковым новообразованием несколько морщинистая. Рост раковых клеток происходит очень быстро.
Самообследование
Как правильно провести самостоятельно пальпацию для выявления опухоли? Алгоритм действий:
- Осмотреть грудную железу и сосок перед зеркалом.
- Сдавить сосок у основания и посмотреть, есть ли выделения.
- Поднять руку за голову. Второй рукой круговыми движениями медленно прощупать железу. Обратить особое внимание на наличие узлов. Уплотнений, шариков внутри ткани.
- Оценить цвет кожного покрова груди, степень отечности, если таковая имеется.
- Продолжить обследование в лежачем положении тела. Круговыми движениями руки прощупывают всю грудь с легким надавливанием пальцев.
- Прощупать подмышечные впадины на наличие узлов и уплотнений.
Самодиагностику необходимо проводить в домашних условиях, в хорошо освещенном помещении. При осмотре внешнего вида молочных желез руки должны быть опущены. Необходимо обратить внимание на оттенок кожи, выделения из сосков, неровности, деформации груди. Обнаружение уплотнения — подозрение на рак. Сморщенная кожа, выделения из соска, запавший или вытянутый сосок – поводы для беспокойства и срочного обращения к онкологу! Заболевание может развиваться быстро, поэтому необходимо срочное диагностирование и определение диагноза. На представленных в Сети фото четко видно, как может выглядеть патология у больной девушки.

Онкомаркеры
Выявлению патологии способствуют анализы крови на онкомаркер. Используется антиген СА 15-3. С его помощью рак можно диагностировать на ранней стадии. Анализ крови может применяться для первичной диагностики рака молочной железы. Норма показателя не должна превышать 27 единиц.
Также в диагностических целях можно использовать онкомаркер 27-29. Его отличает высокая чувствительность. Однако показатель может быть повышен не только при онкологическом заболевании, но и при туберкулезе, кисте, воспалении легких.
Широко используется в диагностике антиген РЭА. Его норма составляет 5 нг/мл. Если показатель превысил 9-10 единиц, диагностируется рак. Применение онкомаркеров является дополнительной диагностической мерой. При отсутствии визуализации опухоли значения онмаркеров не учитываются. Исследования могут проводиться при рецидиве, если есть наличие
Биопсия
Наличие новообразования не всегда указывает на онкологию. Для выявления злокачественности или доброкачественности процесса применяется биопсия. Данный диагностический метод проводится с помощью специального медицинского аппарата. Процедура осуществляется с помощью длинной тонкой иглы, которая вводится в ткани для забора опухолевых клеток. Взятый биоматериал после подвергается гистологическому микроскопическому исследованию. Узнавать результат можно по истечении определённого срока. Расшифровка осуществляется специалистом.
Биопсия является очень точным диагностическим способом и помогает выявлять рак на любой стадии. Иммуногистохимическое исследование взятых клеточных структур устанавливает форму, характер и стадию рака. Скорость разрастания злокачественной опухоли зависит от гормональных изменений в организме и может выражаться в разных симптомах. Методика помогает определить реагирование мутационных клеток на назначенные лекарственные препараты и получить верное заключение о состоянии здоровья.
Маммография
Высокой информативностью обладает рентгенологическое исследование – маммография. Этот метод используется для профилактических осмотров и для установки диагноза.
Маммографическое исследование осуществляется с помощью аппарата маммографа. Он помогает обнаружить онкологический процесс до появления первых признаков рака. Мамограмма показывает отложения кальция в груди, узлы, уплотнения. После 40 лет каждая женщина должна проходить данное обследование, чтобы дифференцировать заболевание.
Магнитная томография позволяет получить четкое изображение патологического очага в грудной железе. Этот метод обеспечивает точную визуализацию патологического очага и злокачественных изменений в железистых тканях во время менопаузы.
МРТ помогает получить основную информацию:
- плотность опухоли
- наличие расширение молочных протоков
- определение разрыва импланта
- локализацию патологии
- размеры новообразования
МРТ – неинвазивный диагностический способ, совершенно безопасный для женского организма. Лучи не оказывают пагубного воздействия во время сканирования. Процедура позволяет получить ранее недоступную информацию при использовании других методов. Также МРТ позволяет провести сканирование костей при раке молочной железы. В пораженной груди происходит деформация твердой ткани.

Скриннинг
Если женщина входит в группу риска, ей обязательно надо выполнить скрининг молочной железы. Скриннинговый метод включает несколько направлений:
- врачебный осмотр
- маммографию
- лабораторные анализы
- генетические исследования
- УЗИ
- различные тесты
Комплексная диагностика позволяет подтвердить или исключить рак и его метастазы. Скриннинг особенно важен после выздоровления от рака, при беременности, в процессе лечения.
Цитограмма
Проводить цитограмму необходимо при выраженном дискомфорте в груди. В качестве профилактики тоже не следует отказываться от процедуры. Для обследования молочной железы проводят цистологическое исследование выделений из соска и содержимого лимфоузлов.
Диагностическая пункция помогает:
- выявить норму и отклонения в клеточном составе
- дать оценку отдельной клетки и их совокупности
- провести морфологию клетки и ее ядра

Цитограмма распознает увеличение размера клетки, неровность контуров ядра, рисунок хроматина. С помощью исследования выявляют увеличенные размеры клеточного ядра, его форму, полиморфизм.
Флюорография
Диагностика с помощью рентгенологических лучей называется флюорографией. Процедура является безопасной. Женщина раздевается до пояса и с помощью аппарата выполняется рентген грудной клетки и молочных желез.
Диагностировать можно наличие фиброза тканей, абсцесс, локализацию и особенности новообразования. Снимок не обладает большой точностью на ранних стадиях рака. Сегодня устаревшие флюорографические аппараты во многих клиниках заменили на современные цифровые. Такая аппаратура обладает большой точностью, позволяет увидеть патологию и оказывать меньшую лучевую нагрузку
Дифференциальная диагностика
Дифференциальные диагностические методы необходимы, если рак молочной железы сопровождается различными сопутствующими болезнями. Детальное клиническое обследование требуется при подвижной фиброаденоме, липогранулеме, мастопатии, сосудистой опухоли. Тщательная диагностика проводится при подозрении на маститоподобный рак груди, когда наблюдается ограниченная подвижность ткани и ее высокая плотность.
Дифференциальную диагностику необходимо провести при различных ошибках диагностики рака молочной железы. При затруднении постановки диагноза детальное обследование молочной железы непременно даст свои результаты. Диагностироваться следует при первых признаках злокачественного процесса. Правильно установленный диагноз обеспечит верное назначение лекарственных средств для эффективной борьбы с патологией.

Фиш-анализ
Цитогенетическое исследование (fish-анализ) – исследование изменений в хромосомах человека. Тест носит и другое название – флуоресцентная гибридизация. Для выполнения информативного генетического анализа осуществляют забор тканей железы. Способ помогает выявить генетическую предрасположенность и изменения в молочной железы. Мужской и женский наследственные факторы – основная причина генетических аномалий. Принцип данного тестирования – исследование ДНК интерфазных ядер.
Читайте также:

