Некроз опухоли на мрт
а) Терминология:
1. Сокращения:
• Псевдопрогрессирование (ПсП)
2. Синонимы:
• Контрастное усиление, связанное с лечением
3. Определение:
• Увеличение размеров зоны контрастного усиления, связанное с лечением, которое имитирует прогрессирование опухолевого процесса:
о Классически описывается после химиолучевой терапии (темозоломид в сочетании с лучевой терапией)
• Обычно наблюдается в течение З-6 месяцев после лучевой терапии (ЛТ)
• Купируется самостоятельно, накапливающие контраст поражения разрешаются без нового курса лечения
б) Визуализация:
1. Общие характеристики псевдопрогрессирования опухоли головного мозга:
• Лучший диагностический критерий:
о Появление нового накапливающего контраст поражения в сочетании с ↑ размеров зоны повышения интенсивности сигнала на FLAIR после лечения глиобластомы (ГБМ) через 3-4 месяца после завершения ЛТ
• Локализация:
о Локализация новообразования, по поводу которого проводилось лечение, или в смежной мозговой ткани о Обычно в пределах зоны облучения
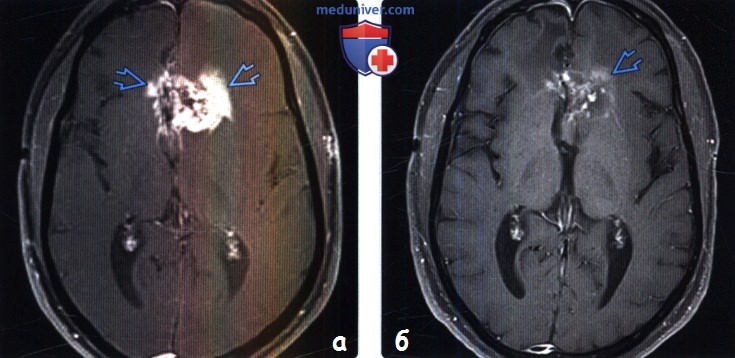
(а) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у мужчины 48 лет, которому проводилась лучевая терапия и курс лечения темодаром в течение трех месяцев по поводу злокачественной глиомы, в лобных долях определяются новые участки накопления контрастного вещества. При первичном послеоперационном МРТ контрастного усиления не наблюдалось. Клиническая картина не ухудшалась.
(б) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у этого же пациента спустя четыре недели при отсутствии изменений в курсе лечения определяется заметное снижение интенсивности контрастного усиления, что обусловлено псевдопрогрессированием опухоли, вероятно, вызванным с воспалительной реакцией.
в) Дифференциальная диагностика псевдопрогрессирования опухоли головного мозга:
1. Рецидив злокачественной глиомы:
• Новый участок контрастного усиления после лечения по поводу новообразования
• Субэпидемимальное распространение указывает на рецидив опухоли
• ДВИ: низкие значения ИКД
• ПВИ: высокие значения CBV указывают на рецидив опухоли
3. Псевдоответ:
• Снижение интенсивности контрастного усиления, связанное с антиангиогенными агентами (авастин), а не с истинным ответом опухоли на лечение
• Опухоль обычно имеет гиперинтенсивный на FLAIR и ДВИ сигнал
• Связано с уменьшением проницаемости сосудов
• Часто приводит к продолженному инфильтративному росту опухоли, не накапливающей контраст
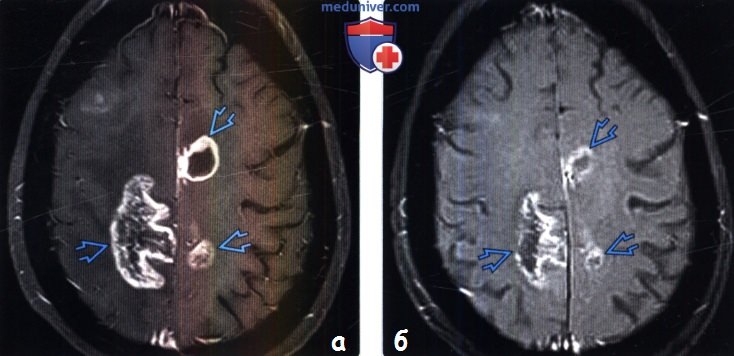
(а) МРТ, постконтрастное Т1 -ВИ, аксиальный срез: у женщины 62 лет с мультифокальной глиобластомой (МГБ) через четыре месяца после курса лечения темодаром, а также курса лучевой терапии в больших полушариях определяются новые зоны контрастного усиления, обусловленные прогрессированием опухоли.
(б) МРТ, постконтрастное Т1 -ВИ, аксиальный срез: у этой же пациентки через восемь недель после предыдущего исследования в условиях отсутствия лечения определяется заметное уменьшение размеров контрастируемых поражений. Появление новых зон накопления контрастного вещества было обусловлено псевдопрогрессированием (ПсП), что связано с более высокой выживаемостью.
г) Патология:
1. Общие характеристики псевдопрогрессирования опухоли головного мозга:
• Считается, что причина ПсП связана с сосудистым и олигодендроглиальным повреждением, приводящим к воспалению и повышению проницаемости гематоэнцефалического барьера
2. Макроскопические и хирургические особенности:
• Расширение сосудов, фибриноидный некроз, поражение эндотелия сосудов нормальной мозговой ткани
д) Клиническая картина:
1. Проявления псевдопрогрессирования опухоли головного мозга:
• Наиболее частые признаки/симптомы:
о Обычно бессимптомное течение
о Возможны симптомы, связанные с увеличением масс-эффекта
2. Течение и прогноз:
• Современным стандартом лечения злокачественных глиом является хирургическая резекция с адъювантной одновременной лучевой терапией и химиотерапией с темозоломидом (темодар):
о Встречаемость ПсП составляет 30-50% среди пациентов, получавших лечение
• Вероятно, степень выраженности изменений увеличивается с увеличением дозы облучения
• ПсП связано с более высокой выживаемостью:
о Может быть связано с положительной корреляцией со статусом метилирования промоторной области гена О6-метилгуа-нин-ДНК-метилтрансферазы (MGMT)
3. Лечение:
• Никаких изменений в курсе лечения не требуется
• Некоторые онкологи проводят лечение глюкокортикостероидами
е) Диагностическая памятка. Обратите внимание:
• Появление новых участков контрастного усиления и масс-эффекта при злокачественной глиоме не всегда означает прогрессирование заболевания
• Для постановки точного диагноза псевдопрогрессирования заболевания могут потребоваться исследования в динамике
ж) Список литературы:
1. Boxerman JL et al: Response Assessment and Magnetic Resonance Imaging Issues for Clinical Trials Involving High-Grade Gliomas. Top Magn Reson Imaging. 24(3):127-36, 2015
2. Yun TJ et al: Glioblastoma treated with concurrent radiation therapy and temozolomide chemotherapy: differentiation of true progression from pseudoprogression with quantitative dynamic contrast-enhanced MR imaging. Radiology. 274(3):830-40, 2015
3. Hygino da Cruz LCJr et al: Pseudoprogression and pseudoresponse: imaging challenges in the assessment of posttreatment glioma. AJNR Am J Neuroradiol. 32(11):1978-85, 2011
Редактор: Искандер Милевски. Дата публикации: 2.5.2019
Массовая гибель раковых клеток может возникнуть спонтанно или на фоне лечения. Некроз опухоли – это разрушение злокачественного, предракового или доброкачественного новообразования, во время которого в кровь пациента поступает большое количество вредных веществ и токсических факторов, вызывая типичные симптомы общей интоксикации.
Разрушенные раковые клетки выбрасывают в организм токсические вещества
Некроз опухоли – что это такое
Быстро растущее злокачественное новообразование любой локализации вызывает массу проблем в организме человека, но общее состояние становится значительно хуже при массовом разрушении опухолевых клеток. Некроз опухоли возникает на фоне следующих факторов:
- Действие лекарственных препаратов;
- Облучение (радиотерапия);
- Частичное удаление опухолевых тканей во время хирургической операции;
- Внешняя механическая травма;
- Действие физических факторов (холод – криодеструкция, тепло – коагуляция);
- Нарушение кровотока (гипоксия тканей);
- Воспалительный процесс в опухоли.
В отличие от апоптоза клеток, некроз опухоли является патологическим процессом, который не предусмотрен природой и не является защитным фактором противоопухолевого иммунитета: одномоментно гибнет множество раковых клеток с обязательным распадом тканевых структур с токсическим воздействием на организм.
Токсические факторы некротического распада
Разрушающиеся структуры опухолевых тканей выбрасывают в кровь больного человека следующие факторы:
- Соли мочевой кислоты, оказывающие отрицательное действие на мочевыделительную систему (почечная недостаточность);
- Продукты обмена фосфора (изменение равновесия микроэлементов кальция и фосфора провоцирует мышечные и неврологические расстройства);
- Соли калия, негативно влияющие на работу сердца и сосудов;
- Опухолевые ферменты и биологически активные вещества с агрессивными свойствами, разрушительно действующими на здоровые ткани и системы.
Худший вариант обменно-метаболических нарушений в организме – ацидоз (повышение кислотности) крови, который изнутри разрушает все внутренние органы.
Симптомы при некротическом распаде опухолевых тканей
Вне зависимости от причины, возникший некроз опухоли провоцирует следующие проявления:
- Нарастающая слабость, быстрая утомляемость;
- Потеря массы тела без видимой причины;
- Температурная реакция в виде озноба и лихорадки;
- Бледная землистого цвета кожа;
- Мышечные судороги;
- Тошнота с периодически возникающей рвотой;
- Проблемы со стулом (понос или запор);
- Отказ от пищи (потеря аппетита);
- Перебои в работе сердца (аритмия);
- Различные варианты неврологических расстройств (от апатии до потери сознания).
Симптомы общей интоксикации разнообразны, но не заметить их невозможно. Некроз опухоли может вызвать типичные признаки максимально рано – сразу после химиотерапии или облучения, на фоне быстро прогрессирующего опухолевого роста, когда часть новообразования спонтанно разрушается.
Методы лечения при заболевании
Важно вовремя обнаружить рак – при поздней диагностике именно некроз опухоли может стать первым проявлением болезни. В каждом конкретном случае лечение подбирается индивидуально с учетом следующих факторов:
- Диагноз (месторасположение опухоли и стадия болезни);
- Наличие типичных симптомов;
- Риск осложнений (кровотечение, кома, заражение крови, воспаление).
По возможности надо удалить новообразование, в котором возник некроз опухоли. Важными элементами терапии являются:
- устранение токсических факторов из крови;
- восстановление метаболического равновесия (надо убрать ацидоз);
- коррекция неприятных симптомов (борьба с рвотой и поносом);
- устранение обезвоживания;
- обезболивание;
- помощь сердцу, печени и почкам;
- устранение воспаления.
Оптимально все эти задачи решать в условиях больницы – в домашних условиях справиться с симптомами общей интоксикации практически невозможно. Распад опухоли не всегда возможно предотвратить (и не нужно), но некроз опухоли оказывает негативное действие на все жизненно важные органы и системы, поэтому врач назначит специальную терапию для предотвращения осложнений.
Мысли об онкологии: просто о сложном на Дзен.Канале Onkos

Лучевой (радиационный) некроз, представляющий собой очаговое структурное поражение в месте локализации опухоли, является отдаленным осложнением со стороны центральной нервной системы (ЦНС) после радиотерапии либо радиохирургии.
Отек тканей и присутствие новообразования вызывают в паренхиме органов ЦНС, находящейся в ложе опухоли, изменения, которые повышают вероятность развития лучевого некроза. Радиационный некроз может возникнуть в том случае, когда радиотерапия назначается по поводу первичных новообразований ЦНС, метастатических поражений головного мозга либо опухолей головы и шеи. Лучевой некроз может развиться после любого применения ионизирующего излучения для лечения опухолей или использования любого протокола такого лечения.
Диагностика лучевого некроза и его лечение представляют значительные трудности, поскольку проявления этого осложнения радиотерапии часто перекрываются симптомами рецидива опухоли. Ошибочный диагноз (рецидив новообразования вместо лучевого некроза) может стать причиной назначения неправильного лечения, способного представлять опасность для жизни пациента.
Симптомы лучевого некроза
Нужно понимать, что лучевой некроз является отдаленным осложнением радиотерапии, развитие которого нередко происходит месяцы, а то и годы спустя после завершения лечения ионизирующим излучением. Чаще всего он проявляется в период от 6 месяцев до 2 лет после завершения последнего курса радиотерапии.
В современной медицинской литературе встречаются данные о частоте развития лучевого некроза, которые отличаются значительной вариативностью – от 5% до 37% всех пациентов, получавших радиотерапию по поводу внутричерепных опухолей.
При этом некоторые авторы сообщают о том, что до 10% всех случаев этого осложнения радиотерапии были бессимптомными и выявление лучевого некроза в подобных случаях целиком является заслугой прогресса в методах нейровизуализации. Лечащим врачам необходимо принимать во внимание возможное отсутствие симптомов лучевого некроза у больных, несмотря на развитие патологического процесса.
В тех случаях, когда развитие лучевого некроза все же сопровождается симптоматикой, у пациентов чаще всего наблюдаются следующие признаки:
- головная боль;
- тошнота;
- когнитивные нарушения;
- судорожные припадки;
- очаговая неврологическая симптоматика, связанная с локализацией очага некроза;
- изменение личности;
- апатия;
- гемипарез.
Мозговые кровоизлияния при лучевом некрозе явление редкое, но, тем не менее, встречающееся в практике нейроонкологов.
Лучевой некроз: диагностика
МРТ является наиболее распространенным методом диагностики лучевого некроза. Однако при этом нужно отметить, что изображения ЛН, полученные с помощью этого метода, очень часто напоминают картину рецидива опухоли – с увеличением контрастности в пораженном участке и отеком, расположенным по периферии патологического очага.
В результате из-за низкой прогностической ценности обычной МРТ большее значение приобрели более современные методы диагностики:
- магнитно-резонансная спектроскопия;
- перфузионная МРТ;
- позитронно-эмиссионная томография (ПЭТ).
Диагностика лучевого некроза с помощью первого из этих методов (магнитно-резонансной спектроскопии) основана на том, что жизнеспособная опухоль обладает ненарушенной сосудистой системой, вследствие чего объем кровотока в ней больше по сравнению с некротической тканью.
Для дифференциального диагноза в этом случае используется показатель относительного церебрального объема крови, полученный с помощью динамической контрастной МРТ. При опухолях этот показатель выше по сравнению с лучевым некрозом.
Оценка состава метаболитов в метастатической опухоли головного мозга с помощью магнитно-резонансной спектроскопии является еще одним ценным методом дифференциальной диагностики. Повышенные показатели соотношения холин/креатинин и холин/N-ацетиласпартат могут свидетельствовать в пользу рецидива опухоли, а не лучевого некроза.
Перспективным направлением в дифференциальной диагностике лучевого некроза можно назвать и ПЭТ с фтортирозином. Некоторые авторы сообщают о чувствительности этого метода в 100% и специфичности 93% при диагностике ЛН.
Что же касается использования гистологического исследования для диагностики лучевого некроза, то надо подчеркнуть, что объем биоптата должен быть таким, чтобы иметь возможность полностью исключить рецидив опухоли и вместе с тем не вызвать клинически значимого неврологического дефицита. При заборе биоптата следует избегать нарушения целостности структур мозга, расположенных в глубине центральной части таламуса, двигательной области коры головного мозга, затылочной области и центров речи.
Обычно в образцах ткани, пораженной некрозом, не обнаруживается преобладание злокачественных клеток. Вместе с тем, ткани облученной опухоли могут содержать некротизированные участки, что не всегда указывает на лучевой некроз.
При лучевом некрозе исследование биоптата может выявлять утолщение кровеносных сосудов с пролиферацией эндотелия и/или гиалинизацию с фиброзом и умеренной инфильтрацией лимфоцитов и макрофагов.
Лучевой некроз: лечение
Для эффективного лечения лучевого некроза первостепенное значение имеет правильно поставленный диагноз, так как ошибочный диагноз рецидива опухоли и последующее противоопухолевое лечение могут привести к нежелательным тяжелым последствиям.
В отношении пациентов без симптомов лучевого некроза, у которых в период наблюдения с помощью МРТ выявляется некротическая масса, может быть избрана выжидательная тактика. Если выбор стратегии лечения не зависит от того, выявлен ли у больного лучевой некроз или рецидив глиомы, состояние такого больного нужно контролировать с помощью серии МРТ.
Однако тактика лечения должна быть другой при наличии таких симптомов как синдром объемного образования в полости черепа, повышенное внутричерепное давление, неврологические нарушения. В подобных случаях возможно использование таких методов лечения (раздельно или в комбинации):
- назначение кортикостероидов;
- в случае неэффективности стероидов можно рассмотреть использование бевацизумаба (моноклональное антитело, которое селективно связывается с биологически активным фактором роста эндотелия сосудов (VEGF) и нейтрализует его);
- гипербарическая оксигенотерапия (подача кислорода под давлением 2-3 атм. На курс лечения: 20-30 сеансов продолжительностью 90-120 минут каждый).
Хирургическое лечение лучевого некроза имеет свои преимущества и недостатки. Удаление некротической массы способствует быстрому снижению повышенного внутричерепного давления и восстановлению неврологических функций. Вместе с тем, такая операция связана с риском серьезных осложнений и проводится в основном пациентам, у которых консервативное лечение оказалось безрезультатным.
Факторы риска лучевого некроза
К настоящему времени установлены несколько факторов риска, которые способствуют развитию лучевого некроза. По мнению ведущих специалистов в области нейроонкологии, несмотря на то, что эти факторы риска были в основном обнаружены у пациентов с артериовенозными мальформациями, которым назначалось радиохирургическое лечение, а также пациентов с глиомой, они могут быть экстраполированы и на всех больных с метастазами в головной мозг:
- объем опухоли и поглощенная доза;
- применение химиотерапии наряду с радиотерапией;
- локализация опухоли (риск развития ЛН является максимальным при облучении лобного отдела коры мозга и значительно меньшим при облучении стволовой области мозга);
- гистологические особенности опухоли.
Установлено также, что радиотерапия некоторых метастатических опухолей головного мозга связана с повышенным риском развития лучевого некроза в зависимости от формы первичной опухоли. Увеличение частоты развития ЛН наблюдается при радиотерапии метастазов в головной мозг при следующих опухолях:
- карцинома почки;
- аденокарцинома легкого;
- меланома кожи с мутацией онкогена BRAF V600;
- HER2-позитивный рак молочной железы.
Кроме того, способствует развитию лучевого некроза и повышенная индивидуальная чувствительность к действию ионизирующего излучения.
Опухоли головного мозга долгое время диагностировали исключительно по клиническим признакам, часто слишком поздно. С появлением нейровизуализационных методов стало возможным выявление опасных патологий на ранних этапах их развития. Уже на первых стадиях формирования опухоль головного мозга на МРТ отчетливо видна, а врачи могут планировать дальнейшие действия. Ранняя диагностика увеличивает шансы на выздоровление даже при онкологических заболеваниях.
Симптомы рака головного мозга
Злокачественные опухоли составляют почти половину выявленных внутричерепных новообразований. Общими проявлениями патологических изменений в мозге могут быть:
- головные боли, часто утренние, с тошнотой и рвотой;
- вертиго (головокружение центрального происхождения);
- нарушение координации движений;
- ухудшение зрения, слуха;
- речевые расстройства;
- раздражительность;
- сонливость;
- судороги;
- поведенческие расстройства;
- слабость в мышцах лица или конечностей;
- онемение, парестезии в отдельных частях тела;
- психические нарушения и др.
Клиника опухолей отличается в зависимости от локализации, размеров, типа новообразования. Патологию дифференцируют исходя из данных, полученных при инструментальном и лабораторном обследовании, гистологического анализа тканей.
По тому, как выглядит опухоль мозга на МРТ, врачи делают предположения о ее природе. Однозначных утверждений быть не может, так как верификацию образований осуществляют с помощью гистологического анализа. Характерными признаками злокачественных опухолей головного мозга на снимках МРТ являются:
- неправильная их форма;
- нечеткие контуры новообразований;
- выраженный перифокальный отек;
- масс-эффект (смещение близлежащих структур);
- гидроцефалия;
- неоднородное накопление контраста (иногда вообще не накапливают);
- "пестрота" опухоли (кровоизлияния, некрозы и/или кисты в структуре) и др.
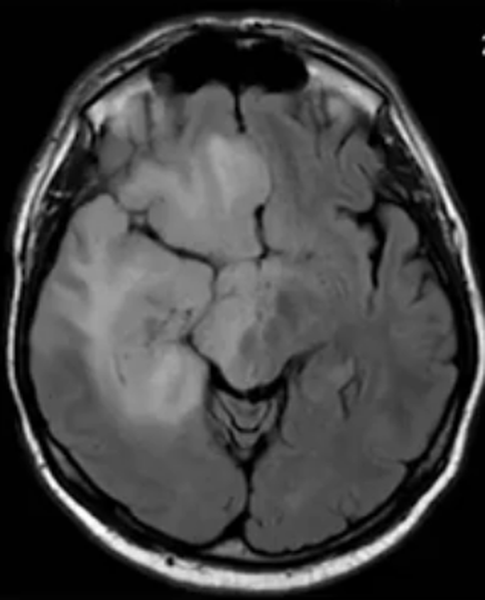
Глиобластома на МРТ головного мозга без контраста
Причины появления опухоли головного мозга
Точный механизм формирования злокачественных образований не установлен. Факторами риска признаны возраст старше 70 лет, принадлежность к мужскому полу. Чаще опухолевые патологии мозга обнаруживают у пациентов, которые имеют:
- отягощенный семейный анамнез;
- контакты с канцерогенными веществами;
- радиационное воздействие;
- черепно-мозговые травмы в анамнезе;
- перенесенные воспалительные патологии головного мозга.
У некоторых пациентов с обнаруженными опухолями врачам не удается выявить ни одного провоцирующего фактора, тогда как у лиц, которые регулярно подвергаются их воздействию, новообразований мозга нет. Такие сведения подвергают сомнению существующие гипотезы о происхождении онкопатологий ЦНС (центральной нервной системы).
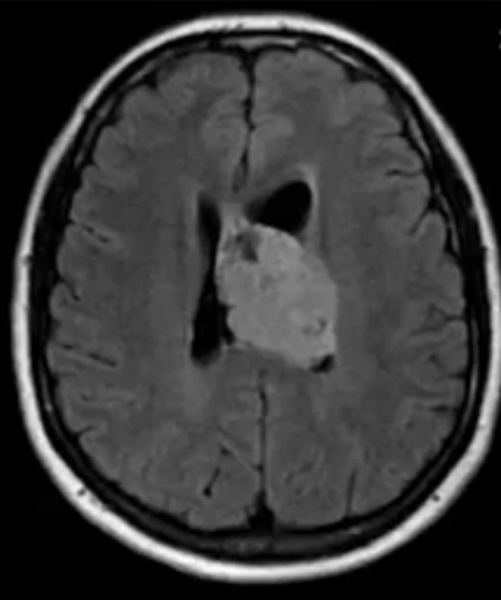
Эпендимома при МР-сканировании головного мозга
Опухоли головы часто по своей природе являются вторичными, т.е. метастазами. По локализации образования могут быть расположены в костях черепа, мягкой и твердой мозговых оболочках, в сером и белом веществе. В структуры головы чаще метастазируют меланомы, рак почки, простаты, легкого, молочной железы, желудка.
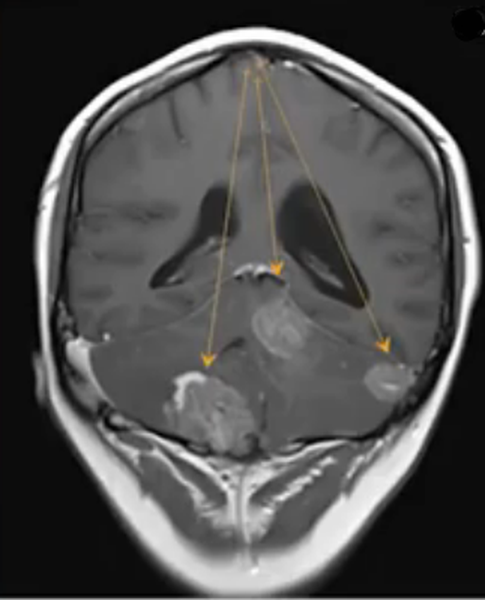
Метастазы в головном мозге на постконтрастном изображении (указаны стрелками)
Может ли МРТ показать опухоль головного мозга?
По результатам магнитно-резонансной томографии врачи могут выявить изменения структуры тканей. Опухоли головного мозга на МРТ определяют по прямым и косвенным признакам. Врачи подозревают патологическое образование по типу и равномерности изменений МР-сигнала:
- гипо- (более слабый, чем окружающие области) или гиперинтенсивный (отклик сильнее, чем от нормальных зон);
- гетероизмененный (смешиваются разные характеристики);
- изоинтенсивный (опухоль выглядит, как другие ткани, но отличается от нормальной архитектоники мозга).
Существуют и косвенные признаки. Последние дают основания подозревать новообразование головного мозга на фоне изоинтенсивного отклика тканей или подтверждают ее наличие при измененном МР-сигнале.
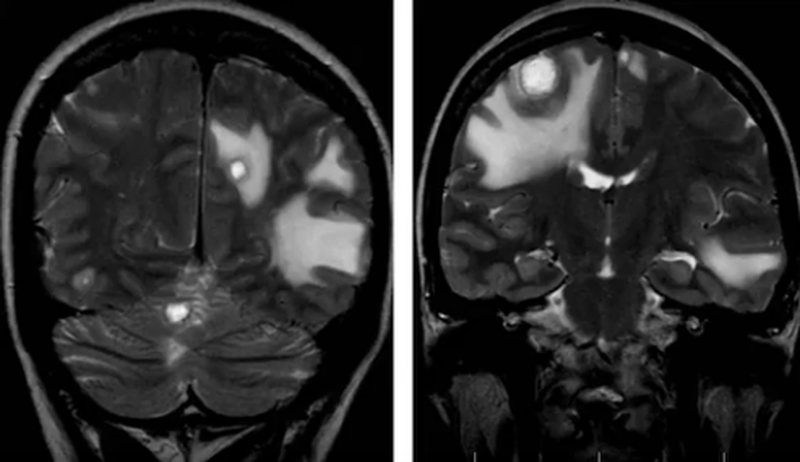
Множественные метастазы в вещество головного мозга на МРТ без контраста
Вторичными проявлениями патологии могут быть:
- латеральная дислокация срединных структур;
- смещение сосудистого пучка;
- изменение величины и деформации желудочков;
- аксиальная дислокация;
- окклюзионная гидроцефалия при блокаде ликворных путей;
- смещение или деформация базальных цистерн;
- отек мозга в зоне опухоли и вокруг нее (локальный, генерализованный, тотальный, перивентрикулярный).
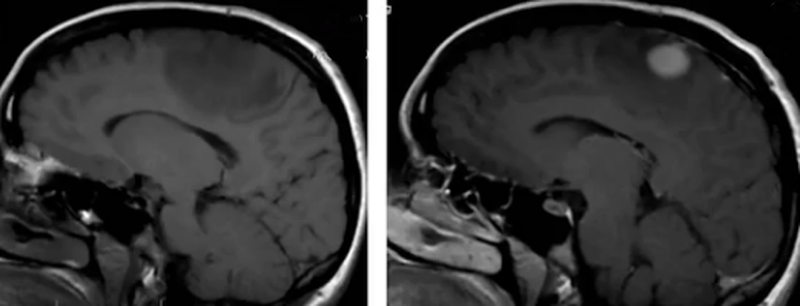
До- и постконтрастное изображение злокачественной опухоли головного мозга
С помощью МРТ при раке мозга выявляют локализацию опухоли, степень ее инвазии в соседние структуры, особенности кровоснабжения, стадию заболевания и наличие метастазов. Для получения дополнительных сведений, сканирование проводят в различных последовательностях (Т1, Т2, FLAIR, диффузно-взвешенное и пр.), в нативном режиме и после контрастирования.
Заключение МРТ при опухоли головного мозга
Пациент получает результаты сканирования на бумаге и/или на информационном носителе со снимками. Заключение составляет врач-рентгенолог. Он изучает снимки, замечает отклонения от нормы и фиксирует их.
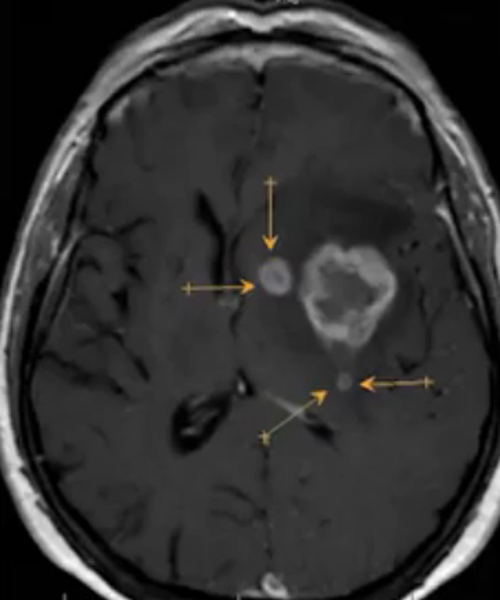
Опухоль головного мозга на МРТ с отсевами (указаны стрелками)
В заключении описывают зоны измененного МР-сигнала, их локализацию, размеры, контуры, наличие масс-эффекта, признаков перифокального отека и дислокационные явления. Выводы рентгенолога нельзя считать диагнозом. Результаты исследования должен изучить врач, который инициировал диагностику, или онколог. На поздних стадиях развития заболевания по структуре и характеристикам опухоли можно с большой долей вероятности определить ее тип. Окончательный диагноз ставят с учетом результатов других исследований.
Рак головного мозга на фото снимке МРТ
В зависимости от типа новообразования отличается его внешний вид. Изучая снимки, врач может лишь предположить природу основных вариантов опухолей по характерным признакам:
- астроцитомы — происходят из глиальной ткани, чаще выявляются в лобных и височных долях. Выглядят как зоны гипоинтенсивного МР-сигнала без четких контуров, плохо или почти не накапливают контраст, нередко содержат в своей структуре обызвествленные зоны и мелкие кисты;
- олигодендроглиомы — плотность снижена неравномерна, контуры относительно четкие, часто сливаются с отеком. Обнаруживаются в лобной или теменной долях.
- эпендимомы — предположительно образуются в эмбриональном периоде. Характеризуются четкими контурами, плотнее, чем здоровые ткани, редко вызывают отек, чаще обнаруживаются в полостях желудочков;
- глиобластомы — злокачественные опухоли, которые отличаются высокой скоростью роста и склонностью к инвазии. Выглядят на снимках, как образования неправильной формы, с нечеткими фестончатыми контурами и выраженным перифокальным отеком. Дают выраженный масс-эффект, смещают головной мозг в полости черепа, повреждая его на отдалении от своего местоположения;
- менингиомы (оболочечные опухоли). На снимках часто дают изоинтенсивный сигнал, отчетливо видны после контрастирования. Имеют четкие контуры, неправильную бугристую форму, обычно нет выраженной зоны перифокального отека;
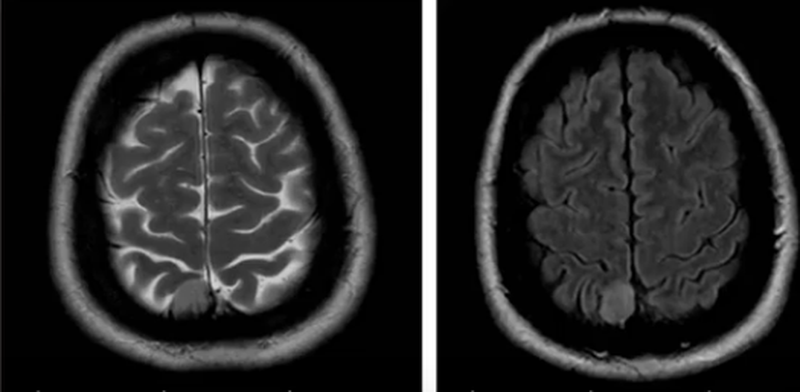
Менингиома на МРТ
- метастазы. Выглядят, как множественные образования в тканях головного мозга различных размеров, неправильной формы, с неровными контурами, накапливающие контраст, с различной интенсивностью отека вокруг;
- невриномы — опухоли черепно-мозговых нервов. Чаще исходят из корешка VIII пары, реже V и остальных. На Т2-взвешенном изображении гиперинтенсивны по сравнению с окружающими тканями. Контуры неправильные, четкие, структура гомогенная, дают масс-эффект.
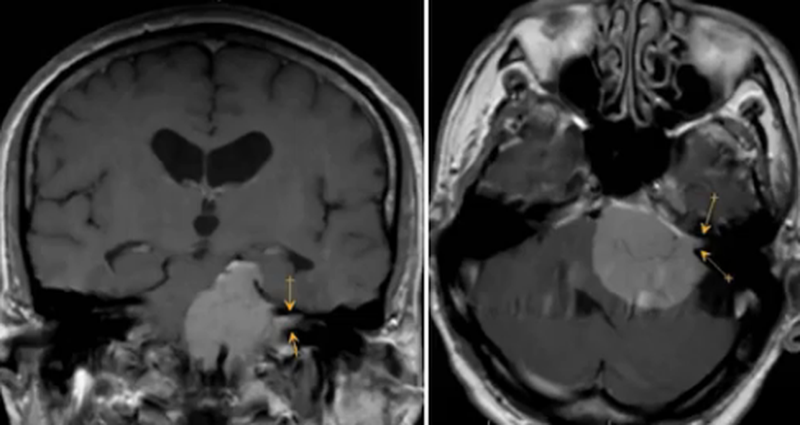
МР-изображение невриномы VIII пары черепно-мозговых нервов (стрелками указана часть опухоли, растущая из внутреннего слухового прохода)
В редких случаях опухоли малого размера не обнаруживают при первом обследовании. При наличии клинических проявлений заболевания врач назначает другие методы исследования или повторное сканирование.
МРТ ― безопасная и высоко информативная диагностическая процедура. Отсутствие лучевой нагрузки позволяет проводить ее столько раз, сколько нужно для контроля состояния больного. Метод актуален для предварительной оценки степени злокачественности образования, повреждения близлежащих структур, особенностей кровоснабжения опухоли. По результатам сканирования врач уточняет сохранность функций мозга, опасности заболевания и составляет план обследования или лечения. Своевременное выявление опухоли в мозге может спасти человеку жизнь. Поэтому роль МРТ в диагностике и лечении онкопатологии ЦНС чрезвычайно велика.

МРТ головного мозга

Показания к МРТ головного мозга

МРТ головы
Дифференциальная диагностика должна проводиться со всеми очаговыми и объемными поражения головного мозга.
При спектроскопических измерениях глиобластом, NAA присутствует в определенной степени, а в метастазах NAA снижен [2]. Коэффициент Cho/Cr соотношения увеличен в перитуморальной области глиом и снижен у метастазов, что объясняется микроскопической инфильтрацией этой зоны клетками опухоли [27, 105]. Эпицентр метастаза в белом веществе иногда распространяется на эпендимарные поверхности [98].
Метастазы, в отличии от глиальных опухолей, имеют более низкий сигнал на DWI в зоне перифокального отека. Значения ADC метастазов ниже, чем у глиальных опухолей. При оценке перфузии rCBF и rCBV - повышены даже за границами накапливающей контраст глиомы, но не повышены за пределами границ метастаза.
При наличии некроза, метастаз не отличаются от глиобластомы. При проведении трактографии отмечается, что метастазы смещают тракты, а глиомы разрушают их. ПЭТ позволило существенно улучшить определение первичного очага, распространенность процесса в теле человека, что позволяет на дооперационном этапе выявить источник [2].

Глиобластома и метастаз представлены массами с перифокальным отёком (звёздочки на рис.1742), а так же являются опухолями, число которых не предрасполагает к постановке диагноза, в связи с тем, что глиобластомы могут быть мультифокальными, а метастазы могут быть солитарными. Ограничение диффузии, оцениваемое по DWI при глиоме, не будет ограничиваться видимыми краями опухоли (головки стрелок на рис.1743), но не распространяется за пределы видимых метастазов (головки стрелок на рис.1744).
Геморрагический инсульт на фоне гипертонического криза типично приводит к формированию гематомы в базальных ядрах и сопровождается тяжёлой клинической картиной, однако, встречаются внутримозговые геморрагии, расположенные в атипичных местах, что происходит в силу разрыва аневризмы, или на фоне церебральной амилоидной ангиопатии.
Таким образом, наличие лобарного (долевого) кровоизлияния даёт основание подозревать в дифференциально диагностическом ряду метастаз, манифестирующий кровоизлиянием. Ответом может служить обнаружение одной из вышеперечисленной причины кровоизлияния.
Так, амилоидная ангиопатия мозговых артериол приводит к формированию множественных мелких петехиальных кровоизлияний, хорошо обнаруживающихся на Т2* в виде мелких точечных очагов пониженной интенсивности МР-сигнала. Аневризма определяется в виде мешковидного выпячивания сосудистой стенки, визуализируемой на Т2 или на МРА.
Кроме того, очень помогает динамическое наблюдение за кровяным сгустком, который со временем уменьшается и оставляет после себя кисту, в отличии от кровоизлияния в метастаз, при котором могут возникать новые геморрагии, и не происходит уменьшения объёма поражения.

Внутримозговая гематома в субкортикальном белом веществе левой теменной доли, на фоне амилоидной ангиопатии, представленная
компактным сгустком повышенной плотности (звёздочка на рис.1745) и перифокальным отёком (головки стрелок на рис.1745). Гематома в левой височной доле, на фоне разрыва аневризмы левой средней мозговой артерии (звёздочки на рис.1746, 1747).

Метастаз с кровоизлиянием в строме опухоли обычно формирует неоднородную и неправильной формы гематому (звёздочка на рис.1748), сопровождающуюся несопоставимым с её размерами перифокальным отёком (головки стрелки на рис.1748). На Т2* так же визуализируется отложение гемосидерина в стенках гематомы (звёздочка на рис.1749). Контрастное усиление приводит к усилению участков опухоли на фоне кровоизлияния, что не происходит с гематомой, а так же позволят выявить скрытые очаги (головки стрелок на рис.1750).
Кавернозная ангиома (кавернома) - врожденная сосудистая мальформация, представляющая собой каверны, содержащие кровь, и имеющая периферическую зону отложения гемосидерина, продукта деградации гемоглобина. Для каверном не характерно увеличение размеров, однако они могут осложняться кровоизлиянием.

Кавернозная ангиома может быть множественная (головки стрелок на рис.1751), имеет пониженный МР-сигнал по Т2 и Т2*, что часто наблюдается по периферии крупных каверном (чёрная стрелка на рис.1753) и целиком представляет мелкие каверномы. Центр каверномы имеет повышенный МР-сигнал по Т1 и Т2 (головки стрелок на рис.1753). На КТ кавернома представлена неоднородной массой, гетерогенной повышенной плотности (стрелки на рис.1752), без чётких границ и без перифокального отёка, который характерен для опухолей и метастазов (головки стрелок на рис.1752). Контрастирование повышает интенсивность МР-сигнала от каверномы по Т1 (белые стрелки на рис.1753). Обратите внимание на последствие ОНМК в левой лобной доле (стрелка на рис.1751).
Ишемический инсульт обычно не представляет сложности в диагностике с помощью МРТ, однако множественные очаги ишемии, возникшие на фоне ангиопатии, вызванной сахарным диабетом, а так же атипичная форма областей инфаркта могут симулировать метастатическое поражение.
Метастаз меланомы в правой гемисфере мозжечка имеет относительно чёткие контуры, небольшой размер метастаза не приводит к возникновению перифокального вазогенного отёка (головка стрелки на рис.1754). Контрастирование вызывает интенсивную адсорбцию контраста и обозначает округлую структуру с чёткими контурами (головка стрелки на рис.1755). На DWI МР-сигнал от метастаза превышает интенсивность сигнала от мозговой ткани (головка стрелки на рис.1756), однако не значительно, что вариабельно, в зависимости от гистологической структуры опухоли, при этом интенсивность МР-сигнала на DWI от метастаза почти неизменна в динамическом наблюдении, но может понижаться из-за возникновения некротического распада центра метастаза.

Ишемический инсульт в правой гемисфере мозжечка в виде зоны, повышенного МР-сигнала по Т2 и Flair (стрелка на рис.1757), а так же не резко повышенный МР-сигнал по Т1 за счёт геморрагического пропитывания (головки стрелок на рис.1758, 1759). После внутривенного контрастного усиления определяется контрастирование, для которого характерен, так называемый, гиральный паттерн контрастирования [24] (стрелки на рис.1758, 1759). Кроме того, область острой ишемии имеет резко повышенный МР-сигнал по DWI (стрелка на рис.1756), постепенно ослабевающий при динамическом наблюдении. Так же, в ходе наблюдения за областью инфаркта, определяется эволюция ишемической зоны в участок энцефаломаляции и формирование зоны глиоза или кисты, в зависимости от размера.

Абсцесс мозга имеет центральное ограничение диффузии, гладкий ободок интенсивности на SWI [8]. На ПЭТ неопластические поражения наблюдаются с повышенной концентрацией РФП, а инфекционные заболевания, как правило, фотопеничны. Абсцесс мозга сопровождается клиникой интоксикации и возникает на фоне гематогенного инфекционного заноса, например, при сепсисе и наличии очага гнойного воспаления в организме, может быть следствием контактного распространения гнойного воспаления из придаточных полостей носа, при расплавлении костных стенок, а так же может быть вызван оппортунистической инфекцией на фоне иммуносупрессии, например, ВИЧ-инфекции.

Мозговой абсцесс определяется в виде образования (стрелка на рис.1760) с выраженным перифокальным отёком (головки стрелок на рис.1760), интенсивно накапливающий контрастный агент по типу кольца с ровным внешним и внутренним краем (стрелка на рис.1761), а так же обладает особенность значительно ограничивать диффузию, вызывая яркий МР-сигнал по DWI (стрелки на рис.1762). Крупный абсцесс (звёздочки на рис.1763, 1764) имеет выраженный перифокальный отёк (головки стрелок на рис.1763, 1764). На КТ абсцесс имеет пониженную плотность в центре (стрелки на рис.1765) и может быть двух-, трехкамерным.

Паразитарное поражение часто носит очаговый характер и представляет сложности при дифференциальной диагностике с метастазами. Паразиты, как правило, имеют невыраженное контрастирование (эхинококк не накапливает контраст). Имеется визуализация сколекса [88].

Множественные мелкие метастазы головного мозга (рис.1766), схожи по структуре с паразитарными очагами. В данном случае, представлены кисты цистицерков, имеющих минимальный перифокальный отёк, или без него (головки стрелок на рис.1767). Внутривенное контрастное усиление характерно, и выявляет сколексы (головки ленточного червя) в стенках кист (стрелки на рис.1768).

В завершении жизненного цикла цистицерк погибает, что сопровождается воспалительным отёком (головки стрелок на рис.1769) и обызвествлением кист (стрелки на рис.1769). Погибшая и обызвествленная эхинококковая киста в правой доле печени (головки стрелок на рис.1770). Эхинококковая киста в белом веществе левой лобной доли (головка стрелки на рис.1771).
Лучевой некроз представляет собой осложнение лучевой терапии, проведенной с линейного ускорителя. Область лучевого поражения может сопровождаться перифокальным отёком, увеличиваться при динамическом наблюдении и накапливать контрастный агент, то есть иметь все признаки продолженного опухолевого роста.
Точный ответ при оценке рецидива опухоли или осложнения лучевой терапии, важен для продолжения лучевой терапии, или её исключения. В дифференциации данных процессов важная роль принадлежит спектроскопии, оценивающей пик Lac и редукцию NAA в области продолженного опухолевого ростка, а в области лучевого некроза измерения демонстрируют редукцию всего спектра метаболитов. Так же, перфузионные исследования показывают высокие цифры CBV и CBF в области опухоли и участки сниженной перфузии в области лучевого некроза.

Обширный перифокальный отёк (головки стрелок на рис.1772), окружающий область глиозных изменений и лучевого некроза (стрелки на рис. 1773). Контрастное усиление при лучевом некрозе демонстрирует участки неправильной формы интенсивного накопления контрастного агента(стрелки на рис.1774).
Эозинофильная гранулёма - это грануломатозно-остеолитический процесс в кости, заболевание группы ретикуло-эндотелиальной системы. Процесс не обязан сопровождается эозинофилией периферической крови, клинические симптомы малоспецифичны. Поражение всех костных слоёв имеет округлую форму - “пробойники”, нет склероза и периостальной реакции.

Эозинофильная гранулёма может симулировать метастаз в кости черепа, однако она, чаще, солитарная, не сопровождается периостальной реакцией и поражает всю толщину плоскости кости свода черепа, как диплоэ, так и компактные пластинки (головки стрелок на рис.1775-1777).
Т2 сканы демонстрируют больше крупных бляшек, чем активных очагов Т1 с контрастным усилением. Большинство очагов при РС расположено в перивентрикулярной зоне, а метастазы в субкортикальном белом веществе.

Очаги рассеянного склероза, преимущественно, поражают белое вещество, чаще паравентрикулярных и юкстакортикальных участков мозга(головки стрелок на рис.1778), однако так же, но реже, могут поражать и кору мозга. Очаги демиелинизации сопровождаются перифокальным отёком, отличным от вазогенного (стрелки на рис.1778, 1779), что характерно для очагов в острой фазе воспалительной демиелинизации. Данные очаги расположены вдоль волокон лучистого венца, при динамическом наблюдении, могут увеличиваться и уменьшаться в размерах, крупные очаги формируют лакунарные ликворные кисты (так называемые “чёрные дыры”). При контрастном усилении патогномоничной чертой очага демиелинизации является накопление контрастного агента по типу незамкнутого кольца (стрелки на рис.1779, 1780).
Токсоплазмоз часто осложняет течение ВИЧ-инфекции, проявляясь наличием очагов с перифокальным отёком, и хорошо поддаётся антибактериальной терапии.

Очаги поражения токсоплазмоза в правой лобной доле и базальных ядрах правого полушария большого мозга (головки стрелок на рис.1781, 1782), окруженные перифокальным вазогенным отёком, интенсивно накапливающие контрастный агент (стрелки на рис.1783). На контрольном исследовании, после лечения бисептолом, через 2,5 месяца, отмечается существенный регресс размеров перифокального отёка (головки стрелок на рис.1784, 1785) и уменьшение очагов поражения в размерах, что убедительно отмечается на МРТ, в режиме Т1, после внутривенного контрастного усиления (стрелки на рис.1786).

Метастазы - очаги периферического распространения злокачественной опухоли с характерными чертами округлого образования, множественности поражения, перифокального отёка и масс-эффекта.
Локализуются в любом отделе ЦНС: супра- (80%) и инфратенториально (20%),субкортикально, в глубинных отделах, в САП и субэпендимарно [88]. Наиболее часто поражается лобная и теменная доля [48].
На сегодняшний день Т1 с контрастным усилением представляет собой лучший метод для обнаружения метастазов в головном мозге [4, 27, 151].
- карцинома легкого (50%),
- меланома кожи (30-40%),
- карцинома молочной железы (18-30%),
- рак почки,
- щитовидной железы,
- желудочно-кишечного тракта,
- мочевого пузыря.
На ранних стадиях заболевания, пациенты с метастатическими опухолями мозга, как правило, бессимптомны. Когда опухоли увеличиваются в размерах и развивается отёк - появляются симптомы [48].

Метастазы опухолей в мозг - очаги периферического распространения злокачественной опухоли с характерными чертами округлого образования, множественности поражения, перифокального отёка и масс-эффекта.

Контрастное усилением метастазов в головном мозге

Локализация метастазов в мозге

Источники метастазов в головной мозг

Клиническая картина, лечение и прогноз при метастазах в мозг

Внутричерепные метастазы являются осложнением рака с грозными последствиями. Томография мозга широко может быть использована для отбора больных с впервые выявленной злокачественной опухолью и для оценки пациентов с известными злокачественными новообразованиями, которые провоцируют развиваются неврологического дефицита.

Метастазирование может быть избирательным (поражается головной или спинной мозг) или тотальным. Располагаются метастазы в мозге беспорядочно, размеры их различны — от мелких до крупных узлов
Читайте также:

