Меланома кожи атлас клинико-морфологической диагностики

Меланома кожи. Атлас клинико-морфологической диагностики
А втор: Анисимов В. В., Горделадзе А.С., Барчук А.С.
Год издания: 1996
Размер: 3.66 МБ
Формат: djvu
Язык: Русский
Практическое руко водст во "Меланома кожи. Атлас клинико-морфологической диагностики" под ред., Анисимо ва В. В., и соавт., рассматривает развитие злокачественного процесса на коже, алгоритмы ее диагностики, возможности лечения. Представлена классификация данного заболевания, его клиническая картина, факторы риска развития онкопроцесса. Для студентов-медиков, онкологов, дерматовенерологов.
Меланома кожи. Атлас клинико-морфологической диагностики
А втор: Анисимов В. В., Горделадзе А.С., Барчук А.С.
Год издания: 1996
Размер: 3.66 МБ
Формат: djvu
Язык: Русский
Практическое руко водст во "Меланома кожи. Атлас клинико-морфологической диагностики" под ред., Анисимо ва В. В., и соавт., рассматривает развитие злокачественного процесса на коже, алгоритмы ее диагностики, возможности лечения. Представлена классификация данного заболевания, его клиническая картина, факторы риска развития онкопроцесса. Для студентов-медиков, онкологов, дерматовенерологов.
Меланома кожи. Атлас клинико-морфологической диагностики
А втор: Анисимов В. В., Горделадзе А.С., Барчук А.С.
Год издания: 1996
Размер: 3.66 МБ
Формат: djvu
Язык: Русский
Практическое руко водст во "Меланома кожи. Атлас клинико-морфологической диагностики" под ред., Анисимо ва В. В., и соавт., рассматривает развитие злокачественного процесса на коже, алгоритмы ее диагностики, возможности лечения. Представлена классификация данного заболевания, его клиническая картина, факторы риска развития онкопроцесса. Для студентов-медиков, онкологов, дерматовенерологов.
Меланома кожи. Атлас клинико-морфологической диагностики
А втор: Анисимов В. В., Горделадзе А.С., Барчук А.С.
Год издания: 1996
Размер: 3.66 МБ
Формат: djvu
Язык: Русский
Практическое руко водст во "Меланома кожи. Атлас клинико-морфологической диагностики" под ред., Анисимо ва В. В., и соавт., рассматривает развитие злокачественного процесса на коже, алгоритмы ее диагностики, возможности лечения. Представлена классификация данного заболевания, его клиническая картина, факторы риска развития онкопроцесса. Для студентов-медиков, онкологов, дерматовенерологов.
Меланома кожи. Атлас клинико-морфологической диагностики
А втор: Анисимов В. В., Горделадзе А.С., Барчук А.С.
Год издания: 1996
Размер: 3.66 МБ
Формат: djvu
Язык: Русский
Практическое руко водст во "Меланома кожи. Атлас клинико-морфологической диагностики" под ред., Анисимо ва В. В., и соавт., рассматривает развитие злокачественного процесса на коже, алгоритмы ее диагностики, возможности лечения. Представлена классификация данного заболевания, его клиническая картина, факторы риска развития онкопроцесса. Для студентов-медиков, онкологов, дерматовенерологов.
Анисимов В.В., Горделадзе А.С., Барчук А.С. и др. Меланома кожи. Атлас клинико-морфологической диагностики
Меланома кожи представляет собой злокачественную опухоль, возникающую в результате неопластической трансформации меланобластов и меланоцитов, являясь первым локальным проявлением общего неопластического заболевания всей меланоцитарной системы организма человека.
Показать полностью… На различных этапах развития онкологии данная опухоль описывалась в литературе под различными названиями: меланома, злокачественная меланома, меланобластома, меланокарцинома и меланоцитобластома. В настоящей монографии мы считаем возможным называть эту опухоль кожи Меланомой, подразумевая ее злокачественный характер. Для врачей всех специальностей и студентов медицинских вузов.
Меланома занимает особую роль среди злокачественных опухолей кожи, являясь социально значимой проблемой в связи с высоким уровнем летальности, что обусловлено значительным метастатическим потенциалом опухоли и низкой эффективностью терапии поздних форм заболевания [1]. Пятилетняя выживаемость больных меланомой на поздних стадиях не превышает 18,0%, а медиана продолжительности жизни — 7,8 мес. Диагностика на ранней стадии заболевания значительно улучшает прогноз [2].
Меланома может возникать как из меланоцитов некоторых вариантов невусов (диспластический невус, невус Рида, меланоз Дюбрейля), так и de novo, то есть на неизмененной коже.
В соответствии со стандартом оказания первичной медико-санитарной помощи при злокачественных новообразованиях кожи (меланома, рак) I–IV стадии (обследование в целях установления диагноза заболевания и подготовки к противоопухолевому лечению), утвержденным Приказом МЗ РФ от 20.12.2012 г. № 1143н, используются следующие методы обследования: осмотр кожи, дерматоскопия, цитологическое, морфологическое (гистологическое) исследования.
Однако в литературе недостаточно внимания уделяется проблеме диагностики меланомы на начальных этапах ее развития, описанию ранних диагностических признаков. Активное информирование населения и врачей различного профиля о потенциальной опасности пигментных образований кожи увеличивает число обращений пациентов и выявлений данного заболевания на ранних стадиях вследствие повышения онкологической настороженности [3].
В 1994 г. для дифференциальной диагностики меланомы предложены три оценочные системы (WHO Melanoma Program), включающие алгоритм ABCD, 7-точечную систему Glasgow, правило ФИГАРО.
7-точечная система Glasgow, разработанная исследователями из университета Glasgow (Шотландия) в 1989 г., включает изучение семи признаков новообразования, три из которых основные, а именно: 1) изменение размеров, объема; 2) изменение формы, очертаний; 3) изменение цвета; а также дополнительные, такие как: 4) воспаление; 5) образование корки или кровоточивости; 6) изменение ощущений, чувствительности; 7) диаметр более 7 мм. По данным исследований чувствительность метода составляет от 79,0% до 100,0% [4, 5].
Пациентка З., 31 год, обратилась на прием к дерматовенерологу по поводу атопического дерматита у своего ребенка, себя считала здоровой. Врач обратил внимание на коричневое новообразование на коже плеча.
Патоморфологическое описание: асимметричная общая структура, атипичные меланоциты расположены в эпидермисе преимущественно в верхних отделах сосочкового слоя дермы с ядерным плеоморфизмом в одиночку и гнездами. Заключение: пигментная меланома, уровень инвазии по Кларку II, толщина менее 1 мм по Бреслоу, без изъязвления (рис. 1а, б).
_575.png)
Данный случай демонстрирует характерные изменения клинической картины, дерматоскопические признаки меланомы кожи при отсутствии субъективных жалоб пациента.
.png)
Пациентка А., 67 лет, пенсионерка, жительница села. Самостоятельно обратилась к дерматовенерологу по месту жительства. Со слов пациентки, полгода назад отметила субъективные ощущения по типу парастезии пигментного невуса в области спины.
.png)
.png)
Пациент Щ., 71 год, пенсионер, житель села. Заметил образование на коже спины три месяца назад, когда новообразование стало мешать надевать одежду. За медицинской помощью не обращался. Новообразование стремительно увеличивалось в размерах, стало кровоточить, покрылось коркой, спустя 1,5 месяца самостоятельно наружно применял мазь Ацикловир в течение двух недель без эффекта. Обратился в районную поликлинику к онкологу, откуда был направлен в ГБУЗ СО СООД. Объективно: на коже верхней трети спины узел куполообразной формы, с гиперкератозом на поверхности, диаметром 10 см с перифокальным воспалением кожи. При обследовании у онколога проведена полная эксцизионная биопсия опухолевого образования с отступом от края опухоли с последующим морфологическим исследованием материала. Патоморфологическое описание препарата: узловая пролиферация атипичных меланоцитов, гнездное расположение клеток, плеоморфизм ядер и обильная цитоплазма. Заключение: пигментная меланома, уровень инвазии по Кларку II, толщина 0,5 см по Бреслоу, с изъязвлением. Обращает внимание, что данный пациент находится на диспансерном наблюдении у терапевта по поводу бронхиальной астмы; посещал врача 2–3 раза в год, проводилось аускультативное исследование, однако на консультацию к дерматовенерологу или онкологу с целью определения степени риска развития ЗОК направлен не был.
Таким образом, несвоевременная диагностика меланомы обусловлена отсутствием субъективных ощущений у больных на ранних стадиях заболевания, свидетельствует о недостаточном уровне противораковой пропаганды среди населения и онкологической грамотности медицинских работников общей лечебной сети. Результаты исследования обосновывают необходимость разработки дополнительных медико-организационных технологий по первичной и вторичной профилактике ЗОК.
.png)
Литература
М. А. Уфимцева* , 1 , доктор медицинских наук
В. В. Петкау**, кандидат медицинский наук
А. С. Шубина*
Д. Е. Емельянов**, кандидат медицинских наук
А. В. Дорофеев**, доктор медицинских наук
К. Н. Сорокина*, кандидат медицинских наук
* ФГБОУ ВО ФГБОУ ВО УГМУ МЗ Ф, Екатеринбург
** ГБУЗ СО СООД, Екатеринбург



Симптомы меланомы кожи
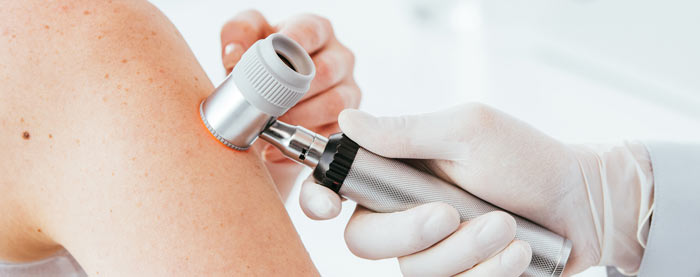
Определить, что это именно меланома, можно только при помощи дерматоскопа. Поэтому не поленитесь, сходите к врачу – он сможет осмотреть родинку на профессиональном оборудовании и поставить точный диагноз. Но для начала пройдите тест, который подскажет, есть ли у вас признаки меланомы.
Классификация меланомы кожи по стадиям
Лечение меланомы кожи
Если у вас нет возможности в ближайшее время попасть к специалисту, проверьте свои родинки по тесту ABCD. Врачи используют его уже много лет, и, хотя сейчас состояние подозрительной родинки можно проверить при помощи современной аппаратуры, тест вполне достоверный – пройдя его, вы сможете обнаружить подозрительные образования. Пройти тест ABCD можно онлайн по этой ссылке: checkyourskin.ru/abcde/. Если ваши подозрения подтвердились, при первой же возможности обратитесь к врачу.
Заподозрить меланому может как сам человек, так и любой врач при общем осмотре, но диагностировать ее может только онколог (онкодерматолог). Дело в том, что непрофильные врачи редко сталкиваются с таким заболеванием и не имеют специального оборудования - дерматоскопа (эпилюминесцентного микроскопа). При его использовании онколог смотрит сквозь верхний слой кожи и может с большим увеличением рассмотреть строение подозрительного новообразования.
Тест ABCD нужно проходить регулярно, периодически проверяя все свои старые родинки, – в любой момент они могут начать перерождение в меланому. И обязательно проверять все новые образования на коже. Помните: на поздних стадиях меланома не лечится, а вот на начальном этапе прогноз благоприятный. Современные методы терапии, которыми владеют квалифицированные врачи-онкологи, помогают справиться с меланомой. Найдите своего врача, который расскажет про современное лечение.
Профилактика меланомы
Основной и важнейший способ профилактики меланомы - защита от солнца. Считается, что единственный солнечный ожог, полученный даже в детстве, в дальнейшем повышает риски возникновения меланомы. Максимально эффективная защита от солнца включает в себя ограничение пребывания на солнце в часы его пиковой активности (днем), отказ от соляриев и использование солнцезащитных кремов даже в городе, и тем более на пляже. Необходимо убедиться, что крем защищает и от ультрафиолета А (УФА), и от ультрафиолета В (УФВ) (это указано на упаковке), и обладает солнцезащитным фактором (SPF) не ниже 15. На пляже крем нужно наносить не реже чем раз в два часа, а детям можно и чаще. В городе солнцезащитный крем на лицо и открытые участки тела нужно наносить не непосредственно перед выходом, а за 15 - 20 минут до этого.
Глаза тоже необходимо защищать от солнца, но правильно: темные очки должны быть куплены в надежном месте и иметь маркировку UV 400 или отметку о 100% защите от УФ-лучей.
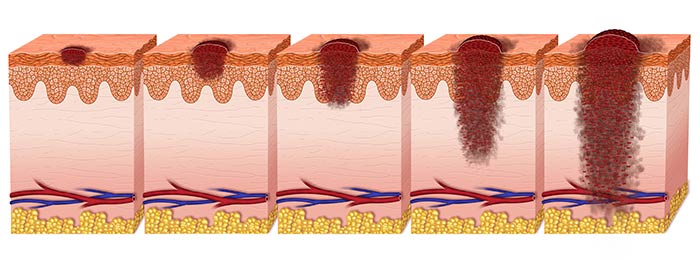
Беспигментная меланома встречается в 1,8-8,1% всех злокачественных меланоцитарных опухолей. Это новообразование отличается агрессивным ростом, поэтому его нужно начать лечить как можно раньше.
В Европейской клинике лечение беспигментной меланомы проводят по международным стандартам. В некоторых случаях пациенты могут принять участие в клинических испытаниях новых методов терапии.
- Беспигментная меланома — что из себя представляет?
- Причины и факторы риска
- Симптомы заболевания
- Зоны локализации образований
- Диагностика
- Классификация заболевания
- Стадии
- Осложнения и последствия болезни
- Лечение заболевания
- Прогноз и профилактика
Беспигментная меланома — что из себя представляет?
Меланому, содержащую мало меланина, отличает довольно быстрый рост в жировую клетчатку и раннее изъязвление. Это создает условия для метастазирования.
В клетках бесцветных меланом содержится небольшое количество меланина из-за:
- недостаточного содержания аминокислоты тирозина в организме;
- нарушения образования меланина в процессе деления клеток опухоли.
Причины и факторы риска
Единственной причины меланомы — как пигментной, так и беспигментной — не существует. В 5-12% случаев заболевание возникает под воздействием наследственной предрасположенности. Тогда потомкам передается один из генов, подвергшихся мутации. Основными из них являются:
- CDK4, отвечающий за выработку фермента, подавляющего развитие опухолей;
- CDKN2A, необходимый для нормального деления клеток.
Риск развития меланомы у родственников составляет 8-14%, если:
- беспигментную меланому диагностировали у двоих или более братьев (сестер) человека, особенно если они являются близнецами;
- злокачественное меланоцитарное образование было у обоих родителей;
- диагноз меланомы был поставлен двоим или большему количеству детей человека.
Большинство (около 90%) случаев развития меланомы приходится на спорадические, то есть не связанные с наследственной передачей, случаи. В этом случае причиной опухоли считают ультрафиолетовое излучение — лучи типа B и A.
Факторами риска злокачественных новообразований из клеток-меланоцитов являются:
- светлая кожа (I и II фенотип по Фитцпатрику), особенно в сочетании с рыжими волосами и веснушками;
- полученные солнечные ожоги (в том числе, и в раннем детстве);
- применение PUVA терапии (для лечения псориаза, витилиго);
- крупный врожденный невус — когда он занимает площадь более 5% (5 ладоней) площади тела;
- иммунодефицит — врожденный, вызванный приемом глюкокортикоидных препаратов или цитостатиков для лечения ревматоидного артрита, аутоиммунных заболеваний, для предупреждения отторжения трансплантата.
- голубой невус;
- невус Отта;
- диспластический невус;
- меланоз Дюбрейля;
- сложный пигментный невус;
- меланоз Пика.
Симптомы заболевания
Беспигментная меланома — это узелок на коже:
В отличие от пигментной меланомы, опухоль из меланоцитов без пигмента чаще всего более симметричная, она менее склонна к отеку и образованию вокруг нее небольших сосочков-сателлитов.
Самое опасное, что рост ахроматической меланомы отмечается не только вверх, но и вглубь кожи. Оно склонно к распаду. Поэтому на поздних стадиях опухоль выглядит как язва, края которой плотные и приподнятые, а на дне видны мелкие сосочки.
Первые симптомы беспигментной меланомы — возникновение на коже (чистой или в области пигментных образований) розового пятна. Такое пятно увеличивается в течение нескольких недель/месяцев, отличается повышенной рыхлостью и кровоточивостью.
Отдельные виды меланомы без пигмента выглядят как постепенно увеличивающаяся бородавка или папиллома. Другие беспигментные меланомы — как появление на ногте коричневой полоски, которая распространяется на кончик пальца.
На начальных стадиях беспигментные опухоли не болят и не зудят, поэтому на них редко обращают внимание.

Зоны локализации образований
Увидеть беспигментную меланому можно на любом участке кожи, в основном, в областях, открытых солнечному свету. Излюбленными местами локализации меланомы без пигмента являются:
- голени;
- пальцы;
- пятки;
- ступни;
- подошвы.
Диагностика
При малейшем подозрении на меланому нужно обратиться к врачу онкологу или дерматоонкологу. С помощью обследования, которое на первом этапе несложное и безболезненное, врач сможет отличить беспигментную меланому от похожих заболеваний: себорейного кератоза, пиогенной гранулемы, невуса Шпитца, базально-клеточного рака кожи, гемангиомы.
Первое, с чего начинают диагностику меланомы врачи Европейской клиники — осмотр образования. Дерматоонкологу нужно оценить внешний вид, консистенцию, симметричность, кровоточивость опухоли, прощупать ближайшие лимфоузлы.
Далее он собирает анамнез — узнает у пациента, когда появилось беспигментное новообразование, устанавливался ли диагноз меланомы у кого-то из ближайших родственников, часты ли были травмы опухоли, подвергалась ли она чрезмерной инсоляции.
На этом же этапе врач проводит цифровую дерматоскопию — осмотр опухоли с помощью специального прибора. Дерматоскоп увеличивает новообразование и позволяет проанализировать строение его глубоких слоев, оценить расположение и ход сосудов. Это очень важно для диагностики беспигментной меланомы.
Если по данным дерматоскопии нельзя исключить злокачественность опухоли, назначается второй этап диагностики. Это биопсия — получение опухолевой ткани для исследований. Выполняется она под местной анестезией и является эксцизионной. Это означает, что полностью удаляется и опухоль, и участок окружающей ткани.
Полученный с помощью биопсии участок изучается под микроскопом. Проводится также иммуногистохимическое исследование (ИГХ). Оно предполагает определение в образце ткани (биоптате) определенных типов белков, и это позволяет узнать вид меланомы и ее чувствительность к химиотерапевтическим препаратам.
При подтверждении диагноза беспигментной меланомы проводится третий этап диагностики — определение распространенности процесса (стадии опухоли). Для этого выявляют метастазы в лимфатические узлы и во внутренние органы:
После этого лимфоузел тщательно, с использованием в том числе и ИГХ-метода, исследуют под микроскопом. Если меланомных клеток не обнаруживается, значит, опухоль не отослала дочерние клетки за пределы занимаемой области.
- Метастазирование во внутренние органы
Оно определяется методами магнитно-резонансной (МРТ) и компьютерной (КТ) томографии.
Классификация заболевания
Существует пять морфологических типов меланомы:
- поверхностно-распространяющаяся;
- по типу злокачественного лентиго;
- узловая;
- подногтевая;
- акральнолентигинозная.
Каждый из этих видов может быть пигментным и беспигментным.
Определяют виды по исследованию биоптата.
Стадии
В своем развитии беспигментная меланома может пройти 4 стадии. Каждая из них, кроме четвертой, делится на несколько подстадий.
Определяются стадии по трем критериям:
- толщине опухоли (глубине ее прорастания в кожу);
- метастазам в регионарные лимфоузлы;
- метастазам во внутренние органы.
| Стадия | Толщина опухоли | Метастазы в регионарные лимфоузлы | Метастазы во внутренние органы |
| 0 | в пределах эпидермиса | нет | нет |
| I A | до сосочкового слоя дермы, сетчатый (глубокий) не затрагивает, язв нет | нет | нет |
| I B | проникает в глубокий слой дермы, возможно — в подкожную клетчатку (толщина — от 1 до 2 мм), язв нет | нет | нет |
| II A | толщина опухоли — от 1 до 2 мм, есть изъязвление или толщина от 2 до 4 мм, язв нет | нет | нет |
| II B | толщина от 2 до 4 мм, с изъязвлениями или толщина выше 4 мм, без язв | нет | нет |
| II С | толщина больше 4 мм, с изъязвлениями | нет | нет |
| III A | любая толщина, язв еще нет | есть микрометастазы в 1-3 регионарных лимфоузлах | нет |
| III B | любая толщина, без образования язвы | или макрометастазы в 1-3 регионарных лимфоузлах или метастазы в кожу возле опухоли, но без метастазов в регионарных лимфоузлах | нет |
| любая толщина, с образованием язвы | или микрометастазы в 1-3 регионарных лимфоузлах или метастазы в кожу возле опухоли, но без метастазов в регионарных лимфоузлах | нет | |
| III С | любая толщина, с изъязвлением | или микро- или макрометастазы в 2-3 регионарных лимфоузлах | нет |
| любая | метастазами поражено больше 3 регионарных лимфоузлов или есть несколько спаянных между собой пораженных лимфоузлов или есть метастазы в кожу возле опухоли при том, что они же есть и в регионарных лимфоузлах | нет | |
| IV | любого размера | любое количество | есть |
Осложнения и последствия болезни
Беспигментная меланома может осложниться отсевов дочерних опухолей, метастазов, во внутренние органы. Это приводит к ухудшению их работы:
- метастазы в легких ухудшают насыщение крови кислородом;
- метастазы в мозге вызывают судороги, изменение личности, нарушение движений и/или чувствительности конечностей. Дочерние опухоли в ствол мозга приводят к нарушению дыхания, сердцебиения, поддержания нормального уровня артериального давления;
- метастазы в кости вызывают сильные боли, разрушение костей, затруднение движений — вплоть до полной их невозможности;
- метастазы в печень приводят к нарушению пищеварения, пожелтению и зуду кожи, ухудшению работы мозга;
- метастазы в кожу вызывают болевой синдром.
Когда неоплазию обнаруживает иммунная система организма, развивается интоксикация. Она проявляется слабостью, снижением аппетита, сонливостью, тошнотой. Человек перестает нормально питаться, и тело не получает нужных ему для жизнедеятельности и для борьбы с опухолью нутриентов.
Через время развивается раковая кахексия — истощение. Оно проявляется потерей веса, постоянной слабостью, отсутствием аппетита. Кахексия еще больше ухудшает состояние человека, нарушает метаболизм и работу всех его внутренних органов.
Лечение заболевания
В Европейской клинике беспигментная меланома лечится по современным протоколам, с учетом стадии процесса:
- При I стадии заболевания проводится хирургическое удаление опухоли и ткани вокруг нее.
- При II стадии удаляют новообразование, дополнительно проверяют лимфоузлы на предмет раковых клеток. Если в лимфатических узлах обнаруживаются мутировавшие меланоциты, узлы удаляются. К лечению могут подключать фотодинамическую терапию, лучевую терапию. Здесь же — при наличии мутации в гене BRAF — проводится лечение BRAF-ингибиторами.
- III стадия лечится удалением опухоли и всех расположенных рядом лимфоузлов. Лечение дополняется химио- и радиотерапией. Подключается иммунотерапия и введение BRAF-ингибиторов. Обязательно проводится терапия, направленная на улучшение состояния и купирование симптомов.
- На IV стадии удаляются крупные опухоли и метастазы, если это необходимо. Назначается химио-, радиотерапия и паллиативное лечение. Обязательно проводится иммунотерапия.
Иммунопрепараты помогают организму бороться с онкологическим процессом. Даже при запущенных формах злокачественной меланоцитарной опухоли пациенты могут рассчитывать на успешное лечение.
При беспигментной меланоме, содержащей мутацию гена BRAF, в Европейской клинике проводится таргетная терапия препаратами BRAF-ингибиторами. Данные лекарственные средства подавляют прогрессирование опухоли и усиливают активацию иммунитета. Применяются BRAF-ингибиторы, начиная со IIC-III стадии. Они увеличивают долговременную выживаемость и рекомендованы к применению даже при неоперабельной опухоли или наличии отдаленных метастазов.
Терапия BRAF-ингибиторами проводится в течение длительного времени — 6-9 месяцев.
Прогноз и профилактика
Прогноз заболевания зависит от его размеров и количества метастазов. Так, при толщине опухоли менее 0,75 мм беспигментная меланома вылечивается полностью. Если новообразование распространяется на 0,75-1,6 мм в толщину, 5-летняя выживаемость составляет около 85%. Узелковая форма опухоли из-за ее быстрого прогрессирования имеет плохой прогноз.
Профилактика заключается в защите от ультрафиолевого излучения — одеждой, солнцезащитным кремом, избеганием загара. Если в роду наблюдались случаи злокачественных образований кожи, или у человека есть факторы риска меланомы, можно определить наличие мутаций в отдельных генах. Если результат будет положительным, придется быть крайне аккуратным в отношении загара, избегать травм кожи и, в особенности, повреждения пигментных образований.
В статье рассмотрены основные клинические аспекты классификации меланомы кожи, в том числе параметры, влияющие на стадирование, прогностические и предиктивные факторы, а также изменения в классификации TNM 8-го издания. Особое внимание уделено современным представлениям о генетических нарушениях при меланоме и стратегиям таргетной терапии.
В статье рассмотрены основные клинические аспекты классификации меланомы кожи, в том числе параметры, влияющие на стадирование, прогностические и предиктивные факторы, а также изменения в классификации TNM 8-го издания. Особое внимание уделено современным представлениям о генетических нарушениях при меланоме и стратегиям таргетной терапии.
Меланома – злокачественная опухоль, возникающая из трансформированных меланоцитов. Эти пигментпродуцирующие клетки имеют нейроэктодермальное происхождение и в процессе эмбриогенеза мигрируют из нервного гребешка в эпидермис и другие сайты, включая менингеальные, слизистые оболочки и сетчатку глаза.
Несмотря на то что меланома может развиваться в любой ткани, где в норме присутствуют меланоциты, кожная локализация остается наиболее распространенной – до 90% всех случаев заболевания [1].
Уровень заболеваемости в мире варьируется от 37 на 100 000 в Австралии до 0,2 на 100 000 в Южной и Центральной Азии. Это напрямую связано с уровнем инсоляции как ведущим фактором развития меланомы. Кроме того, имеет значение фототип кожи по Фитцпатрику, преобладающий среди населения [1].
К сожалению, в отличие от многих солидных опухолей заболеваемость меланомой растет. Так, в США, Великобритании, Швеции и Норвегии число случаев меланомы увеличилось более чем на 3% за последние несколько лет. По оценкам ряда авторов, такая тенденция сохранится по крайней мере до 2022 г. [2].
Прогноз заболевания зависит главным образом от стадии на момент постановки диагноза. При увеличении толщины опухоли по Бреслоу возрастает риск регионарных и отдаленных метастазов.
До недавнего времени приемлемо эффективной терапии для пациентов с метастатической меланомой не существовало. Фундаментальные открытия в области изучения генетических нарушений при меланоме привели к значительному увеличению продолжительности жизни больных с продвинутыми стадиями. Это делает молекулярную классификацию меланомы не только интересной с точки зрения научных изысканий, но и практически значимой при выборе индивидуализированной терапии.
Морфологическая классификация
Согласно морфологической классификации Всемирной организации здравоохранения, выделяют следующие гистологические типы первичной меланомы кожи: поверхностно распространяющуюся, узловую, меланому типа злокачественного лентиго, акрально-лентигинозную, невоидную, меланому у детей, десмопластическую, меланому, возникающую на фоне гигантского врожденного невуса, меланому, развивающуюся на фоне голубого невуса, персистирующую [3]. Среди всех подтипов наиболее распространены узловая и поверхностно распространяющаяся – до 85% всех случаев меланомы. В целом прогностической значимости между гистологическими подгруппами не отмечается, значение имеет скорее присущая каждой из них толщина опухоли [4]. Так, показатель по Бреслоу узловой меланомы выше такового поверхностно распространяющейся меланомы. В то же время прогноз злокачественного лентиго не лучше, чем у других гистотипов при их стратификации по толщине. Интересна связь морфологических особенностей строения меланомы и драйверной мутации [5]. Десмопластической меланоме присущи особенности морфологической и иммуногистохимической диагностики. Способность опухолевых клеток к пери- и интраневральному распространению обусловливает частые местные рецидивы после хирургического лечения [6].
Меланома детского возраста крайне редка, частота ее возникновения в возрасте до 15 лет около 1/1 000 000, или 1,2% всех случаев злокачественных опухолей в этой группе [7].
К акральным относят меланомы, развивающиеся на ладонях, подошвах, и подногтевые меланомы. На их долю приходится около 3% общего числа меланом. Этот тип наиболее выражен у чернокожих пациентов. Считается, что акральная локализация связана с неудовлетворительным прогнозом. Однако это скорее обусловлено не столько морфофенотипическими особенностями, сколько поздней диагностикой [8].
Злокачественное лентиго и злокачественная лентиго-меланома развиваются на коже, подвергающейся хроническому солнечному облучению, что предопределяет их преимущественную локализацию на лице, шее, голове. Кроме того, заболевания чаще наблюдаются у пациентов старшей возрастной группы [9].
Факторы, влияющие на стадию заболевания
Толщина по Бреслоу
Толщина первичной опухоли была введена как прогностический фактор Александром Бреслоу еще в 1970 г. Впоследствии ее значение было подтверждено в исследованиях [10].
Увеличение толщины означает рост метастатического риска и коррелирует со снижением выживаемости.
Установлено, что с увеличением толщины опухоли значительно уменьшается пяти- и десятилетняя выживаемость [4].
Изъязвление
Истинное изъязвление подразумевает комбинацию признаков: полнослойное повреждение эпидермиса (включая шиповатый слой и базальную мембрану), реактивные изменения (отложения фибрина, инфильтрация нейтрофилами, истончение или реактивная гиперплазия окружающего эпидермиса).
При оценке этого параметра важно учитывать анамнестические данные о наличии травмы или предшествующей биопсии образования.
Некоторые авторы рекомендуют указывать степень изъязвления в виде диаметра в миллиметрах или процентах к общему объему поражения. По данным C.M. Balch и соавт., пятилетняя выживаемость у пациентов с поверхностью изъязвления менее 6 мм составляет 44% (5% в группе с диаметром более 6 мм) (p 2 .
Сателлиты, транзитные метастазы
Сателлиты и транзитные метастазы представляют собой скопления в лимфатических сосудах опухолевых клеток меланомы диаметром более 0,05 мм, четко отграниченные от основного инвазивного компонента меланомы нормальной дермой или клетчаткой и расположенные на расстоянии не менее 0,3 мм от первичной опухоли. Структуры, удовлетворяющие названным критериям, расположенные на расстоянии до 2 см от опухолевого узла, относят к сателлитам, более 2 см, но расположенные до регионарных лимфатических узлов, – к транзитным метастазам. Сателлиты и/или транзитные метастазы служат фактором неблагоприятного прогноза, прежде всего за счет риска локорегионарного рецидива, и стадируются как N2c или N3 в зависимости от наличия или отсутствия поражения регионарных лимфатических узлов.
Все остальные кожные метастазы, не подпадающие под указанные критерии, относятся к отдаленным и стадируются как М1.
Факторы, влияющие на прогноз
Согласно данным AJCC, прогностические параметры обязательно отражаются в гистологическом заключении.
Уровень инвазии по Кларку
Выделяют пять анатомических уровней инвазии по Кларку в соответствии с наибольшей степенью инвазии опухолевых клеток.
Согласно AJCC7, митотическая активность по сути заменяет уровень Кларка в качестве параметра, влияющего на стадию Т1 в отсутствие изъязвления [4].
Исключение составляют случаи, когда изъязвление отсутствует и пролиферативная активность не может быть измерена. Уровень инвазии по Кларку 4 или 5 в такой ситуации позволяет отнести меланому к Т1b.
Фаза роста
Узловые меланомы не имеют фазы радиального роста [16].
Лимфоцитарная инфильтрация
По данным многочисленных исследований, наличие опухоль-инфильтрирующих лимфоцитов связано с более благоприятным прогнозом [17, 18]. Кроме того, выраженная лимфоцитарная инфильтрация ассоциирована с менее частым обнаружением позитивных сигнальных лимфатических узлов [19]. По степени и расположению лимфоцитарного инфильтрата в опухоли выделяют:
- brisk – лимфоциты диффузно инфильтрируют всю опухоль, разбивая ее на группы или отдельные клетки (непрерывная инфильтрация всего периферического края);
- non-brisk – лимфоциты инфильтрируют опухоль только фокально (прерывистая/неполная инфильтрация периферического края);
- absent – лимфоциты присутствуют, но не инфильтрируют опухоль (отсутствие лимфоцитарной инфильтрации).
Регрессия
При меланомах феномен регрессии встречается в шесть раз чаще, чем при других солидных опухолях [20]. Точка в споре о прогностическом значении этого параметра до сих пор не поставлена. Одни авторы регрессию в тонких меланомах связывают, как правило, с метастазированием [21], другие подобной корреляции не обнаруживают [22].
Данные последних исследований показывают, что в основе регрессии лежит активация иммунных механизмов защиты. Кроме того, наличие регрессии обусловлено уменьшением риска поражения позитивных лимфатических узлов [23].
Морфологически регрессия проявляется в виде вариабельного разрушения клеток меланомы с частичным или почти полным отсутствием опухолевых клеток в дерме, вариабельного лимфогистиоцитарного инфильтрата, фиброза в дерме, меланофагоцитоза, отека и вертикально ориентированных эктатических кровеносных сосудов [24].
Полный регресс опухоли стадируется как T0.
Лимфоваскулярная инфильтрация и нейротропизм
Лимфоваскулярная инвазия определяется наличием клеток меланомы в просвете лимфатических или кровеносных сосудов. В первичной меланоме она связана с более высоким риском метастазов в лимфатических узлах, а также сателлитов и транзитных метастазов [25], хотя это подтверждается не всеми авторами. В исследовании F. Tas и K. Erturk с участием 705 пациентов показано влияние лимфоваскулярной инвазии на безрецидивную и общую выживаемость [26].
Определение нейротропизма включает наличие клеток меланомы вокруг нервных волокон (периневральная инвазия) или внутри волокон (интраневральная инвазия). Периневральная инвазия/нейротропизм коррелирует с более высокой частотой рецидивов [27].
Изменения в 8-й редакции TNM
С 2018 г. вступит в силу 8-я редакция TNM [28].
Т (tumor)
Изменения коснулись и непосредственно порядка измерения. Значение толщины рекомендовано указывать с точностью до 0,1 знака после запятой. Измерение до 0,01 мм имеет низкую воспроизводимость. Исключением может быть меланома толщиной менее 1 мм.
N (nodus)
Метастазы, определяемые только по результатам биопсии сигнального лимфатического узла, стадируются на N1a, N2a, N3a в зависимости от количества пораженных узлов. Клинически определяемые метастазы стадируются на N1b, N2b, N3b также в зависимости от количества пораженных узлов. Особое внимание уделено сателлитам и транзитным метастазам. При их наличии имеют место стадии N1с, N2с, N3с в зависимости от статуса регионарных лимфатических узлов.
При подгрупповом анализе выживаемости пациентов со стадией III заболевания с учетом одновременно категорий Т и N выделена новая подгруппа IIID (T4bN3a/b/cM0) с самым неблагоприятным прогнозом.
M (metastasis)
При определении М-критерия значение имеют локализация отдаленных метастазов и уровень лактатдегидрогеназы (ЛДГ).
M1a – поражение кожи и мягких тканей, включая мышцы, M1b – поражение легких, M1c – поражение других висцеральных органов, кроме центральной нервной системы (ЦНС).
В новой редакции в отдельную группу M1d выделены пациенты с метастатическим поражением ЦНС как самую прогностически неблагоприятную. Уровень ЛДГ указывается и влияет на субкатегории при любом анатомическом сайте метастатического поражения M1a/b/c/d (0/I).
Молекулярно-генетическая классификация меланомы кожи
Современный уровень знаний в области молекулярной биологии меланомы и связанные с этим успехи таргетной терапии диктуют необходимость разделения меланомы кожи на молекулярно-генетические подтипы.
С практической точки зрения целесообразно выделять меланому кожи с мутациями BRAF V600, RAS и KIT. Данные мутации определяют активацию MAP-киназного каскада, отвечающего за пролиферацию и прогрессию клеточного цикла, и лежат в основе современной таргетной терапии (рисунок). Частота встречаемости различных мутаций зависит от локализации меланомы и характера ультрафиолетового воздействия (табл. 1) [29].
Мутации в гене BRAF являются наиболее частыми активирующими мутациями у пациентов с меланомой кожи (более 50%) и могут обнаруживаться как в первичном очаге, так и в метастазах [29, 30]. По данным Российской скрининговой программы, мутация BRAF встречается с частотой 60,6% (627 мутаций из 1035 исследований), чаще у молодых пациентов (до 50 лет – 72,9%, старше 50 лет – 57,1%; p = 0,00003). В возрастной группе 30–39 лет частота мутации BRAF достигает 81% [31]. Подавляющее большинство мутаций в гене BRAF определяются в кодоне V600 (табл. 2) [29]. Это, с одной стороны, существенно облегчает диагностику, с другой – предопределяет сходные конформационные изменения белка, приводящие к активации сигнального каскада, и позволяет разработать единый подход к таргетной терапии. В исследовании BRIM3 отмечалась сопоставимая эффективность таргетной терапии при мутациях BRAF V600E/K [32]. Эффективность ингибиторов BRAF при других типах мутаций требует дальнейшего изучения ввиду незначительного числа наблюдений. Оптимальной стратегией таргетной терапии меланомы кожи при наличии мутаций BRAF V600E/K на сегодняшний день считается комбинация ингибиторов BRAF и MEK (дабрафениб + траметиниб или вемурафениб + кобиметиниб) [33, 34].
Мутация в гене рецепторной тирозинкиназы c-KIT может играть ключевую роль в патогенезе до 20% меланом слизистой локализации и до 15% – акральной [29]. До 73% мутаций составляют пять hot-spot-мутаций в кодонах 6, 11, 13, 17 и 18, и частота объективного ответа на ингибиторы с-KIT (иматиниб, нилотиниб) может достигать 16–29% [38].
Наиболее фундаментальной является генетическая классификация меланомы кожи, разработанная коллективом авторов в рамках Cancer Genom Atlas Network (TCGA) [39]. На основании полногеномного изучения ДНК и экспрессионного анализа РНК, микро-РНК и протеинов 333 опухолевых образцов меланомы от 331 пациента (67 первичных и 266 метастатических меланом) было выделено четыре генетических подтипа в зависимости от ведущих повреждений генома: BRAF-мутированная, RAS-мутированная, NF1-мутированная и трижды негативная (triple-wild-type) меланома. Интересно, что мутационная нагрузка при меланоме выше, чем при других типах опухолей, изученных ранее по программе TCGA. До 76% мутаций в первичных меланомах и 84% мутаций в метастатических меланомах связаны с ультрафиолетовым воздействием.
BRAF-подтип считается самым распространенным (52%) и характеризуется hot-spot-мутациями в гене BRAF (V600E, V600K, V600R, K601) и более молодым возрастом пациентов.
Второй по распространенности RAS-подтип (28%) характеризуется hot-spot-мутациями (Q61, G12, G13) и гиперэкспрессией AKT3-сигналинга.
Triple-wild-type – самый редкий подтип (6%). При таком подтипе имеют место мутации и амплификации гена KIT, PDGFRa, VEGFR1, GNA11 и GNAQ. Данный подтип имеет низкие показатели сигнатур, ассоциированных с ультрафиолетовой компонентой (30% против > 90% для остальных трех типов), и высокую частоту изменения копийности генов и сложных комплексных перестроек.
Следует отметить, что частота гиперэкспрессии иммунных сигнатур и лимфоидной инфильтрации сопоставима при всех генетических подтипах и служит основным благоприятным прогностическим фактором.
Клиническое значение генетической классификации меланомы кожи отражено в табл. 3 [39].
Читайте также:

